長期記憶の形成における脳領域に特異的な遺伝子発現の制御機構
野中美応・尾藤晴彦
(東京大学大学院医学系研究科 神経生化学分野)
email:野中美応
DOI: 10.7875/first.author.2014.131
Region-specific activation of CRTC1-CREB signaling mediates long-term fear memory.
Mio Nonaka, Ryang Kim, Hotaka Fukushima, Kazuki Sasaki, Kanzo Suzuki, Michiko Okamura, Yuichiro Ishii, Takashi Kawashima, Satoshi Kamijo, Sayaka Takemoto-Kimura, Hiroyuki Okuno, Satoshi Kida, Haruhiko Bito
Neuron, 84, 92-106 (2014)
長期記憶の形成には遺伝子の発現が必要である.この過程において重要な転写因子のひとつにCREBがある.今回,筆者らは,CREBの転写補助因子であるCRTC1に着目し,このタンパク質のニューロンにおける制御機構および転写の増強の作用機序について調べた.さらに,マウスの個体の脳においてCRTC1-CREBシグナル伝達経路が脳領域に特異的にはたらくことを見い出した.具体的には,海馬および扁桃体が必要とされる文脈依存的な恐怖条件づけという長期記憶の学習課題において,扁桃体においては学習に応じたCRTC1の活性化がみられたが,海馬においてはみられなかった.これと一致して,脳領域に特異的にCRTC1の発現を抑制したところ,扁桃体においてはCRTC1の寄与が大きかったのに対し,海馬においては小さいことがわかった.このような脳領域に特異的な転写補助因子の動態により,脳の全域に普遍的に存在するCREBという転写因子が脳領域に特異的に遺伝子発現を制御することを可能にしていることが示唆された.
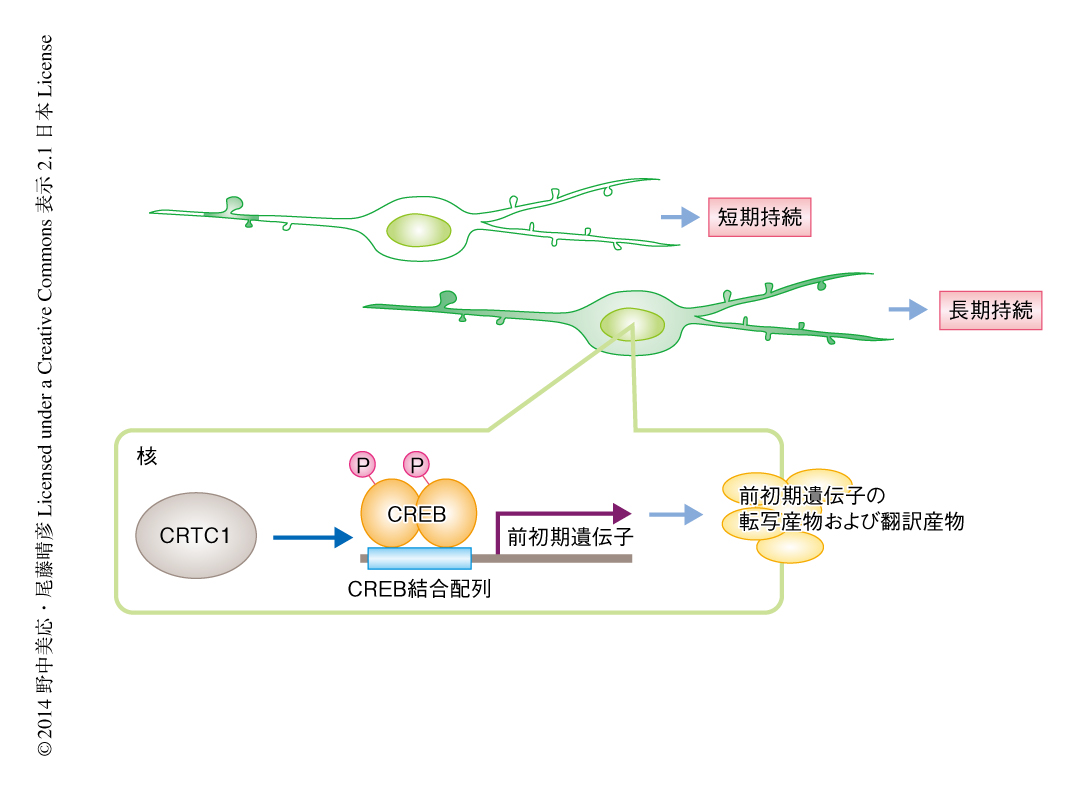
記憶が形成されるときには脳のなかで変化が起こる.とくに,翌日も覚えているような記憶が形成されるときには,シナプスにおけるシグナル伝達や短期間のあいだ持続するような変化が起こるだけでなく,核へとシグナルが伝達し,新たな遺伝子発現およびタンパク質生合成が行われる(図1).この過程において神経活動に依存的に遺伝子発現を誘導する代表的な転写因子としてCREBがある.CREBはアメフラシ,ショウジョウバエから哺乳類にいたるまで,さまざまな種において記憶および学習にかかわるとされている1).CREBの活性化の分子機構は133番目のSerのリン酸化による転写補助因子CBPや転写開始複合体との結合とされてきたが,それだけでは説明できないCREBのもつDNA結合ドメインの寄与が明らかになってきた.近年,CREBのDNA結合ドメインに結合するCRTCという新規の転写補助因子が報告された2,3).CRTCは線虫やショウジョウバエにおいても保存されており,それぞれ,寿命や記憶にかかわるCREBの転写の制御を担うことが示された4,5).哺乳類は3つのアイソフォームCRCT1~CRCT3をもち,中枢神経系においてはおもにCRTC1が発現している.この研究では,哺乳類のニューロンにおけるCRTC1による遺伝子発現の制御のシグナル伝達系および作用機序と,長期記憶における役割について調べた.
CRTC1は21.1%ものSerおよびThrを含み,高度にリン酸化されたタンパク質である.先行するCRTC2の研究により,膵臓や肝臓ではCRTCの脱リン酸化が核への移行をひき起こすことが知られていた3,6).しかし,脳神経系にて記憶の形成におけるCRTC1の動態を調べるためには,ニューロンにおいてそのリン酸化部位および制御のシグナル伝達系を明らかにしなければならない.どんどん増える株化された培養細胞とは異なり,マウスやラットの胎仔の脳から樹立する初代培養ニューロンは量産することができず,生化学的な実験がむずかしい.まず,ウェスタンブロッティング法によるバンドのようすから,CRTC1は神経活動が休止した状態においては高度にリン酸化されていることが推測されたため,テトロドトキシンにより神経活動を抑制した試料を回収しCRTC1を精製した.免疫沈降法に用いる抗体および溶出法について綿密に検討し,ゲル電気泳動および切り出しをしないことによりペプチドを最大限に回収するなど,さまざまにくふうした.いちどの試料の調製から質量分析にて数回分の量しか精製できなかったが,CRTC1のリン酸化部位の同定に成功した.同定された11箇所のリン酸化部位のうち,神経活動に依存してリン酸化の状態が変化する部位を生化学的な手法によりスクリーニングし,重要なリン酸化部位としてSer151およびSer245を同定した.これら2つの部位をAlaに置換すると神経活動がなくてもCREBに依存的な転写を活性化できたことから,この2つのSerをともにAlaに置換した変異体を活性型CRTC1として用いた.
CRTC1は神経活動に依存して核へと移行し,CREBを介した転写活性を増強させる7).では,CRTC1を制御する直上のシグナルはどのようになっているのだろうか? すでに脳神経系においても先行研究が報告されていたが7,8),Ca2+依存的脱リン酸化酵素であるカルシニューリンがCRTC1の核への移行に必須であることが確認された.CRTC1のリン酸化酵素としてはSIK2やAMPKが知られていたが8),CRTC1の核への移行に影響を及ぼすキナーゼ阻害剤およびキナーゼ活性化剤をさらに探索した.その結果,AMPKの活性化剤であるフェンホルミンがCRTC1の核への移行を完全に阻害すること,AMPKの阻害剤であるコンパウンドCが神経活動に共存することでCRTC1の核への移行を促進することを発見した.さらに,AMPKに関連するキナーゼのひとつであるMARK2の関与が明らかにされた.
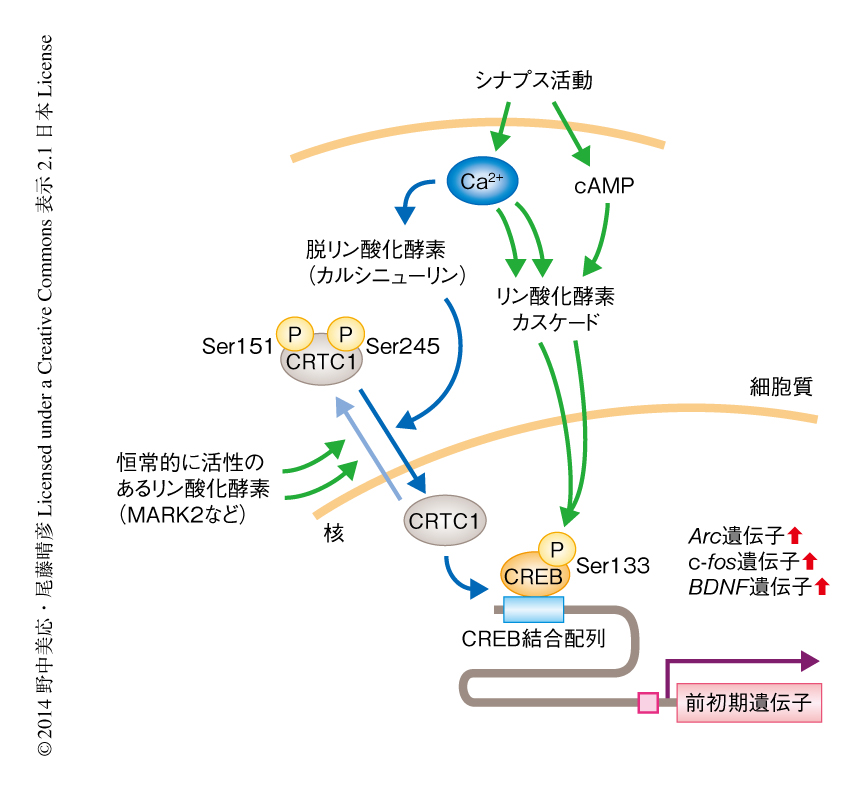
CREBの活性化においてはSer133のリン酸化がスイッチであるとされてきた.したがって,CRTC1によるCREBの転写活性の増強がCREBのSer133のリン酸化を介しているかどうかは重要なポイントであった.まず,活性型CRTC1を発現したニューロンにおいてCREBのSer133のリン酸化はとくに上昇していないことが確かめられた.しかし,この実験では活性型CRTC1を数時間以上も発現させていたため,誘導されたCREBに依存的な遺伝子発現による負のフィードバックによりCREBのSer133のリン酸化が抑制された可能性など,議論の余地があった.そこで,神経活動とは無関係にタモキシフェン誘導体の投与により核へと移行するCRTC1変異体を作製した.神経活動が休止している状態においてタモキシフェン誘導体を投与すると,このCRTC1変異体は急速に核へと移行しCREBに依存的な転写や下流の遺伝子であるc-fos遺伝子の発現を誘導したが,このとき,CREBのSer133はリン酸化されていなかった.このことから,CRTC1の核への移行はCREBに依存的な転写活性を誘導することができ,そのときCREBのSer133のリン酸化を介さないことが示された.しかし,転写リポーターアッセイにより,CRTC1の核への移行により活性化される転写は,神経活動がくわわるとさらに増強されることも明らかにされた.よって,生理的な条件においては,CRTC1の核への移行とCREBのSer133のリン酸化に収斂するリン酸化カスケード,あるいは,ほかの神経活動に依存的なシグナル伝達経路が協同的にCREBに依存的な転写を担うと考えられた(図2).
CREBはc-fos遺伝子やArc遺伝子といったニューロンにおける前初期遺伝子の発現を誘導する.活性型CRTC1の発現により,c-fos遺伝子やArc遺伝子の発現が誘導されることが培養ニューロンおよび個体の脳において示された.しかし,これら前初期遺伝子の発現に対するCRTC1の直接の制御を証明するには,CRTC1がDNAにおいてこれら前初期遺伝子の制御領域に結合することを示さねばならなかった.そこで,クロマチン免疫沈降アッセイを行ったところ,神経活動を誘導したニューロンにおいて,CRTC1の免疫沈降によりc-fos遺伝子,Arc遺伝子,zif268遺伝子,BDNF遺伝子のプロモーターのCREB結合配列を含む断片が共沈降された.
CRTC1はCREBに特異的な転写補助因子なのだろうか? さきに,CRTC1はCREBの転写補助因子であると述べたが,CREBのほかの転写因子にも作用する可能性は否定されていなかった.そこで,A-CREBというCREBに特異的な阻害ペプチドによりCRTC1による転写の増強が完全に抑制されること,および,機能的なCREB結合配列を1箇所のみもつArc遺伝子プロモーターにおいてCREB結合配列に変異を導入するとCRTC1による転写の増強が抑制されること,の2つの方法により,CRTC1の作用がCREBに特異的であるということが証明された.
CRTC1による前初期遺伝子の発現の誘導がCREBのSer133のリン酸化とは独立したシグナル伝達経路による場合,CRTC1を介したCREBの活性化の意義は何だろうか? ひとつには,さきに述べたように,CRTC1はCREBとは独立したシグナル伝達経路による制御をうけることができるという点があげられた.つねに核に局在しSer133の1箇所のリン酸化により活性化されるCREBとは対照的に,CRTC1は神経活動が休止した状態において高度にリン酸化されており,神経活動に依存的なカルシニューリン活性により脱リン酸化されて核へと移行する.CREBのSer133のリン酸化だけでもPKA,ERK,MSK,CaMKIV,CaMKIIなど多くのリン酸化酵素の制御をうけているが9),転写補助因子による制御をくわえることにより制御の幅はさらに広がる.CREBは全身に発現し,その標的となる遺伝子は4000ともいわれるが,部位と発生段階に応じて多種多様な役割を演じ分けることができる1,3).CRTC1などの転写補助因子がこの状況に応じた遺伝子発現の制御を手助けしている可能性がある.
そこで,文脈依存的な恐怖条件づけという長期記憶の学習課題にかかわる海馬および扁桃体において,マウスの個体におけるCRTC1の局在について調べた.その結果,扁桃体では連合学習に応じたCRTC1の核への移行がみられたが,海馬ではみられなかった.これらの脳領域においてCRTC1をノックダウンしたところ,扁桃体においてCRTC1を欠くと記憶の低下がみられたが,海馬においては記憶に変化はみられなかった.つまり,扁桃体および海馬は長期記憶の形成における責任領域であるが,扁桃体においてCRTC1は核へと移行し記憶の形成に必要であったが,海馬においてCRTC1は必要とされなかった.しかし,CRTC1は海馬にも発現しており,より強い刺激をあたえると核へと移行した.そこで,海馬に活性型CRTC1を発現させたところ記憶の向上がみられた.扁桃体において活性型CRTC1を発現させても記憶の向上はみられなかった(図3).このように,CRTC1には脳領域に特異的な機能のあることが明らかになった.
今回,筆者らは,CRTC1という転写補助因子に着目し,個体における脳領域に特異的な動態を明らかにした.転写因子に関連する認知記憶の分野における最近の動向にてらしあわせ,転写補助因子は状況に応じて転写因子の機能を制御する不可欠なタンパク質であるという流れにそい,その一例を具体的に示すことができた10).CRTC1はアルツハイマー病にも関連しており11),さらには,末梢神経系に発現したCRTC1が投射先の膵臓において糖尿病にかかわる代謝制御をし,ひいては,寿命にもかかわるとの報告もあり12),CRTC1は認知力の向上や代謝異常の改善など,新たな創薬の標的としても期待される.
略歴:2007年 京都大学大学院理学研究科 修了,同年 東京大学大学院医学系研究科 研究員,同 特任助教を経て,2012年より英国Edinburgh大学 ポスドク研究員.
研究テーマ:記憶をつかさどる分子機構を分子レベルから個体レベルまで縦断的に理解する.
関心事:海外にいながらにして美食・美酒を探求すること.
尾藤 晴彦(Haruhiko Bito)
東京大学大学院医学系研究科 教授.
研究室URL:http://www.neurochem.m.u-tokyo.ac.jp/
© 2014 野中美応・尾藤晴彦 Licensed under CC 表示 2.1 日本
(東京大学大学院医学系研究科 神経生化学分野)
email:野中美応
DOI: 10.7875/first.author.2014.131
Region-specific activation of CRTC1-CREB signaling mediates long-term fear memory.
Mio Nonaka, Ryang Kim, Hotaka Fukushima, Kazuki Sasaki, Kanzo Suzuki, Michiko Okamura, Yuichiro Ishii, Takashi Kawashima, Satoshi Kamijo, Sayaka Takemoto-Kimura, Hiroyuki Okuno, Satoshi Kida, Haruhiko Bito
Neuron, 84, 92-106 (2014)
要 約
長期記憶の形成には遺伝子の発現が必要である.この過程において重要な転写因子のひとつにCREBがある.今回,筆者らは,CREBの転写補助因子であるCRTC1に着目し,このタンパク質のニューロンにおける制御機構および転写の増強の作用機序について調べた.さらに,マウスの個体の脳においてCRTC1-CREBシグナル伝達経路が脳領域に特異的にはたらくことを見い出した.具体的には,海馬および扁桃体が必要とされる文脈依存的な恐怖条件づけという長期記憶の学習課題において,扁桃体においては学習に応じたCRTC1の活性化がみられたが,海馬においてはみられなかった.これと一致して,脳領域に特異的にCRTC1の発現を抑制したところ,扁桃体においてはCRTC1の寄与が大きかったのに対し,海馬においては小さいことがわかった.このような脳領域に特異的な転写補助因子の動態により,脳の全域に普遍的に存在するCREBという転写因子が脳領域に特異的に遺伝子発現を制御することを可能にしていることが示唆された.
はじめに
記憶が形成されるときには脳のなかで変化が起こる.とくに,翌日も覚えているような記憶が形成されるときには,シナプスにおけるシグナル伝達や短期間のあいだ持続するような変化が起こるだけでなく,核へとシグナルが伝達し,新たな遺伝子発現およびタンパク質生合成が行われる(図1).この過程において神経活動に依存的に遺伝子発現を誘導する代表的な転写因子としてCREBがある.CREBはアメフラシ,ショウジョウバエから哺乳類にいたるまで,さまざまな種において記憶および学習にかかわるとされている1).CREBの活性化の分子機構は133番目のSerのリン酸化による転写補助因子CBPや転写開始複合体との結合とされてきたが,それだけでは説明できないCREBのもつDNA結合ドメインの寄与が明らかになってきた.近年,CREBのDNA結合ドメインに結合するCRTCという新規の転写補助因子が報告された2,3).CRTCは線虫やショウジョウバエにおいても保存されており,それぞれ,寿命や記憶にかかわるCREBの転写の制御を担うことが示された4,5).哺乳類は3つのアイソフォームCRCT1~CRCT3をもち,中枢神経系においてはおもにCRTC1が発現している.この研究では,哺乳類のニューロンにおけるCRTC1による遺伝子発現の制御のシグナル伝達系および作用機序と,長期記憶における役割について調べた.
1.質量分析によるCRTC1のリン酸化部位の同定
CRTC1は21.1%ものSerおよびThrを含み,高度にリン酸化されたタンパク質である.先行するCRTC2の研究により,膵臓や肝臓ではCRTCの脱リン酸化が核への移行をひき起こすことが知られていた3,6).しかし,脳神経系にて記憶の形成におけるCRTC1の動態を調べるためには,ニューロンにおいてそのリン酸化部位および制御のシグナル伝達系を明らかにしなければならない.どんどん増える株化された培養細胞とは異なり,マウスやラットの胎仔の脳から樹立する初代培養ニューロンは量産することができず,生化学的な実験がむずかしい.まず,ウェスタンブロッティング法によるバンドのようすから,CRTC1は神経活動が休止した状態においては高度にリン酸化されていることが推測されたため,テトロドトキシンにより神経活動を抑制した試料を回収しCRTC1を精製した.免疫沈降法に用いる抗体および溶出法について綿密に検討し,ゲル電気泳動および切り出しをしないことによりペプチドを最大限に回収するなど,さまざまにくふうした.いちどの試料の調製から質量分析にて数回分の量しか精製できなかったが,CRTC1のリン酸化部位の同定に成功した.同定された11箇所のリン酸化部位のうち,神経活動に依存してリン酸化の状態が変化する部位を生化学的な手法によりスクリーニングし,重要なリン酸化部位としてSer151およびSer245を同定した.これら2つの部位をAlaに置換すると神経活動がなくてもCREBに依存的な転写を活性化できたことから,この2つのSerをともにAlaに置換した変異体を活性型CRTC1として用いた.
2.CRTC1の局在を制御するシグナル伝達経路およびシグナルタンパク質の同定
CRTC1は神経活動に依存して核へと移行し,CREBを介した転写活性を増強させる7).では,CRTC1を制御する直上のシグナルはどのようになっているのだろうか? すでに脳神経系においても先行研究が報告されていたが7,8),Ca2+依存的脱リン酸化酵素であるカルシニューリンがCRTC1の核への移行に必須であることが確認された.CRTC1のリン酸化酵素としてはSIK2やAMPKが知られていたが8),CRTC1の核への移行に影響を及ぼすキナーゼ阻害剤およびキナーゼ活性化剤をさらに探索した.その結果,AMPKの活性化剤であるフェンホルミンがCRTC1の核への移行を完全に阻害すること,AMPKの阻害剤であるコンパウンドCが神経活動に共存することでCRTC1の核への移行を促進することを発見した.さらに,AMPKに関連するキナーゼのひとつであるMARK2の関与が明らかにされた.
3.CRTC1とCREBのSer133のリン酸化との関係
CREBの活性化においてはSer133のリン酸化がスイッチであるとされてきた.したがって,CRTC1によるCREBの転写活性の増強がCREBのSer133のリン酸化を介しているかどうかは重要なポイントであった.まず,活性型CRTC1を発現したニューロンにおいてCREBのSer133のリン酸化はとくに上昇していないことが確かめられた.しかし,この実験では活性型CRTC1を数時間以上も発現させていたため,誘導されたCREBに依存的な遺伝子発現による負のフィードバックによりCREBのSer133のリン酸化が抑制された可能性など,議論の余地があった.そこで,神経活動とは無関係にタモキシフェン誘導体の投与により核へと移行するCRTC1変異体を作製した.神経活動が休止している状態においてタモキシフェン誘導体を投与すると,このCRTC1変異体は急速に核へと移行しCREBに依存的な転写や下流の遺伝子であるc-fos遺伝子の発現を誘導したが,このとき,CREBのSer133はリン酸化されていなかった.このことから,CRTC1の核への移行はCREBに依存的な転写活性を誘導することができ,そのときCREBのSer133のリン酸化を介さないことが示された.しかし,転写リポーターアッセイにより,CRTC1の核への移行により活性化される転写は,神経活動がくわわるとさらに増強されることも明らかにされた.よって,生理的な条件においては,CRTC1の核への移行とCREBのSer133のリン酸化に収斂するリン酸化カスケード,あるいは,ほかの神経活動に依存的なシグナル伝達経路が協同的にCREBに依存的な転写を担うと考えられた(図2).
4.CRTC1の遺伝子プロモーターへの結合およびCREBの特異性
CREBはc-fos遺伝子やArc遺伝子といったニューロンにおける前初期遺伝子の発現を誘導する.活性型CRTC1の発現により,c-fos遺伝子やArc遺伝子の発現が誘導されることが培養ニューロンおよび個体の脳において示された.しかし,これら前初期遺伝子の発現に対するCRTC1の直接の制御を証明するには,CRTC1がDNAにおいてこれら前初期遺伝子の制御領域に結合することを示さねばならなかった.そこで,クロマチン免疫沈降アッセイを行ったところ,神経活動を誘導したニューロンにおいて,CRTC1の免疫沈降によりc-fos遺伝子,Arc遺伝子,zif268遺伝子,BDNF遺伝子のプロモーターのCREB結合配列を含む断片が共沈降された.
CRTC1はCREBに特異的な転写補助因子なのだろうか? さきに,CRTC1はCREBの転写補助因子であると述べたが,CREBのほかの転写因子にも作用する可能性は否定されていなかった.そこで,A-CREBというCREBに特異的な阻害ペプチドによりCRTC1による転写の増強が完全に抑制されること,および,機能的なCREB結合配列を1箇所のみもつArc遺伝子プロモーターにおいてCREB結合配列に変異を導入するとCRTC1による転写の増強が抑制されること,の2つの方法により,CRTC1の作用がCREBに特異的であるということが証明された.
5.恐怖条件づけ学習課題での長期記憶におけるCRTC1の脳領域に特異的な役割
CRTC1による前初期遺伝子の発現の誘導がCREBのSer133のリン酸化とは独立したシグナル伝達経路による場合,CRTC1を介したCREBの活性化の意義は何だろうか? ひとつには,さきに述べたように,CRTC1はCREBとは独立したシグナル伝達経路による制御をうけることができるという点があげられた.つねに核に局在しSer133の1箇所のリン酸化により活性化されるCREBとは対照的に,CRTC1は神経活動が休止した状態において高度にリン酸化されており,神経活動に依存的なカルシニューリン活性により脱リン酸化されて核へと移行する.CREBのSer133のリン酸化だけでもPKA,ERK,MSK,CaMKIV,CaMKIIなど多くのリン酸化酵素の制御をうけているが9),転写補助因子による制御をくわえることにより制御の幅はさらに広がる.CREBは全身に発現し,その標的となる遺伝子は4000ともいわれるが,部位と発生段階に応じて多種多様な役割を演じ分けることができる1,3).CRTC1などの転写補助因子がこの状況に応じた遺伝子発現の制御を手助けしている可能性がある.
そこで,文脈依存的な恐怖条件づけという長期記憶の学習課題にかかわる海馬および扁桃体において,マウスの個体におけるCRTC1の局在について調べた.その結果,扁桃体では連合学習に応じたCRTC1の核への移行がみられたが,海馬ではみられなかった.これらの脳領域においてCRTC1をノックダウンしたところ,扁桃体においてCRTC1を欠くと記憶の低下がみられたが,海馬においては記憶に変化はみられなかった.つまり,扁桃体および海馬は長期記憶の形成における責任領域であるが,扁桃体においてCRTC1は核へと移行し記憶の形成に必要であったが,海馬においてCRTC1は必要とされなかった.しかし,CRTC1は海馬にも発現しており,より強い刺激をあたえると核へと移行した.そこで,海馬に活性型CRTC1を発現させたところ記憶の向上がみられた.扁桃体において活性型CRTC1を発現させても記憶の向上はみられなかった(図3).このように,CRTC1には脳領域に特異的な機能のあることが明らかになった.
おわりに
今回,筆者らは,CRTC1という転写補助因子に着目し,個体における脳領域に特異的な動態を明らかにした.転写因子に関連する認知記憶の分野における最近の動向にてらしあわせ,転写補助因子は状況に応じて転写因子の機能を制御する不可欠なタンパク質であるという流れにそい,その一例を具体的に示すことができた10).CRTC1はアルツハイマー病にも関連しており11),さらには,末梢神経系に発現したCRTC1が投射先の膵臓において糖尿病にかかわる代謝制御をし,ひいては,寿命にもかかわるとの報告もあり12),CRTC1は認知力の向上や代謝異常の改善など,新たな創薬の標的としても期待される.
文 献
- Silva, A. J., Kogan, J. H., Frankland, P. W. et al.: CREB and memory. Annu. Rev. Neurosci., 21, 127-148 (1998)[PubMed]
- Conkright, M. D., Canettieri, G., Screaton, R. et al.: TORCs: transducers of regulated CREB activity. Mol. Cell, 12, 413-423 (2003)[PubMed]
- Altarejos, J. Y. & Montminy, M.: CREB and the CRTC co-activators: sensors for hormonal and metabolic signals. Nat. Rev. Mol. Cell Biol., 12, 141-151 (2011)[PubMed]
- Mair, W., Morantte, I., Rodrigues, A. P. et al.: Lifespan extension induced by AMPK and calcineurin is mediated by CRTC-1 and CREB. Nature, 470, 404-408 (2011)[PubMed]
- Hirano, Y., Masuda, T., Naganos, S. et al.: Fasting launches CRTC to facilitate long-term memory formation in Drosophila. Science, 339, 443-446 (2013)[PubMed] [新着論文レビュー]
- Screaton, R. A., Conkright, M. D., Katoh, Y. et al.: The CREB coactivator TORC2 functions as a calcium- and cAMP-sensitive coincidence detector. Cell, 119, 61-74 (2004)[PubMed]
- Ch’ng, T. H., Uzgil, B., Lin, P. et al.: Activity-dependent transport of the transcriptional coactivator CRTC1 from synapse to nucleus. Cell, 150, 207-221 (2012)[PubMed]
- Sasaki, T., Takemori, H., Yagita, Y. et al.: SIK2 is a key regulator for neuronal survival after ischemia via TORC1-CREB. Neuron, 69, 106-119 (2011)[PubMed] [新着論文レビュー]
- Shaywitz, A. J. & Greenberg, M. E.: CREB: a stimulus-induced transcription factor activated by a diverse array of extracellular signals. Annu. Rev. Biochem., 68, 821-861 (1999)[PubMed]
- Nonaka, M., Kim, R., Sharry, S. et al.: Towards a better understanding of cognitive behaviors regulated by gene expression downstream of activity-dependent transcription factors. Neurobiol. Learn. Mem., 115, 21-29 (2014)[PubMed]
- Parra-Damas, A., Valero, J., Chen, M. et al.: Crtc1 activates a transcriptional program deregulated at early Alzheimer’s disease-related stages. J. Neurosci., 34, 5776-5787 (2014)[PubMed]
- Riera, C. E., Huising, M. O., Follett, P. et al.: TRPV1 pain receptors regulate longevity and metabolism by neuropeptide signaling. Cell, 157, 1023-1036 (2014)[PubMed]
著者プロフィール
略歴:2007年 京都大学大学院理学研究科 修了,同年 東京大学大学院医学系研究科 研究員,同 特任助教を経て,2012年より英国Edinburgh大学 ポスドク研究員.
研究テーマ:記憶をつかさどる分子機構を分子レベルから個体レベルまで縦断的に理解する.
関心事:海外にいながらにして美食・美酒を探求すること.
尾藤 晴彦(Haruhiko Bito)
東京大学大学院医学系研究科 教授.
研究室URL:http://www.neurochem.m.u-tokyo.ac.jp/
© 2014 野中美応・尾藤晴彦 Licensed under CC 表示 2.1 日本