哺乳類において細胞の大きさを制御するタンパク質Largen
山本一男・Tak W. Mak
(カナダToronto大学Departments of Medical Biophysics and Immunology)
email:山本一男
DOI: 10.7875/first.author.2014.042
Largen: a molecular regulator of mammalian cell size control.
Kazuo Yamamoto, Valentina Gandin, Masato Sasaki, Susan McCracken, Wanda Li, Jennifer Liepa Silvester, Andrew J. Elia, Feng Wang, Yosuke Wakutani, Roumiana Alexandrova, Yathor D Oo, Peter J. Mullen, Satoshi Inoue, Momoe Itsumi, Valentina Lapin, Jillian Haight, Andrew Wakeham, Arda Shahinian, Mitsuhiko Ikura, Ivan Topisirovic, Nahum Sonenberg, Tak W. Mak
Molecular Cell, 53, 904-915 (2014)
哺乳類が細胞の大きさを維持する機構についてはよくわかっていない.筆者らは,新規の遺伝学的なスクリーニングにより,ヒトの細胞において過剰に発現させることにより細胞の大きさを増大させる遺伝子の産物としてLargenを同定した.Largenはin vitroにおいてミトコンドリアタンパク質をコードするmRNAなどの翻訳を活性化した.Largenを過剰に発現した細胞においてはミトコンドリアおよびATPの産生が増加した.Largenを組織特異的に過剰発現するトランスジェニックマウスを用いた実験により,Largenはin vivoにおいても細胞の大きさを増大させることが示された.以上の結果は,哺乳類における細胞の大きさの制御において,Largenが翻訳とミトコンドリアの機能とを結びつける重要なタンパク質であることを示した.
われわれの身体は60兆個ともいわれる,さまざまなかたちや大きさの細胞からなりたっている.分化した細胞の大きさはおおむね一定の範囲におさまるが,代謝が活発に行われている器官や成熟の過程のある時期において,あるいは,損傷の治癒の過程や非対称分裂の結果,細胞の大きさは変化することがある.これらの事実は,細胞はそれ自体の大きさをある一定の範囲に保ち,必要に応じて別の定常状態へと遷移することが可能な制御機構をもつことを示す.
細胞の大きさの変異体は,最初に出芽酵母において発見された1).体系的な欠失変異体の作製により細胞の大きさに影響をあたえる数々の遺伝子が同定されている2,3).同様に,ショウジョウバエにおいてもRNAi法を用いた体系的なスクリーニングが行われ,細胞の大きさの制御におけるmTORシグナル伝達経路の重要性が明らかにされた4,5).mTORは細胞の増殖において中心的な役割をはたすセリン/スレオニンキナーゼである6,7).細胞の増殖に関連するシグナルはおしなべてこのキナーゼに集約され,mTOR複合体1あるいはmTOR複合体2を介し下流へと伝達される.
S6キナーゼ1/2および4E結合タンパク質はmTOR複合体1の代表的な基質であり,ともに翻訳を制御する8,9).mTOR複合体2はAkt,SGK1,PKCαなどのAGCキナーゼをリン酸化して活性化することにより細胞の生存および同化作用を制御する10).興味深いことに,ラパマイシンによりmTORの活性を特異的に阻害すると,多くの細胞において大きさが縮小することが知られている11).筆者らは,この現象を利用して,ラパマイシンによる細胞の大きさの縮小作用に拮抗する遺伝子のスクリーニング法を開発した.そしてこの方法により,細胞の大きさを制御するタンパク質としてLargenを同定した.Largenはミトコンドリアの活性および翻訳を活性化したが,すでに知られているmTORやHippoなどによる細胞の成長を制御するシグナル伝達経路とは,別にはたらいている点において重要と思われた.
考案した遺伝子スクリーニング法は以下のとおりである.1)ヒトに由来するJurkat細胞に対しERM(enhanced retroviral mutagen,強化レトロウイルス突然変異原)法により変異体プールを作製する.2)この変異体プールをラパマイシンにより処理する.3)処理した変異体プールから大きさの大きい細胞のみを回収する.4)回収した細胞をクローン化しおのおのの原因遺伝子を同定する.ERM法とは,テトラサイクリンに感受性をもつ転写因子により制御される遺伝子プロモーターの下流にHAタグとスプライス供与配列を挿入したレトロウイルスベクターを細胞に感染させることにより,標的となる細胞のもつ遺伝子をランダムに活性化する方法である12).これにより,レトロウイルスの挿入されたゲノム部位の近傍に存在する遺伝子の発現はつねに活性化されるが,テトラサイクリン(または,その安定誘導体であるドキシサイクリン)を投与することによりその発現をオフにすることのできる変異細胞が作出される.もし,ラパマイシンによる細胞の大きさの縮小作用に拮抗する遺伝子があるとするならば,その遺伝子を人工的に過剰発現させた細胞はラパマイシンにより処理しても縮小せず,ほかの細胞と大きさにより区別できるはずであり,そのような細胞は蛍光フローサイトメーターにより単純に“大きい細胞”をソーティングすることで濃縮されるはずである.ソーティングをくり返して目的とする変異細胞を十分に濃縮したのち,限定希釈法により細胞をクローン化する.しかるのち,おのおのの細胞クローンのラパマイシンに対する細胞の大きさの応答性をドキシサイクリンの存在下と非存在下とで比較することにより擬陽性を排除し,人工的に発現の活性化されている遺伝子の作用によってのみラパマイシンによる細胞の大きさの縮小作用に拮抗する表現型を示す変異細胞を同定する.おのおのの細胞クローンにおける原因遺伝子は,ERM法にて導入したタグを指標にしたRT-PCR法によって得た塩基配列をゲノムの情報と照会することにより容易に同定できる.
以上の戦略により,実際に細胞の大きさの変異した細胞クローンが200個以上も得られ,細胞の大きさの制御にかかわる数十個の遺伝子を同定することができた.
得られた遺伝子のうち,ある遺伝子を発現ベクターに挿入してJurkat細胞,293T細胞,HeLa細胞において過剰に発現させたところ,細胞の大きさが増大し,ラパマイシンにより処理しても対照となる親株の細胞より大きいままであった.反対に,その遺伝子の内在性の発現をsiRNAにより阻害すると細胞は縮小し,一部で細胞死が誘導された.これらの結果から,既存のデータベースにおいてPRR16(proline-rich protein 16)遺伝子として分類されるこの遺伝子にコードされるタンパク質をLargenと命名し,さらなる解析を行った.
Largenを過剰に発現した細胞においては正常な細胞と比較してより多くのタンパク質が蓄積しているという観察の結果から,標識アミノ酸の取り込み実験やルシフェラーゼレポーターアッセイ系を用いた実験により,Largenを過剰発現させると翻訳の効率が上昇することを確認した.Largenと翻訳開始因子との相互作用を想定して免疫沈降実験を行ったが,eIF4A,eIF4B,eIF4Eなど一部の翻訳開始因子がゆるく会合したほかには,Largenと結合するタンパク質はみられなかった.同様に,mTORシグナル伝達経路あるいはHippoシグナル伝達経路を構成するタンパク質との相互作用も見い出せなかった.細胞質に存在するリボソームをスクロース密度勾配遠心法により分画し,得られたポリソームに含まれるmRNAをマイクロアレイ法により解析したところ,Largenを過剰に発現した細胞ではとくにヒストンやミトコンドリアタンパク質などの翻訳が著しく促進されていることが示された.Mitotrackerによる染色やミトコンドリアゲノムの定量により,Largenを過剰に発現した細胞においてはミトコンドリアの増加していることが明らかになった.このミトコンドリアの増加に対応して,Largenを過剰に発現した細胞では酸素の消費が亢進しATPを過剰に産生していることが確認された.正常な細胞をミトコンドリア呼吸鎖の阻害剤であるFCCPにより処理したところ細胞の大きさは縮小した.Largenを過剰に発現した細胞においてもFCCPの処理により細胞の大きさは縮小したが,その度合いは正常な細胞より小さかった.この差は,Largenを過剰に発現した細胞においてはミトコンドリアが活性化しているためと考えられ,細胞の大きさの制御とミトコンドリアとの関連が示唆された.
Largenの過剰発現により誘導されるこれらの特性がin vivoにおいても発揮されるかどうかを調べるため,トランスジェニックマウスを作製した.Largenを全身において過剰発現するトランスジェニックマウスは胎生致死となった.したがって,Largenの発現は発生の過程において厳密に制御される必要があるものと考えられた.これに対し,Largenを肝臓において特異的に過剰発現するトランスジェニックマウス,および,筋において特異的に過剰発現するトランスジェニックマウスは正常なメンデル比で得られ,その成体において肝臓あるいは心筋の細胞が増大することが確認された.したがって,Largenは生体においても細胞の大きさを制御していることが証明された.
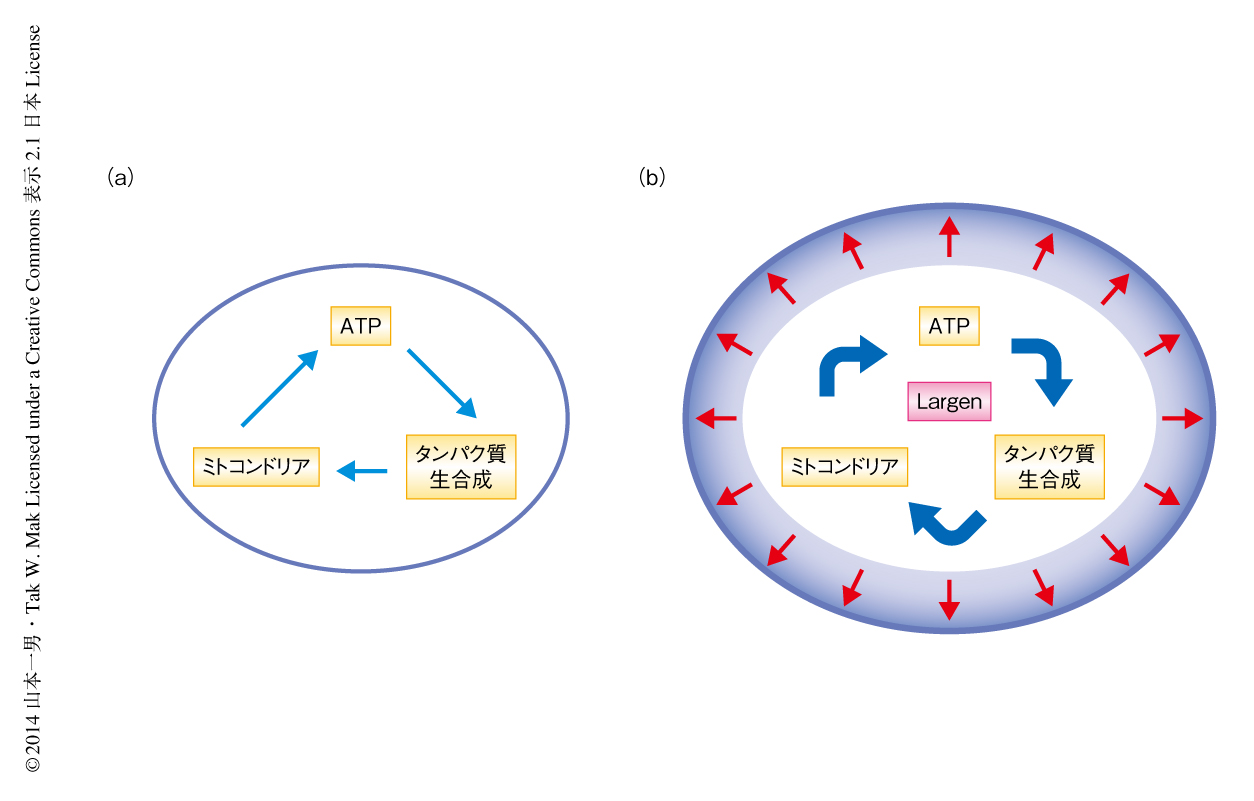
以上の結果より,細胞がその大きさを制御するしくみの一端が明らかになり,これまで機能が不明であったPRR16遺伝子を,細胞の大きさの制御にかかわるタンパク質Largenをコードする遺伝子として掘りおこすことができた.現在のところ,Largenの過剰発現によりミトコンドリアが増加し,ATPの産生が増強されて,細胞におけるタンパク質生合成が総体的に促進される結果,細胞の大きさが増大するという機構が考えられる(図1).しかしながら,これらの制御機構については明らかではない.さらなる分子細胞生物学的な実験により詳細を究明するとともに,Largenのノックアウトマウスの作製などが必要とされるだろう.現在までに得られた情報から,Largenはおそらく細胞の代謝制御に関与していると推測されることから,Largenの機能を詳細に解明できれば,細胞代謝の異常によりひき起こされるがんやメタボリックシンドロームなどの病態に対する理解が深まるとともに,これら複合的な疾患に対し従来とは異なる観点からの創薬に発展するとも期待される.
略歴:1992年 埼玉医科大学医学部 助手,1994年 大阪大学大学院理学研究科にて博士号取得,1997年 長崎大学医学部 講師,2003年 長崎大学大学院医歯薬学総合研究科 助教授,2007年 カナダToronto大学 上席研究員を経て,2012年より長崎大学医学部共同利用研究センター 准教授.
研究テーマ:細胞の大きさを規定する分子基盤.
抱負:さまざまな生命現象を細胞の大きさという観点から俯瞰してみたい.
Tak W. Mak
カナダToronto大学Professor.
© 2014 山本一男・Tak W. Mak Licensed under CC 表示 2.1 日本
(カナダToronto大学Departments of Medical Biophysics and Immunology)
email:山本一男
DOI: 10.7875/first.author.2014.042
Largen: a molecular regulator of mammalian cell size control.
Kazuo Yamamoto, Valentina Gandin, Masato Sasaki, Susan McCracken, Wanda Li, Jennifer Liepa Silvester, Andrew J. Elia, Feng Wang, Yosuke Wakutani, Roumiana Alexandrova, Yathor D Oo, Peter J. Mullen, Satoshi Inoue, Momoe Itsumi, Valentina Lapin, Jillian Haight, Andrew Wakeham, Arda Shahinian, Mitsuhiko Ikura, Ivan Topisirovic, Nahum Sonenberg, Tak W. Mak
Molecular Cell, 53, 904-915 (2014)
要 約
哺乳類が細胞の大きさを維持する機構についてはよくわかっていない.筆者らは,新規の遺伝学的なスクリーニングにより,ヒトの細胞において過剰に発現させることにより細胞の大きさを増大させる遺伝子の産物としてLargenを同定した.Largenはin vitroにおいてミトコンドリアタンパク質をコードするmRNAなどの翻訳を活性化した.Largenを過剰に発現した細胞においてはミトコンドリアおよびATPの産生が増加した.Largenを組織特異的に過剰発現するトランスジェニックマウスを用いた実験により,Largenはin vivoにおいても細胞の大きさを増大させることが示された.以上の結果は,哺乳類における細胞の大きさの制御において,Largenが翻訳とミトコンドリアの機能とを結びつける重要なタンパク質であることを示した.
はじめに
われわれの身体は60兆個ともいわれる,さまざまなかたちや大きさの細胞からなりたっている.分化した細胞の大きさはおおむね一定の範囲におさまるが,代謝が活発に行われている器官や成熟の過程のある時期において,あるいは,損傷の治癒の過程や非対称分裂の結果,細胞の大きさは変化することがある.これらの事実は,細胞はそれ自体の大きさをある一定の範囲に保ち,必要に応じて別の定常状態へと遷移することが可能な制御機構をもつことを示す.
細胞の大きさの変異体は,最初に出芽酵母において発見された1).体系的な欠失変異体の作製により細胞の大きさに影響をあたえる数々の遺伝子が同定されている2,3).同様に,ショウジョウバエにおいてもRNAi法を用いた体系的なスクリーニングが行われ,細胞の大きさの制御におけるmTORシグナル伝達経路の重要性が明らかにされた4,5).mTORは細胞の増殖において中心的な役割をはたすセリン/スレオニンキナーゼである6,7).細胞の増殖に関連するシグナルはおしなべてこのキナーゼに集約され,mTOR複合体1あるいはmTOR複合体2を介し下流へと伝達される.
S6キナーゼ1/2および4E結合タンパク質はmTOR複合体1の代表的な基質であり,ともに翻訳を制御する8,9).mTOR複合体2はAkt,SGK1,PKCαなどのAGCキナーゼをリン酸化して活性化することにより細胞の生存および同化作用を制御する10).興味深いことに,ラパマイシンによりmTORの活性を特異的に阻害すると,多くの細胞において大きさが縮小することが知られている11).筆者らは,この現象を利用して,ラパマイシンによる細胞の大きさの縮小作用に拮抗する遺伝子のスクリーニング法を開発した.そしてこの方法により,細胞の大きさを制御するタンパク質としてLargenを同定した.Largenはミトコンドリアの活性および翻訳を活性化したが,すでに知られているmTORやHippoなどによる細胞の成長を制御するシグナル伝達経路とは,別にはたらいている点において重要と思われた.
1.細胞の大きさを制御する遺伝子のスクリーニング
考案した遺伝子スクリーニング法は以下のとおりである.1)ヒトに由来するJurkat細胞に対しERM(enhanced retroviral mutagen,強化レトロウイルス突然変異原)法により変異体プールを作製する.2)この変異体プールをラパマイシンにより処理する.3)処理した変異体プールから大きさの大きい細胞のみを回収する.4)回収した細胞をクローン化しおのおのの原因遺伝子を同定する.ERM法とは,テトラサイクリンに感受性をもつ転写因子により制御される遺伝子プロモーターの下流にHAタグとスプライス供与配列を挿入したレトロウイルスベクターを細胞に感染させることにより,標的となる細胞のもつ遺伝子をランダムに活性化する方法である12).これにより,レトロウイルスの挿入されたゲノム部位の近傍に存在する遺伝子の発現はつねに活性化されるが,テトラサイクリン(または,その安定誘導体であるドキシサイクリン)を投与することによりその発現をオフにすることのできる変異細胞が作出される.もし,ラパマイシンによる細胞の大きさの縮小作用に拮抗する遺伝子があるとするならば,その遺伝子を人工的に過剰発現させた細胞はラパマイシンにより処理しても縮小せず,ほかの細胞と大きさにより区別できるはずであり,そのような細胞は蛍光フローサイトメーターにより単純に“大きい細胞”をソーティングすることで濃縮されるはずである.ソーティングをくり返して目的とする変異細胞を十分に濃縮したのち,限定希釈法により細胞をクローン化する.しかるのち,おのおのの細胞クローンのラパマイシンに対する細胞の大きさの応答性をドキシサイクリンの存在下と非存在下とで比較することにより擬陽性を排除し,人工的に発現の活性化されている遺伝子の作用によってのみラパマイシンによる細胞の大きさの縮小作用に拮抗する表現型を示す変異細胞を同定する.おのおのの細胞クローンにおける原因遺伝子は,ERM法にて導入したタグを指標にしたRT-PCR法によって得た塩基配列をゲノムの情報と照会することにより容易に同定できる.
以上の戦略により,実際に細胞の大きさの変異した細胞クローンが200個以上も得られ,細胞の大きさの制御にかかわる数十個の遺伝子を同定することができた.
2.細胞の大きさを制御するタンパク質Largenの同定
得られた遺伝子のうち,ある遺伝子を発現ベクターに挿入してJurkat細胞,293T細胞,HeLa細胞において過剰に発現させたところ,細胞の大きさが増大し,ラパマイシンにより処理しても対照となる親株の細胞より大きいままであった.反対に,その遺伝子の内在性の発現をsiRNAにより阻害すると細胞は縮小し,一部で細胞死が誘導された.これらの結果から,既存のデータベースにおいてPRR16(proline-rich protein 16)遺伝子として分類されるこの遺伝子にコードされるタンパク質をLargenと命名し,さらなる解析を行った.
3.Largenと翻訳およびミトコンドリアとのかかわり
Largenを過剰に発現した細胞においては正常な細胞と比較してより多くのタンパク質が蓄積しているという観察の結果から,標識アミノ酸の取り込み実験やルシフェラーゼレポーターアッセイ系を用いた実験により,Largenを過剰発現させると翻訳の効率が上昇することを確認した.Largenと翻訳開始因子との相互作用を想定して免疫沈降実験を行ったが,eIF4A,eIF4B,eIF4Eなど一部の翻訳開始因子がゆるく会合したほかには,Largenと結合するタンパク質はみられなかった.同様に,mTORシグナル伝達経路あるいはHippoシグナル伝達経路を構成するタンパク質との相互作用も見い出せなかった.細胞質に存在するリボソームをスクロース密度勾配遠心法により分画し,得られたポリソームに含まれるmRNAをマイクロアレイ法により解析したところ,Largenを過剰に発現した細胞ではとくにヒストンやミトコンドリアタンパク質などの翻訳が著しく促進されていることが示された.Mitotrackerによる染色やミトコンドリアゲノムの定量により,Largenを過剰に発現した細胞においてはミトコンドリアの増加していることが明らかになった.このミトコンドリアの増加に対応して,Largenを過剰に発現した細胞では酸素の消費が亢進しATPを過剰に産生していることが確認された.正常な細胞をミトコンドリア呼吸鎖の阻害剤であるFCCPにより処理したところ細胞の大きさは縮小した.Largenを過剰に発現した細胞においてもFCCPの処理により細胞の大きさは縮小したが,その度合いは正常な細胞より小さかった.この差は,Largenを過剰に発現した細胞においてはミトコンドリアが活性化しているためと考えられ,細胞の大きさの制御とミトコンドリアとの関連が示唆された.
4.Largenのマウスを用いた解析
Largenの過剰発現により誘導されるこれらの特性がin vivoにおいても発揮されるかどうかを調べるため,トランスジェニックマウスを作製した.Largenを全身において過剰発現するトランスジェニックマウスは胎生致死となった.したがって,Largenの発現は発生の過程において厳密に制御される必要があるものと考えられた.これに対し,Largenを肝臓において特異的に過剰発現するトランスジェニックマウス,および,筋において特異的に過剰発現するトランスジェニックマウスは正常なメンデル比で得られ,その成体において肝臓あるいは心筋の細胞が増大することが確認された.したがって,Largenは生体においても細胞の大きさを制御していることが証明された.
おわりに
以上の結果より,細胞がその大きさを制御するしくみの一端が明らかになり,これまで機能が不明であったPRR16遺伝子を,細胞の大きさの制御にかかわるタンパク質Largenをコードする遺伝子として掘りおこすことができた.現在のところ,Largenの過剰発現によりミトコンドリアが増加し,ATPの産生が増強されて,細胞におけるタンパク質生合成が総体的に促進される結果,細胞の大きさが増大するという機構が考えられる(図1).しかしながら,これらの制御機構については明らかではない.さらなる分子細胞生物学的な実験により詳細を究明するとともに,Largenのノックアウトマウスの作製などが必要とされるだろう.現在までに得られた情報から,Largenはおそらく細胞の代謝制御に関与していると推測されることから,Largenの機能を詳細に解明できれば,細胞代謝の異常によりひき起こされるがんやメタボリックシンドロームなどの病態に対する理解が深まるとともに,これら複合的な疾患に対し従来とは異なる観点からの創薬に発展するとも期待される.
文 献
- Nurse, P.: A long twentieth century of the cell cycle and beyond. Cell, 100, 1-8 (2000)[PubMed]
- Jorgensen, P., Nishikawa, J. L., Breitkreutz, B. J. et al.: Systematic identification of pathways that couple cell growth and division in yeast. Science, 297, 395-400 (2002)[PubMed]
- Zhang, J., Schneider, C., Ottmers, L. et al.: Genomic scale mutant hunt identifies cell size homeostasis genes in S. cerevisiae. Curr. Biol., 12, 1992-2001 (2002)[PubMed]
- Bjorklund, M., Taipale, M., Varjosalo, M. et al.: Identification of pathways regulating cell size and cell-cycle progression by RNAi. Nature, 439, 1009-1013 (2006)[PubMed]
- Guertin, D. A., Guntur, K. V., Bell, G. W. et al.: Functional genomics identifies TOR-regulated genes that control growth and division. Curr. Biol,, 16, 958-970 (2006)[PubMed]
- Laplante, M. & Sabatini, D. M.: mTOR signaling in growth control and disease. Cell, 149, 273-293 (2012)[PubMed]
- Loewith, R. & Hall, M. N.: Target of rapamycin (TOR) in nutrient signaling and growth control. Genetics, 189, 1177-201 (2011)[PubMed]
- Ma, X. M. & Blenis, J.: Molecular mechanisms of mTOR-mediated translational control. Nat. Rev. Mol. Cell Biol., 10, 307-318 (2009)[PubMed]
- Magnuson, B., Ekim, B. & Fingar, D. C.: Regulation and function of ribosomal protein S6 kinase (S6K) within mTOR signaling networks. Biochem. J., 441, 1-21 (2012)[PubMed]
- Oh, W. J. & Jacinto, E.: mTOR complex 2 signaling and functions. Cell Cycle, 10, 2305-2316 (2011)[PubMed]
- Fingar, D. C., Salama, S., Tsou, C. et al.: Mammalian cell size is controlled by mTOR and its downstream targets S6K1 and 4EBP1/eIF4E. Genes Dev., 16, 1472-1487 (2002)[PubMed]
- Liu, D. & Songyang, Z.: ERM-mediated genetic screens in mammalian cells. Methods Enzymol., 446, 409-419 (2008)[PubMed]
著者プロフィール
略歴:1992年 埼玉医科大学医学部 助手,1994年 大阪大学大学院理学研究科にて博士号取得,1997年 長崎大学医学部 講師,2003年 長崎大学大学院医歯薬学総合研究科 助教授,2007年 カナダToronto大学 上席研究員を経て,2012年より長崎大学医学部共同利用研究センター 准教授.
研究テーマ:細胞の大きさを規定する分子基盤.
抱負:さまざまな生命現象を細胞の大きさという観点から俯瞰してみたい.
Tak W. Mak
カナダToronto大学Professor.
© 2014 山本一男・Tak W. Mak Licensed under CC 表示 2.1 日本