肥満においてセマフォリン3Eにより誘導される脂肪組織の炎症はインスリン抵抗性を惹起する
南野 徹・吉田陽子
(新潟大学大学院医歯学総合研究科 循環器学分野)
email:南野 徹
DOI: 10.7875/first.author.2013.139
Semaphorin3E-induced inflammation contributes to insulin resistance in dietary obesity.
Ippei Shimizu, Yohko Yoshida, Junji Moriya, Aika Nojima, Akiyoshi Uemura, Yoshio Kobayashi, Tohru Minamino
Cell Metabolism, 18, 491-504 (2013)
セマフォリンおよびその受容体であるプレキシンは胎生期の神経発生を制御する神経軸索ガイダンスタンパク質である.今回の研究において,筆者らは,肥満においてセマフォリン3Eが脂肪組織の炎症および全身のインスリン抵抗性を惹起することを明らかにした.肥満モデルマウスの内臓脂肪組織ではセマフォリン3Eおよびその特異的な受容体であるプレキシンD1の発現が亢進していた.セマフォリン3E-プレキシンD1シグナルを阻害すると脂肪組織の炎症およびインスリン抵抗性は著明に改善し,反対に,脂肪組織においてセマフォリン3Eを過剰に発現させたマウスでは脂肪組織の炎症およびインスリン抵抗性が惹起された.セマフォリン3Eはマクロファージの脂肪組織への浸潤を誘導しており,マクロファージにおけるプレキシンD1の発現の低下はセマフォリン3Eのもつマクロファージの誘導作用を減弱させた.さらに,脂肪組織におけるp53の活性化を阻害するとセマフォリン3Eの発現は低下し脂肪組織の炎症は改善した.これらの結果から,セマフォリン3Eはマクロファージ誘導タンパク質としての役割をはたしており,また,肥満においてp53の活性化によりセマフォリン3Eの発現が誘導されることで,脂肪組織の炎症および全身のインスリン抵抗性が惹起されることが明らかになった.
近年,肥満や糖尿病の患者は劇的に増加しており,現代社会の大きな問題になっている.肥満に関連した脂肪組織の炎症は,全身のインスリン抵抗性や糖尿病の発症に深く関与していることが知られている1).肥満における脂肪組織では増大した遊離脂肪酸や酸化ストレスが炎症細胞の浸潤やTNFα,CCL2(MCP-1)といった炎症性サイトカインの産生を促進し,過剰に産生されたCCL2が脂肪組織にマクロファージの浸潤を誘導することにより,さらに炎症性サイトカインが産生されるという悪循環が生じている.炎症の生じた脂肪組織において産生された炎症性サイトカインが全身を循環することにより,骨格筋や肝臓といったインスリンの標的となる臓器にも影響が及び,全身のインスリン抵抗性や糖尿病がひき起こされると考えられている2).
セマフォリンとその受容体であるプレキシンは反発性の神経軸索ガイダンスタンパク質として見い出されたが,今日では,心血管系,骨格筋,腎臓,神経系といった多種多様な臓器の発生の制御に重要であることがわかっている.セマフォリンは脊椎動物においてはクラス3~クラス7まで存在し,分泌型タンパク質であるクラス3セマフォリンにはセマフォリン3A~セマフォリン3Gの7つのサブタイプが存在する.クラス3セマフォリンは神経および心血管系における器官の形成に重要であるが,細胞の増殖,細胞死,遊走などにも関与し,神経疾患やがんなどにも関連していることが報告されている.セマフォリン3Eにはその特異的な受容体としてプレキシンD1が知られているが,これらは器官形成だけでなく心血管疾患や腫瘍の増殖にも関連していることが知られている.以前に,筆者らは,糖尿病においてはセマフォリン3Eの発現が亢進しており,これが虚血組織における血管の新生を阻害していることを報告した3).セマフォリン-プレキシンシグナルは免疫系の制御にかかわることも報告されており,このシグナルが炎症の制御にかかわっていることが示唆された.これらのことから,筆者らは,セマフォリン3Eが肥満において脂肪組織の炎症を惹起し全身のインスリン抵抗性をひき起こすという仮説をたて研究を開始した.
肥満における脂肪組織においてセマフォリンおよびプレキシンの役割を調べるため,マウスに高脂肪高ショ糖食をあたえ食餌誘導性の肥満モデルマウスを作製した.この肥満モデルマウスではマクロファージを主体とする炎症細胞の浸潤がみられ,TNFαやCCL2といった炎症性サイトカインの発現が著明に亢進していた.さらに,インスリン抵抗性や耐糖能の異常といった糖代謝の異常もきたしていた.そこで,肥満における脂肪組織においてセマフォリン3EおよびプレキシンD1の発現を調べたところ,脂肪組織において著明に亢進していた.さらにくわしく調べると,セマフォリン3Eはおもに脂肪細胞の細胞質において,プレキシンD1は脂肪組織へ浸潤した細胞,とくに,マクロファージにおいて発現が亢進していた.そのとき,血中のセマフォリン3Eの濃度も上昇しており,脂肪組織から分泌されるセマフォリン3Eとマクロファージにおいて発現したプレキシンD1との相互作用が,肥満における脂肪組織の炎症に関与している可能性が示唆された.さらに,ヒトの糖尿病の患者においても血中のセマフォリン3Eの濃度が上昇しており,ヒトの代謝性疾患においてもセマフォリン3E-プレキシンD1シグナルが重要なはたらきをしている可能性が示唆された.
肥満におけるセマフォリン3E-プレキシンD1シグナルのはたす役割について詳細に検証するため,肥満モデルマウスにセマフォリン3Eと結合しその作用を阻害するはたらきをもつ可溶性プレキシンD1を投与した.その結果,体重や摂餌量,酸素消費量などの代謝プロファイルは変化しなかったにもかかわらず,脂肪組織の炎症は有意に改善し,インスリン抵抗性や耐糖能の異常といった糖代謝の異常も著明に改善した.セマフォリン3Eホモノックアウトマウスにおいても同様に,肥満における脂肪組織の炎症や糖代謝の異常が著明に改善していたことから,セマフォリン3E-プレキシンD1シグナルは肥満において脂肪組織の炎症や糖代謝の異常を誘導する作用のあることが示唆された.
セマフォリン3Eが過剰に発現したときの脂肪組織への影響を調べるため,脂肪組織において特異的にセマフォリン3Eを過剰に発現するマウスを作製した.このマウスに通常食をあたえたとき,脂肪組織および血中のセマフォリン3Eの濃度は著明に上昇しており,脂肪組織ではマクロファージを主体とする炎症細胞の浸潤や炎症性サイトカインの発現の亢進を認めた.さらに,著明な糖代謝の異常もきたしていたが,これはTNFα中和抗体の投与により改善した.
マクロファージなどの炎症細胞はその細胞の表面にCCL2受容体を発現しているため,CCL2が分泌されるとそれに反応して炎症組織や感染組織に炎症細胞の浸潤が誘導されることが知られている.そこで,培養マクロファージ細胞を用いて細胞遊走アッセイを行いマクロファージの誘導性について検証したところ,セマフォリン3EはCCL2と同等にマクロファージを誘導する作用があり,マクロファージにおいてプレキシンD1を抑制するとこの作用は抑制されることがわかった.また,野生型マウスより作製した肥満モデルマウスから採取した脂肪組織を培養した上清を用いて細胞遊走アッセイを行ったときには培養マクロファージ細胞の浸潤が誘導されたが,セマフォリン3Eホモノックアウトマウスより作製した肥満モデルマウスから採取した脂肪組織を培養した上清ではマクロファージの浸潤は抑制された.
セマフォリン3Eは反発性の神経軸索ガイダンスタンパク質としてはたらくときには,プレキシンD1,Nrp1(ニューロピリン1),VEGF受容体2からなる複合体と作用し,PI3K-Aktシグナル伝達経路を活性化させることが知られている4).そこで,培養マクロファージ細胞を用いた細胞遊走アッセイにおいてこれを検証したところ,Nrp1,VEGF受容体2,PI3K,Aktの抑制により,セマフォリン3Eによるマクロファージの誘導作用は著明に抑制され,セマフォリン3EはplexinD1,Nrp1,VEGF受容体2に依存的にマクロファージ誘導タンパク質としてはたらくと考えられた.
骨髄細胞において発現するプレキシンD1の脂肪組織の炎症における役割を検証するため,プレキシンD1の発現をノックダウンした骨髄を移植したマウスを作製したところ,このマウスでは肥満における脂肪組織および糖代謝の異常が抑制された.このことから,肥満においてマクロファージの脂肪組織への浸潤は,プレキシンD1を介し誘導されると考えられた.
以前に筆者らは,肥満においては酸化ストレスやDNA損傷が蓄積し脂肪組織においてp53が活性化すること,活性化したp53は脂肪組織の炎症を惹起し全身のインスリン抵抗性をひき起こすことを報告した5).そこで,p53とセマフォリン3Eとの関連性について調べるため脂肪組織に特異的なp53ノックアウトマウスを作製したところ,肥満において脂肪組織および血中におけるセマフォリン3Eの濃度の上昇が著明に抑制されており,脂肪組織の炎症や糖代謝の異常も抑制されていた.しかし,このノックアウトマウスに可溶性プレキシンを投与しセマフォリン3E-プレキシンD1シグナルを抑制しても,相加的な改善効果はなかった.このことから,p53に依存性の脂肪組織の炎症においてセマフォリン3E-プレキシンD1シグナルはp53の下流のシグナルとして重要なはたらきをしている可能性が示唆された.
セマフォリン3Eによる糖代謝の制御におけるp53活性化のはたす役割について検証するため,野生型マウスの脂肪組織にp53活性化剤であるキナクリンを投与した.その結果,脂肪組織および血中においてセマフォリン3Eの濃度が上昇するとともに,脂肪組織の炎症および糖代謝の異常が惹起されたが,これらの変化は脂肪組織に特異的なp53ノックアウトマウスでは起こらず,キナクリンにより誘導される脂肪組織の炎症はp53に依存的なものであると考えられた.さらに,クロマチン免疫沈降法を用いて検証したところ,p53はセマフォリン3E遺伝子のプロモーター領域に結合していることがわかった.また,キナクリンにより脂肪組織のp53を活性化させたマウスに対し可溶性プレキシンD1やTNFα中和抗体を投与したところ,脂肪組織の炎症および糖代謝の異常は改善した.これらの結果より,セマフォリン3Eは肥満におけるp53に依存性の脂肪組織の炎症において重要な役割をはたしていると考えられた.
この研究において,筆者らは,セマフォリン3E-プレキシンD1シグナルが脂肪組織の炎症を惹起し,インスリン抵抗性や糖尿病の発症および進展に重要な役割をはたしていることを明らかにした(図1).セマフォリン3EがプレキシンD1陽性マクロファージを誘導し,脂肪組織でのp53の活性化がセマフォリン3Eによるマクロファージの浸潤の誘導を促進することにより,脂肪組織の炎症や糖代謝の異常が惹起されることが明らかになった.がん抑制遺伝子であるp53遺伝子はDNA修復,アポトーシス,老化などに関連し,ゲノムの安定性の維持や発がんの抑制にも寄与している.近年,p53遺伝子は加齢に関連する疾患にも関与することが知られてきており,加齢にともないp53の発現が亢進することや6),p53の持続的な活性化は早期の老化をひき起こすこと7),老化した心血管ではp53の発現が亢進していることなどが報告され8-10),動脈硬化や心不全といった疾患においても重要な役割をはたしていると考えられるようになった.また最近では,代謝異常や代謝制御との関連性を示唆する報告もなされており,以前に筆者らも,肥満における脂肪組織においてp53に依存性の炎症が惹起されることを報告している.この研究では,セマフォリン3E-プレキシンD1シグナルがp53に依存性の脂肪組織の炎症において重要な役割をはたし,このシグナルの抑制が肥満における代謝異常を改善させることを示した.p53それ自体の抑制は発がんを誘導する可能性も考えられることから,セマフォリン3E-プレキシンD1シグナルの抑制は肥満患者の糖代謝の異常に対する新規の治療標的となる可能性が示唆された.
略歴:1997年 東京大学大学院医学系研究科にて博士号取得,同年 米国Harvard Medical Schoolリサーチフェロー,2000年 帝京大学医学部 助手,2001年 千葉大学大学院医学研究院 助手,2010年 同 講師を経て,2012年より新潟大学医歯学総合研究科 教授.
研究テーマ:生活習慣病と老化.再生医療.
抱負:加齢に関連する疾患の発症機序の解明を目標としています.
研究室URL:http://www.med.niigata-u.ac.jp/car/index.html
吉田 陽子(Yohko Yoshida)
新潟大学医歯学総合病院 医員.
© 2013 南野 徹・吉田陽子 Licensed under CC 表示 2.1 日本
(新潟大学大学院医歯学総合研究科 循環器学分野)
email:南野 徹
DOI: 10.7875/first.author.2013.139
Semaphorin3E-induced inflammation contributes to insulin resistance in dietary obesity.
Ippei Shimizu, Yohko Yoshida, Junji Moriya, Aika Nojima, Akiyoshi Uemura, Yoshio Kobayashi, Tohru Minamino
Cell Metabolism, 18, 491-504 (2013)
要 約
セマフォリンおよびその受容体であるプレキシンは胎生期の神経発生を制御する神経軸索ガイダンスタンパク質である.今回の研究において,筆者らは,肥満においてセマフォリン3Eが脂肪組織の炎症および全身のインスリン抵抗性を惹起することを明らかにした.肥満モデルマウスの内臓脂肪組織ではセマフォリン3Eおよびその特異的な受容体であるプレキシンD1の発現が亢進していた.セマフォリン3E-プレキシンD1シグナルを阻害すると脂肪組織の炎症およびインスリン抵抗性は著明に改善し,反対に,脂肪組織においてセマフォリン3Eを過剰に発現させたマウスでは脂肪組織の炎症およびインスリン抵抗性が惹起された.セマフォリン3Eはマクロファージの脂肪組織への浸潤を誘導しており,マクロファージにおけるプレキシンD1の発現の低下はセマフォリン3Eのもつマクロファージの誘導作用を減弱させた.さらに,脂肪組織におけるp53の活性化を阻害するとセマフォリン3Eの発現は低下し脂肪組織の炎症は改善した.これらの結果から,セマフォリン3Eはマクロファージ誘導タンパク質としての役割をはたしており,また,肥満においてp53の活性化によりセマフォリン3Eの発現が誘導されることで,脂肪組織の炎症および全身のインスリン抵抗性が惹起されることが明らかになった.
はじめに
近年,肥満や糖尿病の患者は劇的に増加しており,現代社会の大きな問題になっている.肥満に関連した脂肪組織の炎症は,全身のインスリン抵抗性や糖尿病の発症に深く関与していることが知られている1).肥満における脂肪組織では増大した遊離脂肪酸や酸化ストレスが炎症細胞の浸潤やTNFα,CCL2(MCP-1)といった炎症性サイトカインの産生を促進し,過剰に産生されたCCL2が脂肪組織にマクロファージの浸潤を誘導することにより,さらに炎症性サイトカインが産生されるという悪循環が生じている.炎症の生じた脂肪組織において産生された炎症性サイトカインが全身を循環することにより,骨格筋や肝臓といったインスリンの標的となる臓器にも影響が及び,全身のインスリン抵抗性や糖尿病がひき起こされると考えられている2).
セマフォリンとその受容体であるプレキシンは反発性の神経軸索ガイダンスタンパク質として見い出されたが,今日では,心血管系,骨格筋,腎臓,神経系といった多種多様な臓器の発生の制御に重要であることがわかっている.セマフォリンは脊椎動物においてはクラス3~クラス7まで存在し,分泌型タンパク質であるクラス3セマフォリンにはセマフォリン3A~セマフォリン3Gの7つのサブタイプが存在する.クラス3セマフォリンは神経および心血管系における器官の形成に重要であるが,細胞の増殖,細胞死,遊走などにも関与し,神経疾患やがんなどにも関連していることが報告されている.セマフォリン3Eにはその特異的な受容体としてプレキシンD1が知られているが,これらは器官形成だけでなく心血管疾患や腫瘍の増殖にも関連していることが知られている.以前に,筆者らは,糖尿病においてはセマフォリン3Eの発現が亢進しており,これが虚血組織における血管の新生を阻害していることを報告した3).セマフォリン-プレキシンシグナルは免疫系の制御にかかわることも報告されており,このシグナルが炎症の制御にかかわっていることが示唆された.これらのことから,筆者らは,セマフォリン3Eが肥満において脂肪組織の炎症を惹起し全身のインスリン抵抗性をひき起こすという仮説をたて研究を開始した.
1.セマフォリン3E-プレキシンD1シグナルは肥満における内臓脂肪組織において亢進する
肥満における脂肪組織においてセマフォリンおよびプレキシンの役割を調べるため,マウスに高脂肪高ショ糖食をあたえ食餌誘導性の肥満モデルマウスを作製した.この肥満モデルマウスではマクロファージを主体とする炎症細胞の浸潤がみられ,TNFαやCCL2といった炎症性サイトカインの発現が著明に亢進していた.さらに,インスリン抵抗性や耐糖能の異常といった糖代謝の異常もきたしていた.そこで,肥満における脂肪組織においてセマフォリン3EおよびプレキシンD1の発現を調べたところ,脂肪組織において著明に亢進していた.さらにくわしく調べると,セマフォリン3Eはおもに脂肪細胞の細胞質において,プレキシンD1は脂肪組織へ浸潤した細胞,とくに,マクロファージにおいて発現が亢進していた.そのとき,血中のセマフォリン3Eの濃度も上昇しており,脂肪組織から分泌されるセマフォリン3Eとマクロファージにおいて発現したプレキシンD1との相互作用が,肥満における脂肪組織の炎症に関与している可能性が示唆された.さらに,ヒトの糖尿病の患者においても血中のセマフォリン3Eの濃度が上昇しており,ヒトの代謝性疾患においてもセマフォリン3E-プレキシンD1シグナルが重要なはたらきをしている可能性が示唆された.
2.脂肪組織の炎症におけるセマフォリン3E-プレキシンD1シグナルの役割
肥満におけるセマフォリン3E-プレキシンD1シグナルのはたす役割について詳細に検証するため,肥満モデルマウスにセマフォリン3Eと結合しその作用を阻害するはたらきをもつ可溶性プレキシンD1を投与した.その結果,体重や摂餌量,酸素消費量などの代謝プロファイルは変化しなかったにもかかわらず,脂肪組織の炎症は有意に改善し,インスリン抵抗性や耐糖能の異常といった糖代謝の異常も著明に改善した.セマフォリン3Eホモノックアウトマウスにおいても同様に,肥満における脂肪組織の炎症や糖代謝の異常が著明に改善していたことから,セマフォリン3E-プレキシンD1シグナルは肥満において脂肪組織の炎症や糖代謝の異常を誘導する作用のあることが示唆された.
3.セマフォリン3Eの過剰な発現は脂肪組織の炎症を惹起する
セマフォリン3Eが過剰に発現したときの脂肪組織への影響を調べるため,脂肪組織において特異的にセマフォリン3Eを過剰に発現するマウスを作製した.このマウスに通常食をあたえたとき,脂肪組織および血中のセマフォリン3Eの濃度は著明に上昇しており,脂肪組織ではマクロファージを主体とする炎症細胞の浸潤や炎症性サイトカインの発現の亢進を認めた.さらに,著明な糖代謝の異常もきたしていたが,これはTNFα中和抗体の投与により改善した.
4.セマフォリン3Eはマクロファージ誘導タンパク質としてはたらく
マクロファージなどの炎症細胞はその細胞の表面にCCL2受容体を発現しているため,CCL2が分泌されるとそれに反応して炎症組織や感染組織に炎症細胞の浸潤が誘導されることが知られている.そこで,培養マクロファージ細胞を用いて細胞遊走アッセイを行いマクロファージの誘導性について検証したところ,セマフォリン3EはCCL2と同等にマクロファージを誘導する作用があり,マクロファージにおいてプレキシンD1を抑制するとこの作用は抑制されることがわかった.また,野生型マウスより作製した肥満モデルマウスから採取した脂肪組織を培養した上清を用いて細胞遊走アッセイを行ったときには培養マクロファージ細胞の浸潤が誘導されたが,セマフォリン3Eホモノックアウトマウスより作製した肥満モデルマウスから採取した脂肪組織を培養した上清ではマクロファージの浸潤は抑制された.
セマフォリン3Eは反発性の神経軸索ガイダンスタンパク質としてはたらくときには,プレキシンD1,Nrp1(ニューロピリン1),VEGF受容体2からなる複合体と作用し,PI3K-Aktシグナル伝達経路を活性化させることが知られている4).そこで,培養マクロファージ細胞を用いた細胞遊走アッセイにおいてこれを検証したところ,Nrp1,VEGF受容体2,PI3K,Aktの抑制により,セマフォリン3Eによるマクロファージの誘導作用は著明に抑制され,セマフォリン3EはplexinD1,Nrp1,VEGF受容体2に依存的にマクロファージ誘導タンパク質としてはたらくと考えられた.
5.免疫細胞におけるプレキシンD1の抑制は内臓脂肪組織へのマクロファージの浸潤を抑制する
骨髄細胞において発現するプレキシンD1の脂肪組織の炎症における役割を検証するため,プレキシンD1の発現をノックダウンした骨髄を移植したマウスを作製したところ,このマウスでは肥満における脂肪組織および糖代謝の異常が抑制された.このことから,肥満においてマクロファージの脂肪組織への浸潤は,プレキシンD1を介し誘導されると考えられた.
6.p53の抑制はセマフォリン3Eの発現を抑制し脂肪組織の炎症を改善する
以前に筆者らは,肥満においては酸化ストレスやDNA損傷が蓄積し脂肪組織においてp53が活性化すること,活性化したp53は脂肪組織の炎症を惹起し全身のインスリン抵抗性をひき起こすことを報告した5).そこで,p53とセマフォリン3Eとの関連性について調べるため脂肪組織に特異的なp53ノックアウトマウスを作製したところ,肥満において脂肪組織および血中におけるセマフォリン3Eの濃度の上昇が著明に抑制されており,脂肪組織の炎症や糖代謝の異常も抑制されていた.しかし,このノックアウトマウスに可溶性プレキシンを投与しセマフォリン3E-プレキシンD1シグナルを抑制しても,相加的な改善効果はなかった.このことから,p53に依存性の脂肪組織の炎症においてセマフォリン3E-プレキシンD1シグナルはp53の下流のシグナルとして重要なはたらきをしている可能性が示唆された.
7.p53の活性化はセマフォリン3E-プレキシンD1シグナルを介し脂肪組織の炎症を悪化させる
セマフォリン3Eによる糖代謝の制御におけるp53活性化のはたす役割について検証するため,野生型マウスの脂肪組織にp53活性化剤であるキナクリンを投与した.その結果,脂肪組織および血中においてセマフォリン3Eの濃度が上昇するとともに,脂肪組織の炎症および糖代謝の異常が惹起されたが,これらの変化は脂肪組織に特異的なp53ノックアウトマウスでは起こらず,キナクリンにより誘導される脂肪組織の炎症はp53に依存的なものであると考えられた.さらに,クロマチン免疫沈降法を用いて検証したところ,p53はセマフォリン3E遺伝子のプロモーター領域に結合していることがわかった.また,キナクリンにより脂肪組織のp53を活性化させたマウスに対し可溶性プレキシンD1やTNFα中和抗体を投与したところ,脂肪組織の炎症および糖代謝の異常は改善した.これらの結果より,セマフォリン3Eは肥満におけるp53に依存性の脂肪組織の炎症において重要な役割をはたしていると考えられた.
おわりに
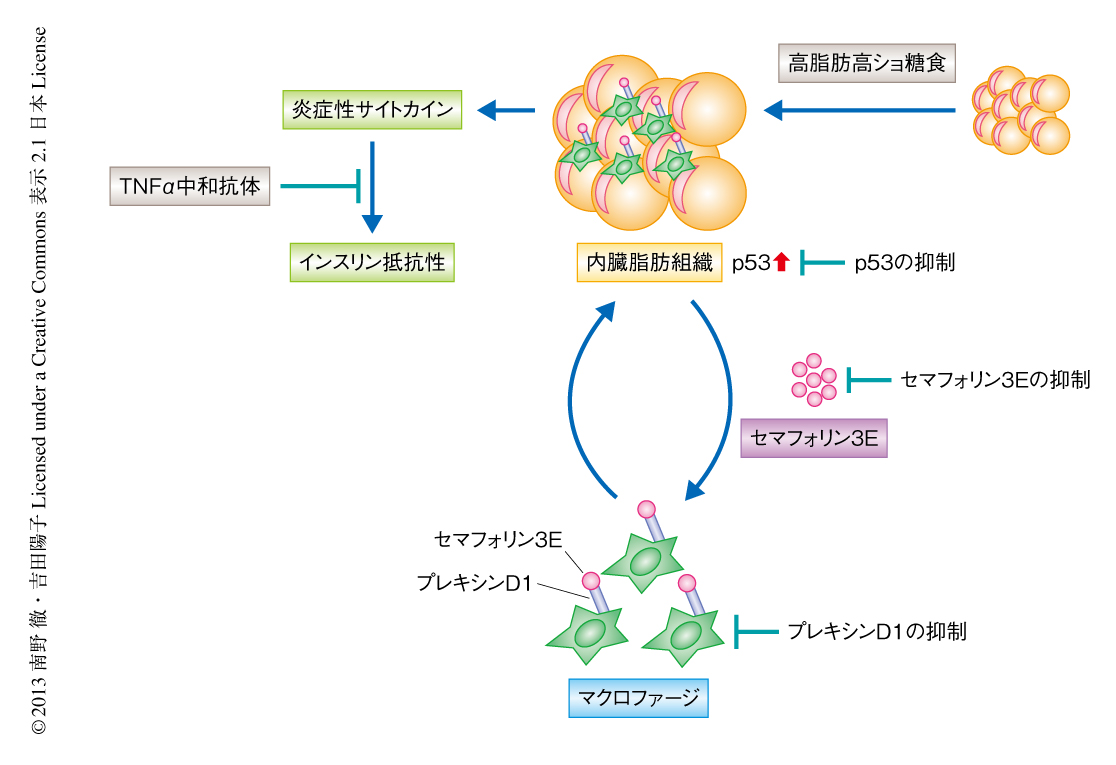
この研究において,筆者らは,セマフォリン3E-プレキシンD1シグナルが脂肪組織の炎症を惹起し,インスリン抵抗性や糖尿病の発症および進展に重要な役割をはたしていることを明らかにした(図1).セマフォリン3EがプレキシンD1陽性マクロファージを誘導し,脂肪組織でのp53の活性化がセマフォリン3Eによるマクロファージの浸潤の誘導を促進することにより,脂肪組織の炎症や糖代謝の異常が惹起されることが明らかになった.がん抑制遺伝子であるp53遺伝子はDNA修復,アポトーシス,老化などに関連し,ゲノムの安定性の維持や発がんの抑制にも寄与している.近年,p53遺伝子は加齢に関連する疾患にも関与することが知られてきており,加齢にともないp53の発現が亢進することや6),p53の持続的な活性化は早期の老化をひき起こすこと7),老化した心血管ではp53の発現が亢進していることなどが報告され8-10),動脈硬化や心不全といった疾患においても重要な役割をはたしていると考えられるようになった.また最近では,代謝異常や代謝制御との関連性を示唆する報告もなされており,以前に筆者らも,肥満における脂肪組織においてp53に依存性の炎症が惹起されることを報告している.この研究では,セマフォリン3E-プレキシンD1シグナルがp53に依存性の脂肪組織の炎症において重要な役割をはたし,このシグナルの抑制が肥満における代謝異常を改善させることを示した.p53それ自体の抑制は発がんを誘導する可能性も考えられることから,セマフォリン3E-プレキシンD1シグナルの抑制は肥満患者の糖代謝の異常に対する新規の治療標的となる可能性が示唆された.
文 献
- Hotamisligil, G. S.: Inflammation and metabolic disorders. Nature, 444, 860-867 (2006)[PubMed]
- Schenk, S., Saberi, M. & Olefsky, J. M.: Insulin sensitivity: modulation by nutrients and inflammation. J. Clin. Invest., 118, 2992-3002 (2008)[PubMed]
- Moriya, J., Minamino, T., Komuro, I. et al.: Inhibition of semaphorin as a novel strategy for therapeutic angiogenesis. Circ. Res., 106, 391-398 (2010)[PubMed]
- Bellon, A., Luchino, J., Mann, F. et al. .: VEGFR2 (KDR/Flk1) signaling mediates axon growth in response to semaphorin 3E in the developing brain. Neuron, 66, 205-219 (2010)[PubMed]
- Minamino, T., Orimo, M., Shimizu, I. et al.: A crucial role for adipose tissue p53 in the regulation of insulin resistance. Nat. Med., 15, 1082-1087 (2009)[PubMed]
- Edwards, M. G., Anderson, R. M., Prolla, T. A. et al.: Gene expression profiling of aging reveals activation of a p53-mediated transcriptional program. BMC Genomics, 8, 80 (2007)[PubMed]
- Tyner, S. D., Venkatachalam, S., Choi, J. et al.: p53 mutant mice that display early ageing-associated phenotypes. Nature, 415, 45-53 (2002)[PubMed]
- Minamino, T. & Komuro, I.: Vascular cell senescence: contribution to atherosclerosis. Circ. Res., 100, 15-26 (2007)[PubMed]
- Minamino, T. & Komuro, I.: Vascular aging: insights from studies on cellular senescence, stem cell aging, and progeroid syndromes. Nat. Clin. Pract. Cardiovasc. Med., 5, 637-648 (2008)[PubMed]
- Sano, M., Minamino, T., Toko, H. et al.: p53-induced inhibition of Hif-1 causes cardiac dysfunction during pressure overload. Nature, 446, 444-448 (2007)[PubMed]
著者プロフィール
略歴:1997年 東京大学大学院医学系研究科にて博士号取得,同年 米国Harvard Medical Schoolリサーチフェロー,2000年 帝京大学医学部 助手,2001年 千葉大学大学院医学研究院 助手,2010年 同 講師を経て,2012年より新潟大学医歯学総合研究科 教授.
研究テーマ:生活習慣病と老化.再生医療.
抱負:加齢に関連する疾患の発症機序の解明を目標としています.
研究室URL:http://www.med.niigata-u.ac.jp/car/index.html
吉田 陽子(Yohko Yoshida)
新潟大学医歯学総合病院 医員.
© 2013 南野 徹・吉田陽子 Licensed under CC 表示 2.1 日本