RNAiは新規の機構を介して特定の遺伝子の発現を抑制する
山中総一郎・Shiv I. S. Grewal
(米国NIH National Cancer Institute,Laboratory of Biochemistry and Molecular Biology)
email:山中総一郎
DOI: 10.7875/first.author.2012.156
RNAi triggered by specialized machinery silences developmental genes and retrotransposons.
Soichiro Yamanaka, Sameet Mehta, Francisca E. Reyes-Turcu, Fanglei Zhuang, Ryan T. Fuchs, Yikang Rong, Gregory B. Robb, Shiv I. S. Grewal
Nature, 493, 557-560 (2013)
RNAiは転写ののち起こる遺伝子の発現抑制機構であり,かつ,セントロメアにみられるようなリピート配列のヘテロクロマチン化を促進する転写段階での遺伝子の発現抑制機構でもある.RNAiは生命現象において重要な役割を担っているのにもかかわらず,標的となる遺伝子の全体像はいまだ明らかにされていない.この論文において,筆者らは,分裂酵母を用いて,RNAiやヘテロクロマチン関連タンパク質がこれまで考えられていたよりもはるかに多様な遺伝子の発現を,RNA分解酵素複合体であるエキソソームとともに抑制することを見い出した.エキソソームの変異体ではこれらの標的遺伝子座におけるsiRNAの産生とヘテロクロマチンの形成が観察された.さらに,この新規の標的遺伝子座からのsiRNAの産生とヘテロクロマチンの形成は,mRNAの3’末端へのポリA鎖の付加に関与するタンパク質により促進されていることも見い出された.以上の結果は,RNAiとエキソソームの機能が重複するように特定の遺伝子の発現を抑制していることを示しており,さらに,この機能的な相互作用が分裂酵母だけでなくショウジョウバエにおいても保存されていることが明らかになった.
ゲノムは三次元的にダイナミックに構築されており,遺伝的に伝達される染色体の高次構造はヘテロクロマチンとよばれる領域において観察される.ヘテロクロマチンはゲノムの恒常性の維持に必須の役割をはたしている.たとえば,遺伝子の発現抑制,正確な染色体分配,異所的な染色体組換えの抑制などがそれにあたる.ゲノムにおけるヘテロクロマチンの形成は時空間的に厳密に制御され,異なる種の細胞がそれぞれの属性を獲得することに寄与している.ヘテロクロマチンの異所的な形成や解体は細胞に傷害をひき起こすことがあり,さらには,高等真核生物において腫瘍の形成にいたることもある.以上のように,ヘテロクロマチンは生体において非常に重要なはたらきをもつにもかかわらず,その形成機構の多くはいまだ明らかになっていない.
筆者らのグループは,分裂酵母を用いて長年にわたりヘテロクロマチンの形成機構を研究してきた.分裂酵母は一倍体の単細胞真核生物であり,外界の栄養源の枯渇に応答してその分裂様式を体細胞分裂(増殖)から減数分裂(配偶子の形成)へとスイッチさせる.分裂酵母においてヘテロクロマチンはセントロメア領域やテロメア領域などに広く分布する.これら領域におけるヘテロクロマチンの形成は細胞周期や外界からの刺激などに左右されず,ヘテロクロマチンはゲノムに安定して存在することから,恒常的ヘテロクロマチンとよばれている.ヒストンH3の9番目のリジン残基のメチル化(H3K9me)はヘテロクロマチン領域に特異的なヒストン修飾で,分裂酵母においてはClr4がこの修飾を担っている.そして,dg/dhリピート配列とよばれる特定のDNAくり返し配列はこれら恒常的ヘテロクロマチンに共通して存在する.
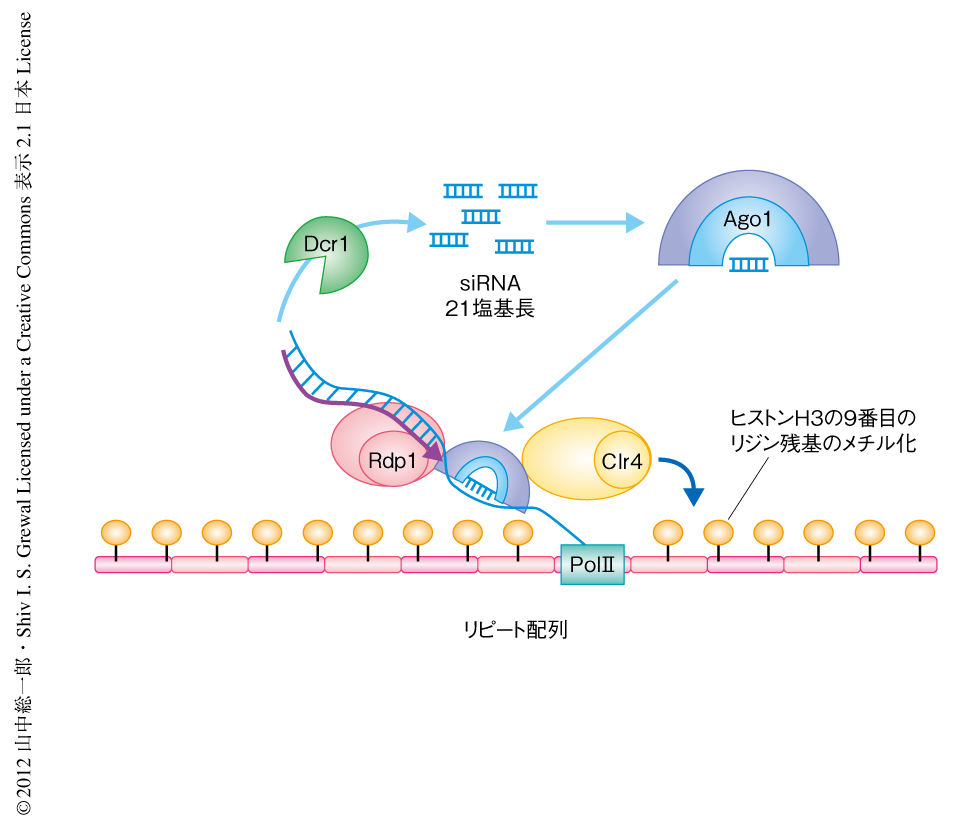
dg/dhリピート配列に由来する転写産物は,ArgonauteのホモログであるAgo1を含むRITS(RNA-induced transcriptional silencing)複合体,RNA依存性RNAポリメラーゼであるRdp1,DicerのホモログであるDcr1,といったRNAi(RNA interference,RNA干渉)に関連する一連のタンパク質によりプロセシングされ,siRNA(small interfering RNA)となる.RITS複合体に含まれるChp1はヒストンH3の9番目のリジン残基のメチル化を特異的に認識するクロモドメインをもつ.Chp1によるヒストンH3の9番目のリジン残基のメチル化の認識と,Ago1に結合したsiRNAと転写産物との相補性という2つの結合能により,RITS複合体はdg/dhリピート配列に呼び込まれる.そして,RITS複合体はClr4を含む複合体を呼び込むことによりヒストンH3の9番目のリジン残基のメチル化を促進すると考えられている(図1).
興味深いことに,Clr4の欠損株ではsiRNAは産生されない.このことは,dg/dhリピート配列からの転写産物をsiRNAに変換することと,Clr4複合体をゲノムに呼び込みヒストンH3の9番目のリジン残基のメチル化を促すことが,連動して起こることを示している.また,ほとんどのsiRNAはヘテロクロマチン領域のdg/dhリピート配列から産生されているという結果は,RNAiとヘテロクロマチンの形成との密接なかかわりを強く支持している.ただし,分裂酵母のゲノムに存在するdg/dhリピート配列とは別種のリピート配列であるレトロトランスポゾンからのsiRNAの産生は現在まで報告されておらず,RNAiはdg/dhリピート配列のもつ特異的な構造を認識していると考えられている1,2).
分裂酵母のゲノムにおいては恒常的ヘテロクロマチンのほかの領域にもヒストンH3の9番目のリジン残基のメチル化のピークが多く存在し,これらはヘテロクロマチンアイランドとよばれている3).ヘテロクロマチンアイランドの多くは分裂酵母が性分化する際に発現する遺伝子座に形成され,外界の栄養源,とくに,窒素源の枯渇に応答して解体する.その性質からヘテロクロマチンアイランドは条件的ヘテロクロマチンのひとつに分類される.そして,ヘテロクロマチンアイランドはRNAiとは異なるRNA分解をつかさどるエキソソームに依存して形成される4).
エキソソームは種間で広く保存されたRNA分解複合体で,そのはたらきは広範囲かつ個体にとり必須なものである.エキソソームはリボソームRNA,snRNA(small nuclear RNA,核内低分子RNA),snoRNA(small nucleolar RNA,核小体低分子RNA)などの3’末端の成熟の過程に必要であり,また,mRNAを含む多種のRNAの品質管理機構においても役割をもつ.エキソソームは基質となるRNAを分解する際に特定のタンパク質と共同してはたらくことが知られている5).TRAMP複合体はそのようなタンパク質のひとつで,基質となるRNAの3’末端へのポリA鎖の付加をとおしエキソソームによる分解を促進する.また,mRNAの3’末端にポリA鎖を付加することでその安定化に寄与することが知られるPla1が,エキソソームによる選択的な分解を促進することも報告されている.
筆者らのグループによるこれまでの結果から,エキソソームはRNAiと同様に,セントロメアからの転写産物を分解することが示されている6).このことは,RNAiとエキソソームがセントロメア領域において基質を共有していることを示している.筆者らは,ゲノムにおいてセントロメア領域のほかの領域でもRNAiがエキソソームと基質の分解を分担している可能性を考えた.そして,RNAiの基質の分解への寄与はエキソソームの変異体においてより顕著に観察されると仮定した.
エキソソームのサブユニットのひとつRrp6を欠損したrrp6変異体におけるsmall RNA(小分子RNA)の産生パターンをディープシークエンシング法により解析した.その際,分裂酵母の全RNAから15~40塩基長のRNAを精製し,それをもとにライブラリーを作製した.分裂酵母においてRNAiが基質に作用する際には,おもに20~24塩基長のsiRNAを産生する.そのため,得られたデータにはsiRNAと非特異的なRNA分解による中間産物の両者が含まれる.そこで,small RNAの産生がRNAiに依存したものであるかどうかを明らかにするため,Ago1を欠損したためにRNAiの起こらないrrp6 ago1二重変異体も同時に解析した.その結果,RNAiに依存したsmall RNAの産生がセントロメアやテロメアといった恒常的ヘテロクロマチンだけでなく,ゲノムにおけるさまざまな領域で観察された.さらに,ChIP-chip(chromatin immuno-precipitation-DNA chip,染色体免疫沈降-DNAチップ)法を用いてrrp6変異体およびrrp6 ago1二重変異体においてヘテロクロマチンのマーカーのひとつであるヒストンH3の9番目のリジン残基のメチル化の分布を同定したところ,small RNAを産生するほとんどの領域においてAgo1に依存的なヒストンH3の9番目のリジン残基のメチル化の上昇がみられた.以降,発見された新たなRNAiの標的部位をヘテロクロマチンドメイン(heterochromatin domain:HOOD)とよぶ.ヘテロクロマチンドメインは性分化の際に発現する遺伝子座や膜貫通ドメインをもつ遺伝子座に多く形成され,それらはヘテロクロマチンアイランドとは異なっていた.また,多くの場合,siRNAの産生される遺伝子の相補鎖には既知の非コードRNAが存在した.この非コードRNAはタンパク質をコードする転写産物と二本鎖RNAを形成することによりRNAiの応答を刺激している可能性がある.
ヘテロクロマチンドメインに含まれる遺伝子座にマップされるsmall RNAを取り出してその長さを調べたところ,20~24塩基長に集中して分布していた.また,small RNAの特異的な長さの分布はAgo1に依存していた.この特徴的な長さの分布は分裂酵母のAgoに取り込まれているsiRNAの長さと一致しており,ヘテロクロマチンドメインから産生されるsmall RNAはsiRNAであることが強く示唆された.さらに,Chp1がrrp6変異体においてヘテロクロマチンドメインに含まれる遺伝子座に局在することも,これら一連のデータと一致した.
レトロトランスポゾンは,ゲノムのある部分からまた別のある部分へとコピー&ペーストされることでそれ自体の配列を増幅することの知られる利己的な遺伝子である.レトロトランスポゾンはゲノムの安定性を負に制御することから,宿主である細胞はその発現を抑制するためさまざまな手段をとることが知られている.レトロトランスポゾンは高等生物においてRNAiにより発現を抑制されている.それに対し,分裂酵母のレトロトランスポゾンであるTf2はヒストンデアセチラーゼを介し転写の段階で発現を抑制されていることが報告されている7).興味深いことに,rrp6変異体においてTf2からのsmall RNAの産生とヒストンH3の9番目のリジン残基のメチル化のレベルの増加が観察された.また,Tf2に由来するsmall RNAの多くはsiRNAと同じく20~24塩基長の特徴的な長さをもち,5’末端にウリジンをもっていた.以上の結果は,rrp6変異体においては分裂酵母のトランスポゾンも高等真核生物と同様にRNAiによる制御をうけていることを表わした.
ヘテロクロマチンドメインの形成はrrp6変異体でのみ観察される特殊な現象ではなかった.野生株を低温や低グルコースといったストレス条件のもと培養したところ,複数のヘテロクロマチンドメインの形成が観察された.そして,この形成はRNAiに依存したものであった.このことは,rrp6変異体は野生型の分裂酵母がより自然な環境にさらされたときの状態を模倣していることを示唆した.
ここまで,ヘテロクロマチンドメインがゲノムにおいてさまざまな領域に形成されていることを示した.では,このヘテロクロマチンドメインに形成されたヘテロクロマチンの意義はなんだろうか? そこで,rrp6変異体とclr4変異体もしくはRNAi欠損株とを掛け合わせた二重変異体を用いてヘテロクロマチンドメインに含まれる遺伝子の転写産物のレベルを観察した.すると,それぞれ単独の変異体における発現量は野生株とほとんど差がないかわずかに上昇するにとどまったの対し,rrp6 clr4二重変異体およびrrp6変異とRNAi欠損との二重変異体においてはこれが著しく増加することが観察された.このことは,RNAiとエキソソームの両方がヘテロクロマチンドメインに含まれる遺伝子座の発現抑制に重要であることを示した.
Red1は古典的なポリA鎖付加酵素であるPla1やポリA鎖結合タンパク質であるPab2,および,エキソソームと協同して,減数分裂に特異的に発現するRNAを体細胞分裂期において分解する8,9).ヘテロクロマチンドメインにコードされているいくつかのRNAには,このRed1の標的となるRNAも含まれていた.驚くべきことに,rrp6 red1二重変異体,rrp6変異とpla1温度感受性変異との二重変異体,rrp6 pab2二重変異体では,ほぼすべてのヘテロクロマチンドメインの形成が阻害された.このことは,エキソソームを活性化すると考えられている一連のタンパク質がRNAiをも活性化する可能性を示した.つまり,Red1,Pla1,Pab2はRNAi経路とエキソソーム経路の2つの経路のハブとしての役割をはたしていることが考えられた.
ヘテロクロマチンドメインに含まれる遺伝子には分裂酵母の性分化の際に発現が誘導されるものが多く含まれていたことから,ヘテロクロマチンドメインの形成が性分化シグナルにより制御されている可能性を検討した.その結果,ほとんどのヘテロクロマチンドメインは性分化シグナルを誘導した際に消滅したのに対し,レトロトランスポゾンに対し形成されたヘテロクロマチンドメインはとどまることが観察された.このことは,性分化シグナルはRNAiを介して特定の領域のクロマチンの状態を初期化することを表わした.
ショウジョウバエを用いて高等真核生物におけるヘテロクロマチンドメインとRNAiとの相互関係を検討した.ショウジョウバエにおいてrrp6ホモ変異体は幼虫の初期段階で成長が止まり死にいたる.そこで,幼虫の全RNAからsmall RNAのライブラリーを作製しその分布を解析した.すると,rrp6ホモ変異体ではrrp6ヘテロ変異体に比べリピート配列に由来するsmall RNAが著しく増加していることが観察された.また,このsmall RNAの大部分は25~28塩基長の長さをもち,また5’末端にウリジンをもっていたことから,piRNA(PIWI-interacting RNA)様のsmall RNAであることが示唆された10).また,small RNAだけでなくリピート配列からの転写産物にも増加がみられた.以上の結果は,エキソソームの変異体においてはRNAiがリピート配列に由来するRNAを効果的に処理していることを示しており,エキソソームとRNAiがその基質を分け合っているという分裂酵母においてみられた現象が,ショウジョウバエにおいても保存されていることが考えられた.
今回の研究において,RNAiやヘテロクロマチン関連タンパク質とエキソソームは性分化の際に発現する遺伝子やレトロトランスポゾンの発現を抑制していることが示された.
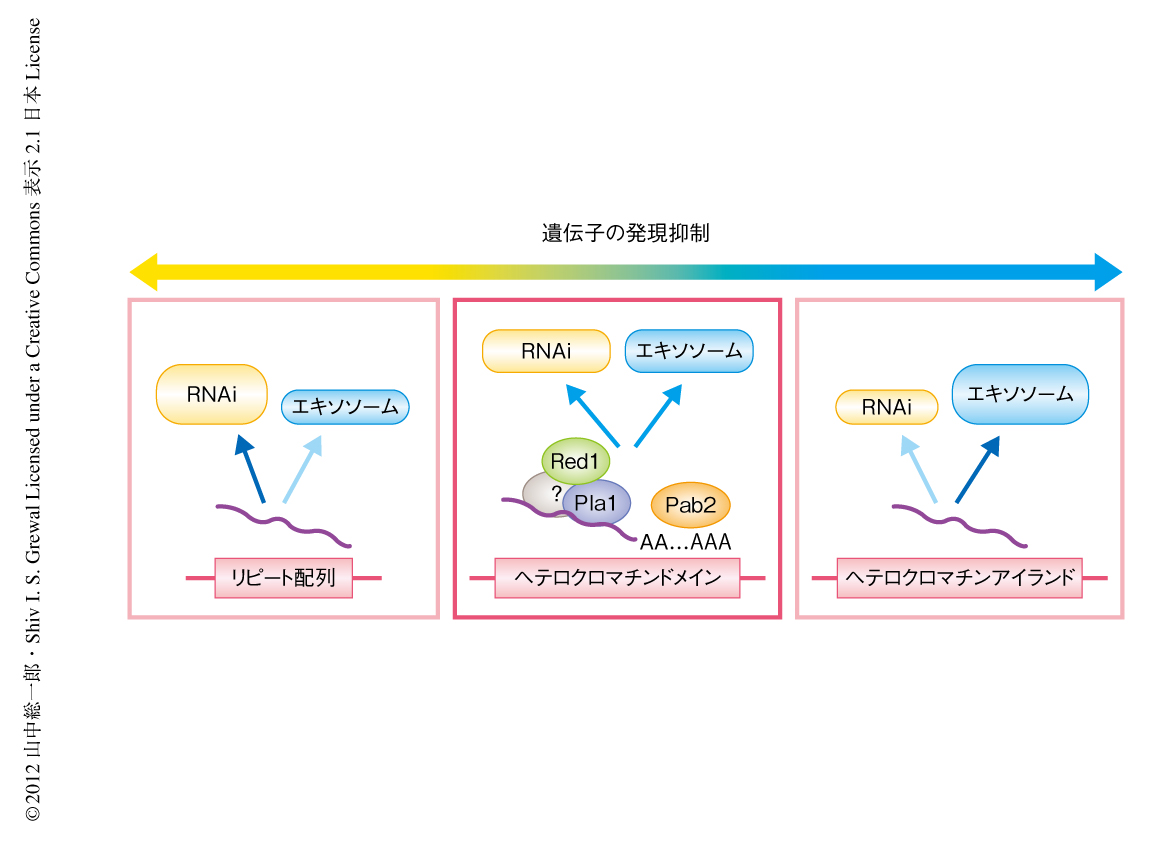
ここで,これまでの知見とこの論文において示された結果から,セントロメア領域,ヘテロクロマチンアイランド,ヘテロクロマチンドメインに共通した遺伝子の発現抑制のしくみに関して考察する.セントロメアのdg/dhリピート配列においてはRNAiとエキソソームが遺伝子の発現抑制に寄与している.そして,遺伝子破壊株の表現型の強さから判断すると,RNAiの寄与がエキソソームに比べ強い.また,ヘテロクロマチンアイランドにおいてもRNAiとエキソソームが遺伝子の発現抑制に関与しているが,遺伝子破壊株の表現型はエキソソームのほうがはるかに強い.これら2つの領域と比べ,ヘテロクロマチンドメインではRNAiあるいはエキソソームの単独の変異体では表現型が弱い,もしくは,ほとんどなく,二重変異体においてはじめて強い表現型がみられたことから,RNAiとエキソソームとが互いを補完するようにして遺伝子の発現抑制を行っていることが示唆された.つまり,RNAiとエキソソームの両者による遺伝子の発現抑制が,程度は違えど,これらヘテロクロマチン領域において共通して起こっていることが考えられた(図2).
rrp6変異体において観察されたsiRNAを産生する領域のすべてが野生株におけるRNAiのターゲットではないかもしれないが,RNAiは外界からの刺激に応答してそのうちのいくつかの領域を制御していた.また,エキソソームはRNAiを活性化するような転写産物もしくはsmall RNAの量を制御しているのかもしれない.このように考えると,RNAiは特定の外界からの刺激に応答してゲノムをリプログラミングする適応機構としての役割をはたしていると考えられる.RNAiはRed1に依存して性分化の際に発現する遺伝子の発現を抑制しているが,Red1は性分化の際に局在が大きく変化する.このことから,Red1,Pla1,Pab2はsiRNAの産生を制御するシグナル経路の標的となっている可能性も考えられる.また,細胞における別のポリA鎖付加酵素のひとつであるTRAMPは,これまで,RNAi経路とエキソソーム経路のどちらの経路も活性化しうることが示唆されている.このことは,同一の遺伝子の発現制御に複数のポリA鎖付加複合体が関与している可能性を示している.実際,複数のヘテロクロマチンドメインにおける遺伝子の発現がTRAMP変異体において脱抑制されることが知られている.今後の課題は,複数のRNAプロセシング機構が分化の際における遺伝子の発現制御,また,ゲノム安定性にどのように寄与しているかを,酵母のみならず高等真核生物において明らかにすることであろう.
略歴:2010年 東京大学大学院理学系研究科 修了,同年より米国NIH National Cancer Instituteにてvisiting fellow.
研究テーマ:RNA分解,エピジェネティクス.
関心事:遺伝子の発現抑制における多様な分子機構を解明したい.
Shiv I. S. Grewal
米国NIH National Cancer InstituteにてSenior Investigator.
© 2012 山中総一郎・Shiv I. S. Grewal Licensed under CC 表示 2.1 日本
(米国NIH National Cancer Institute,Laboratory of Biochemistry and Molecular Biology)
email:山中総一郎
DOI: 10.7875/first.author.2012.156
RNAi triggered by specialized machinery silences developmental genes and retrotransposons.
Soichiro Yamanaka, Sameet Mehta, Francisca E. Reyes-Turcu, Fanglei Zhuang, Ryan T. Fuchs, Yikang Rong, Gregory B. Robb, Shiv I. S. Grewal
Nature, 493, 557-560 (2013)
要 約
RNAiは転写ののち起こる遺伝子の発現抑制機構であり,かつ,セントロメアにみられるようなリピート配列のヘテロクロマチン化を促進する転写段階での遺伝子の発現抑制機構でもある.RNAiは生命現象において重要な役割を担っているのにもかかわらず,標的となる遺伝子の全体像はいまだ明らかにされていない.この論文において,筆者らは,分裂酵母を用いて,RNAiやヘテロクロマチン関連タンパク質がこれまで考えられていたよりもはるかに多様な遺伝子の発現を,RNA分解酵素複合体であるエキソソームとともに抑制することを見い出した.エキソソームの変異体ではこれらの標的遺伝子座におけるsiRNAの産生とヘテロクロマチンの形成が観察された.さらに,この新規の標的遺伝子座からのsiRNAの産生とヘテロクロマチンの形成は,mRNAの3’末端へのポリA鎖の付加に関与するタンパク質により促進されていることも見い出された.以上の結果は,RNAiとエキソソームの機能が重複するように特定の遺伝子の発現を抑制していることを示しており,さらに,この機能的な相互作用が分裂酵母だけでなくショウジョウバエにおいても保存されていることが明らかになった.
はじめに
ゲノムは三次元的にダイナミックに構築されており,遺伝的に伝達される染色体の高次構造はヘテロクロマチンとよばれる領域において観察される.ヘテロクロマチンはゲノムの恒常性の維持に必須の役割をはたしている.たとえば,遺伝子の発現抑制,正確な染色体分配,異所的な染色体組換えの抑制などがそれにあたる.ゲノムにおけるヘテロクロマチンの形成は時空間的に厳密に制御され,異なる種の細胞がそれぞれの属性を獲得することに寄与している.ヘテロクロマチンの異所的な形成や解体は細胞に傷害をひき起こすことがあり,さらには,高等真核生物において腫瘍の形成にいたることもある.以上のように,ヘテロクロマチンは生体において非常に重要なはたらきをもつにもかかわらず,その形成機構の多くはいまだ明らかになっていない.
筆者らのグループは,分裂酵母を用いて長年にわたりヘテロクロマチンの形成機構を研究してきた.分裂酵母は一倍体の単細胞真核生物であり,外界の栄養源の枯渇に応答してその分裂様式を体細胞分裂(増殖)から減数分裂(配偶子の形成)へとスイッチさせる.分裂酵母においてヘテロクロマチンはセントロメア領域やテロメア領域などに広く分布する.これら領域におけるヘテロクロマチンの形成は細胞周期や外界からの刺激などに左右されず,ヘテロクロマチンはゲノムに安定して存在することから,恒常的ヘテロクロマチンとよばれている.ヒストンH3の9番目のリジン残基のメチル化(H3K9me)はヘテロクロマチン領域に特異的なヒストン修飾で,分裂酵母においてはClr4がこの修飾を担っている.そして,dg/dhリピート配列とよばれる特定のDNAくり返し配列はこれら恒常的ヘテロクロマチンに共通して存在する.
dg/dhリピート配列に由来する転写産物は,ArgonauteのホモログであるAgo1を含むRITS(RNA-induced transcriptional silencing)複合体,RNA依存性RNAポリメラーゼであるRdp1,DicerのホモログであるDcr1,といったRNAi(RNA interference,RNA干渉)に関連する一連のタンパク質によりプロセシングされ,siRNA(small interfering RNA)となる.RITS複合体に含まれるChp1はヒストンH3の9番目のリジン残基のメチル化を特異的に認識するクロモドメインをもつ.Chp1によるヒストンH3の9番目のリジン残基のメチル化の認識と,Ago1に結合したsiRNAと転写産物との相補性という2つの結合能により,RITS複合体はdg/dhリピート配列に呼び込まれる.そして,RITS複合体はClr4を含む複合体を呼び込むことによりヒストンH3の9番目のリジン残基のメチル化を促進すると考えられている(図1).
興味深いことに,Clr4の欠損株ではsiRNAは産生されない.このことは,dg/dhリピート配列からの転写産物をsiRNAに変換することと,Clr4複合体をゲノムに呼び込みヒストンH3の9番目のリジン残基のメチル化を促すことが,連動して起こることを示している.また,ほとんどのsiRNAはヘテロクロマチン領域のdg/dhリピート配列から産生されているという結果は,RNAiとヘテロクロマチンの形成との密接なかかわりを強く支持している.ただし,分裂酵母のゲノムに存在するdg/dhリピート配列とは別種のリピート配列であるレトロトランスポゾンからのsiRNAの産生は現在まで報告されておらず,RNAiはdg/dhリピート配列のもつ特異的な構造を認識していると考えられている1,2).
分裂酵母のゲノムにおいては恒常的ヘテロクロマチンのほかの領域にもヒストンH3の9番目のリジン残基のメチル化のピークが多く存在し,これらはヘテロクロマチンアイランドとよばれている3).ヘテロクロマチンアイランドの多くは分裂酵母が性分化する際に発現する遺伝子座に形成され,外界の栄養源,とくに,窒素源の枯渇に応答して解体する.その性質からヘテロクロマチンアイランドは条件的ヘテロクロマチンのひとつに分類される.そして,ヘテロクロマチンアイランドはRNAiとは異なるRNA分解をつかさどるエキソソームに依存して形成される4).
エキソソームは種間で広く保存されたRNA分解複合体で,そのはたらきは広範囲かつ個体にとり必須なものである.エキソソームはリボソームRNA,snRNA(small nuclear RNA,核内低分子RNA),snoRNA(small nucleolar RNA,核小体低分子RNA)などの3’末端の成熟の過程に必要であり,また,mRNAを含む多種のRNAの品質管理機構においても役割をもつ.エキソソームは基質となるRNAを分解する際に特定のタンパク質と共同してはたらくことが知られている5).TRAMP複合体はそのようなタンパク質のひとつで,基質となるRNAの3’末端へのポリA鎖の付加をとおしエキソソームによる分解を促進する.また,mRNAの3’末端にポリA鎖を付加することでその安定化に寄与することが知られるPla1が,エキソソームによる選択的な分解を促進することも報告されている.
筆者らのグループによるこれまでの結果から,エキソソームはRNAiと同様に,セントロメアからの転写産物を分解することが示されている6).このことは,RNAiとエキソソームがセントロメア領域において基質を共有していることを示している.筆者らは,ゲノムにおいてセントロメア領域のほかの領域でもRNAiがエキソソームと基質の分解を分担している可能性を考えた.そして,RNAiの基質の分解への寄与はエキソソームの変異体においてより顕著に観察されると仮定した.
1.ゲノムの多くの領域においてRNAiに依存したヘテロクロマチンの形成が観察される
エキソソームのサブユニットのひとつRrp6を欠損したrrp6変異体におけるsmall RNA(小分子RNA)の産生パターンをディープシークエンシング法により解析した.その際,分裂酵母の全RNAから15~40塩基長のRNAを精製し,それをもとにライブラリーを作製した.分裂酵母においてRNAiが基質に作用する際には,おもに20~24塩基長のsiRNAを産生する.そのため,得られたデータにはsiRNAと非特異的なRNA分解による中間産物の両者が含まれる.そこで,small RNAの産生がRNAiに依存したものであるかどうかを明らかにするため,Ago1を欠損したためにRNAiの起こらないrrp6 ago1二重変異体も同時に解析した.その結果,RNAiに依存したsmall RNAの産生がセントロメアやテロメアといった恒常的ヘテロクロマチンだけでなく,ゲノムにおけるさまざまな領域で観察された.さらに,ChIP-chip(chromatin immuno-precipitation-DNA chip,染色体免疫沈降-DNAチップ)法を用いてrrp6変異体およびrrp6 ago1二重変異体においてヘテロクロマチンのマーカーのひとつであるヒストンH3の9番目のリジン残基のメチル化の分布を同定したところ,small RNAを産生するほとんどの領域においてAgo1に依存的なヒストンH3の9番目のリジン残基のメチル化の上昇がみられた.以降,発見された新たなRNAiの標的部位をヘテロクロマチンドメイン(heterochromatin domain:HOOD)とよぶ.ヘテロクロマチンドメインは性分化の際に発現する遺伝子座や膜貫通ドメインをもつ遺伝子座に多く形成され,それらはヘテロクロマチンアイランドとは異なっていた.また,多くの場合,siRNAの産生される遺伝子の相補鎖には既知の非コードRNAが存在した.この非コードRNAはタンパク質をコードする転写産物と二本鎖RNAを形成することによりRNAiの応答を刺激している可能性がある.
ヘテロクロマチンドメインに含まれる遺伝子座にマップされるsmall RNAを取り出してその長さを調べたところ,20~24塩基長に集中して分布していた.また,small RNAの特異的な長さの分布はAgo1に依存していた.この特徴的な長さの分布は分裂酵母のAgoに取り込まれているsiRNAの長さと一致しており,ヘテロクロマチンドメインから産生されるsmall RNAはsiRNAであることが強く示唆された.さらに,Chp1がrrp6変異体においてヘテロクロマチンドメインに含まれる遺伝子座に局在することも,これら一連のデータと一致した.
レトロトランスポゾンは,ゲノムのある部分からまた別のある部分へとコピー&ペーストされることでそれ自体の配列を増幅することの知られる利己的な遺伝子である.レトロトランスポゾンはゲノムの安定性を負に制御することから,宿主である細胞はその発現を抑制するためさまざまな手段をとることが知られている.レトロトランスポゾンは高等生物においてRNAiにより発現を抑制されている.それに対し,分裂酵母のレトロトランスポゾンであるTf2はヒストンデアセチラーゼを介し転写の段階で発現を抑制されていることが報告されている7).興味深いことに,rrp6変異体においてTf2からのsmall RNAの産生とヒストンH3の9番目のリジン残基のメチル化のレベルの増加が観察された.また,Tf2に由来するsmall RNAの多くはsiRNAと同じく20~24塩基長の特徴的な長さをもち,5’末端にウリジンをもっていた.以上の結果は,rrp6変異体においては分裂酵母のトランスポゾンも高等真核生物と同様にRNAiによる制御をうけていることを表わした.
2.ヘテロクロマチンドメインは野生株においても観察される
ヘテロクロマチンドメインの形成はrrp6変異体でのみ観察される特殊な現象ではなかった.野生株を低温や低グルコースといったストレス条件のもと培養したところ,複数のヘテロクロマチンドメインの形成が観察された.そして,この形成はRNAiに依存したものであった.このことは,rrp6変異体は野生型の分裂酵母がより自然な環境にさらされたときの状態を模倣していることを示唆した.
3.RNAiはエキソソームとともにヘテロクロマチンドメインに含まれる遺伝子座の発現抑制に寄与する
ここまで,ヘテロクロマチンドメインがゲノムにおいてさまざまな領域に形成されていることを示した.では,このヘテロクロマチンドメインに形成されたヘテロクロマチンの意義はなんだろうか? そこで,rrp6変異体とclr4変異体もしくはRNAi欠損株とを掛け合わせた二重変異体を用いてヘテロクロマチンドメインに含まれる遺伝子の転写産物のレベルを観察した.すると,それぞれ単独の変異体における発現量は野生株とほとんど差がないかわずかに上昇するにとどまったの対し,rrp6 clr4二重変異体およびrrp6変異とRNAi欠損との二重変異体においてはこれが著しく増加することが観察された.このことは,RNAiとエキソソームの両方がヘテロクロマチンドメインに含まれる遺伝子座の発現抑制に重要であることを示した.
4.RNAiとエキソソームは同一のタンパク質により活性化される
Red1は古典的なポリA鎖付加酵素であるPla1やポリA鎖結合タンパク質であるPab2,および,エキソソームと協同して,減数分裂に特異的に発現するRNAを体細胞分裂期において分解する8,9).ヘテロクロマチンドメインにコードされているいくつかのRNAには,このRed1の標的となるRNAも含まれていた.驚くべきことに,rrp6 red1二重変異体,rrp6変異とpla1温度感受性変異との二重変異体,rrp6 pab2二重変異体では,ほぼすべてのヘテロクロマチンドメインの形成が阻害された.このことは,エキソソームを活性化すると考えられている一連のタンパク質がRNAiをも活性化する可能性を示した.つまり,Red1,Pla1,Pab2はRNAi経路とエキソソーム経路の2つの経路のハブとしての役割をはたしていることが考えられた.
5.ヘテロクロマチンドメインの形成は性分化シグナルにより制御されている
ヘテロクロマチンドメインに含まれる遺伝子には分裂酵母の性分化の際に発現が誘導されるものが多く含まれていたことから,ヘテロクロマチンドメインの形成が性分化シグナルにより制御されている可能性を検討した.その結果,ほとんどのヘテロクロマチンドメインは性分化シグナルを誘導した際に消滅したのに対し,レトロトランスポゾンに対し形成されたヘテロクロマチンドメインはとどまることが観察された.このことは,性分化シグナルはRNAiを介して特定の領域のクロマチンの状態を初期化することを表わした.
6.ショウジョウバエにおいてもRNAiとエキソソームは基質となるRNAを共有する
ショウジョウバエを用いて高等真核生物におけるヘテロクロマチンドメインとRNAiとの相互関係を検討した.ショウジョウバエにおいてrrp6ホモ変異体は幼虫の初期段階で成長が止まり死にいたる.そこで,幼虫の全RNAからsmall RNAのライブラリーを作製しその分布を解析した.すると,rrp6ホモ変異体ではrrp6ヘテロ変異体に比べリピート配列に由来するsmall RNAが著しく増加していることが観察された.また,このsmall RNAの大部分は25~28塩基長の長さをもち,また5’末端にウリジンをもっていたことから,piRNA(PIWI-interacting RNA)様のsmall RNAであることが示唆された10).また,small RNAだけでなくリピート配列からの転写産物にも増加がみられた.以上の結果は,エキソソームの変異体においてはRNAiがリピート配列に由来するRNAを効果的に処理していることを示しており,エキソソームとRNAiがその基質を分け合っているという分裂酵母においてみられた現象が,ショウジョウバエにおいても保存されていることが考えられた.
おわりに
今回の研究において,RNAiやヘテロクロマチン関連タンパク質とエキソソームは性分化の際に発現する遺伝子やレトロトランスポゾンの発現を抑制していることが示された.
ここで,これまでの知見とこの論文において示された結果から,セントロメア領域,ヘテロクロマチンアイランド,ヘテロクロマチンドメインに共通した遺伝子の発現抑制のしくみに関して考察する.セントロメアのdg/dhリピート配列においてはRNAiとエキソソームが遺伝子の発現抑制に寄与している.そして,遺伝子破壊株の表現型の強さから判断すると,RNAiの寄与がエキソソームに比べ強い.また,ヘテロクロマチンアイランドにおいてもRNAiとエキソソームが遺伝子の発現抑制に関与しているが,遺伝子破壊株の表現型はエキソソームのほうがはるかに強い.これら2つの領域と比べ,ヘテロクロマチンドメインではRNAiあるいはエキソソームの単独の変異体では表現型が弱い,もしくは,ほとんどなく,二重変異体においてはじめて強い表現型がみられたことから,RNAiとエキソソームとが互いを補完するようにして遺伝子の発現抑制を行っていることが示唆された.つまり,RNAiとエキソソームの両者による遺伝子の発現抑制が,程度は違えど,これらヘテロクロマチン領域において共通して起こっていることが考えられた(図2).
rrp6変異体において観察されたsiRNAを産生する領域のすべてが野生株におけるRNAiのターゲットではないかもしれないが,RNAiは外界からの刺激に応答してそのうちのいくつかの領域を制御していた.また,エキソソームはRNAiを活性化するような転写産物もしくはsmall RNAの量を制御しているのかもしれない.このように考えると,RNAiは特定の外界からの刺激に応答してゲノムをリプログラミングする適応機構としての役割をはたしていると考えられる.RNAiはRed1に依存して性分化の際に発現する遺伝子の発現を抑制しているが,Red1は性分化の際に局在が大きく変化する.このことから,Red1,Pla1,Pab2はsiRNAの産生を制御するシグナル経路の標的となっている可能性も考えられる.また,細胞における別のポリA鎖付加酵素のひとつであるTRAMPは,これまで,RNAi経路とエキソソーム経路のどちらの経路も活性化しうることが示唆されている.このことは,同一の遺伝子の発現制御に複数のポリA鎖付加複合体が関与している可能性を示している.実際,複数のヘテロクロマチンドメインにおける遺伝子の発現がTRAMP変異体において脱抑制されることが知られている.今後の課題は,複数のRNAプロセシング機構が分化の際における遺伝子の発現制御,また,ゲノム安定性にどのように寄与しているかを,酵母のみならず高等真核生物において明らかにすることであろう.
文 献
- Matzke, M. A. & Birchler, J. A.: RNAi-mediated pathways in the nucleus. Nat. Rev. Genet., 6, 24-35 (2005)[PubMed]
- Reyes-Turcu, F. E. & Grewal, S. I.: Different means, same end-heterochromatin formation by RNAi and RNAi-independent RNA processing factors in fission yeast. Curr. Opin. Genet. Dev., 22, 156-163 (2012)[PubMed]
- Cam, H. P., Sugiyama, T., Chen, E. S. et al.: Comprehensive analysis of heterochromatin- and RNAi-mediated epigenetic control of the fission yeast genome. Nat. Genet., 37, 809-819 (2005)[PubMed]
- Zofall, M., Yamanaka, S., Reyes-Turcu, F. E. et al.: RNA elimination machinery targeting meiotic mRNAs promotes facultative heterochromatin formation. Science, 335, 96-100 (2012)[PubMed]
- Houseley, J., LaCava, J. & Tollervey, D.: RNA-quality control by the exosome. Nat. Rev. Mol. Cell Biol., 7, 529-539 (2006)[PubMed]
- Reyes-Turcu, F. E., Zhang, K., Zofall, M. et al.: Defects in RNA quality control factors reveal RNAi-independent nucleation of heterochromatin. Nat. Struct. Mol. Biol., 18, 1132-1138 (2011)[PubMed]
- Cam, H. P., Noma, K., Ebina, H. et al.: Host genome surveillance for retrotransposons by transposon-derived proteins. Nature, 451, 431-436 (2008)[PubMed]
- Sugiyama, T. & Sugioka-Sugiyama, R.: Red1 promotes the elimination of meiosis-specific mRNAs in vegetatively growing fission yeast. EMBO J., 30, 1027-1039 (2011)[PubMed]
- Yamanaka, S., Yamashita, A., Harigaya, Y. et al.: Importance of polyadenylation in the selective elimination of meiotic mRNAs in growing S. pombe cells. EMBO J., 29, 2173-2181 (2010)[PubMed]
- Senti, K. A. & Brennecke, J.: The piRNA pathway: a fly's perspective on the guardian of the genome. Trends Genet., 26, 499-509 (2010)[PubMed]
著者プロフィール
略歴:2010年 東京大学大学院理学系研究科 修了,同年より米国NIH National Cancer Instituteにてvisiting fellow.
研究テーマ:RNA分解,エピジェネティクス.
関心事:遺伝子の発現抑制における多様な分子機構を解明したい.
Shiv I. S. Grewal
米国NIH National Cancer InstituteにてSenior Investigator.
© 2012 山中総一郎・Shiv I. S. Grewal Licensed under CC 表示 2.1 日本