パーキンソン病の原因遺伝子LRRK2の変異によりひき起こされるヒトの神経幹細胞における進行性の変性
鈴木啓一郎・Juan Carlos Izpisua Belmonte
(米国Salk Institute for Biological Studies,Gene Expression Laboratory)
email:鈴木啓一郎
DOI: 10.7875/first.author.2012.141
Progressive degeneration of human neural stem cells caused by pathogenic LRRK2.
Guang-Hui Liu, Jing Qu, Keiichiro Suzuki, Emmanuel Nivet, Mo Li, Nuria Montserrat, Fei Yi, Xiuling Xu, Sergio Ruiz, Weiqi Zhang, Ulrich Wagner, Audrey Kim, Bing Ren, Ying Li, April Goebl, Jessica Kim, Rupa Devi Soligalla, Ilir Dubova, James Thompson, John Yates III, Concepcion Rodriguez Esteban, Ignacio Sancho-Martinez, Juan Carlos Izpisua Belmonte
Nature, 491, 603-607 (2012)
核膜の崩壊は多くの遺伝性疾患の原因,あるいは,老化現象のひとつとして知られている.この研究では,加齢にともない発症率の高くなる神経変性疾患であるパーキンソン病における原因遺伝子のひとつLRRK2遺伝子について,もっとも高い頻度でみられる変異をもつ患者に由来する細胞を用い解析した.患者の皮膚細胞からiPS細胞を樹立して神経幹細胞に分化させ,老化を模倣する目的で培養皿において継代をくり返したところ,健常者から同様に分化させた神経幹細胞に比べ,核膜の変形やニューロンへの分化能の低下が有意に観察された.また,これらの神経幹細胞においてみられた表現型は,iPS細胞においてこのLRRK2遺伝子の変異を特異的に修復することにより消失し,逆に,同じ変異をヒトのES細胞に導入することにより再現できたことから,この変異が原因であることが確認された.さらに,この変異をもつパーキンソン病の患者の脳の組織を解析したところ,健常者に比べ核膜の変形が高頻度にみられた.以上の解析により,iPS技術を用いることでパーキンソン病における老化に依存した核膜の崩壊という新たな表現型を発見し,将来的な診断や治療の分子標的としての可能性を示すことができた.
核膜は真核生物において核と細胞質とを隔てる,内膜と外膜の2層の脂質からなる構造体であり,内膜の内側には核の構造維持と転写の制御を行う線維状タンパク質であるラミンが存在する.ヒトではA型ラミンおよびC型ラミンをLMNA遺伝子が,B型ラミンであるラミンB1とラミンB2をLMNB1遺伝子とLMNB2遺伝子がそれぞれコードしており,ほかの膜タンパク質とともに核ラミナを形成している.核膜は細胞にとり非常に重要な役割をはたしており,核膜の崩壊はさまざまな遺伝性疾患や老化した細胞において認められている1-5).
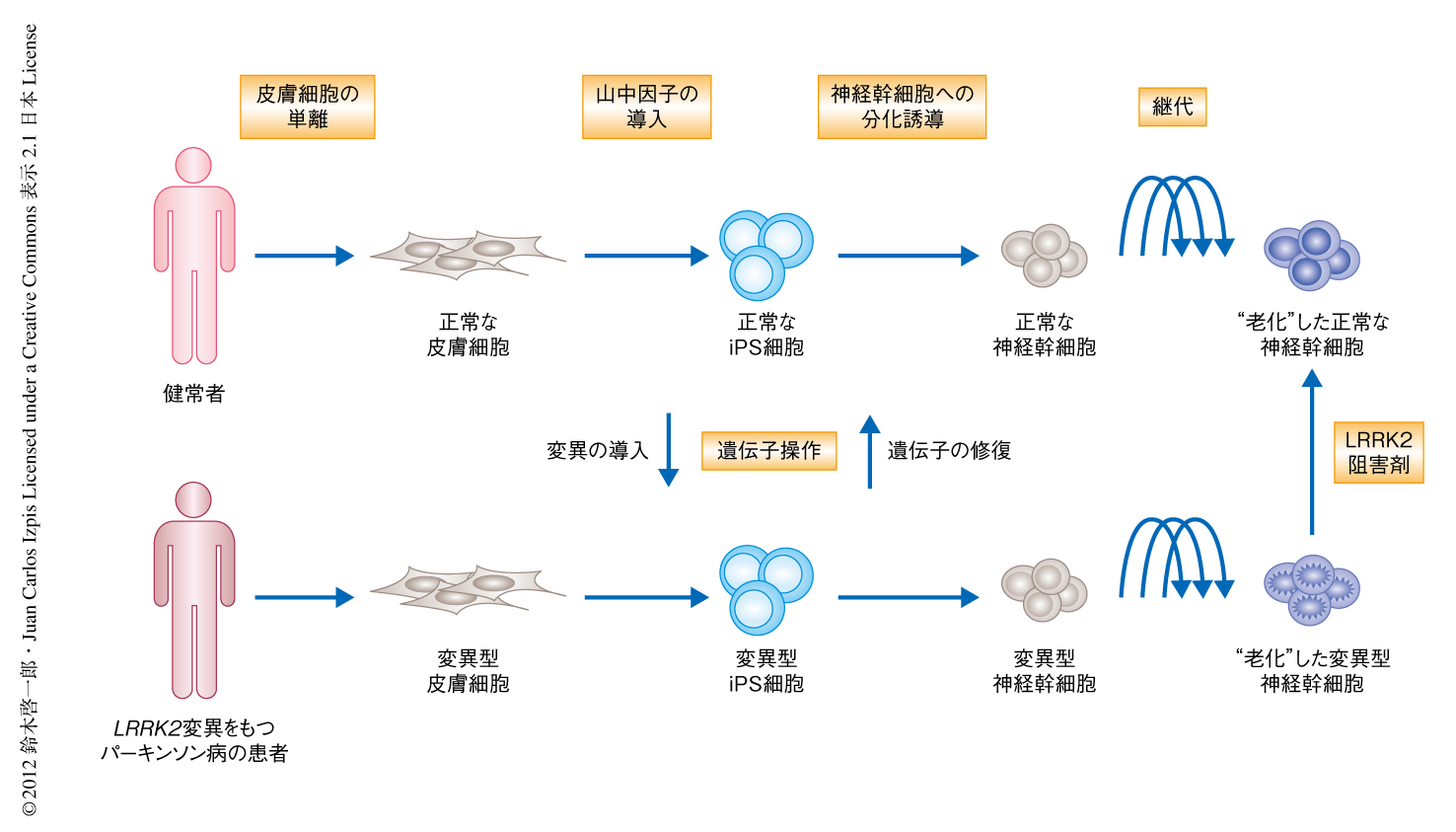
この研究では,老化した細胞に観察される核膜の変性と,加齢にともない発症リスクの高まる神経変性疾患のひとつであるパーキンソン病との関係に注目した.パーキンソン病はアルツハイマー病についで世界で2番目に多い神経変性疾患で,神経伝達物質であるドーパミンを産生するニューロンの変性を主体とする進行性の疾患であり,さまざまな運動障害をひき起こす6).しかし,その病因や分子機構についていまだ不明な点が多く,根本的な治療法は皆無である.その要因のひとつとして,これまでヒトにおいてはニューロンを用いた研究が困難であることがあげられてきた.しかしながら,2012年にノーベル医学賞を受賞した山中伸弥らによるiPS細胞(induced pluripotent stem cell,人工多能性幹細胞)の開発により,疾患患者の皮膚細胞よりiPS細胞を樹立し,さらにそれをニューロンに分化させることで,疾患の分子機構の解明や創薬スクリーニングへ利用することが可能になった7).しかし実際には,遺伝的な背景による影響は大きく,たとえ親子に由来する細胞であっても別個体のあいだでの比較はむずかしく,厳密な比較対照のないことがヒトにおける解析のうえでのつぎなる課題となっていた.以前に,筆者らは,ヒト細胞を用いて相同組換えにより染色体において特定の標的遺伝子を自由に改変する技術を開発し8),この技術を用いて同一の遺伝的な背景をもつ遺伝子を修復した細胞を作製した.今回は,これらの技術を組み合わせることにより,パーキンソン病において老化に関連する疾患の分子機構の解明をめざし研究を行った(図1).
加齢にともない症状の現われるパーキンソン病において,変異の割合のもっとも高い,LRRK2の2019番目のグリシン残基がセリン残基となる変異に注目した.この変異ではLRRK2遺伝子のキナーゼドメインに一塩基置換が生じ,LRRK2のもつリン酸化酵素活性が過剰に高くなっている.まず,このLRRK2変異タンパク質に結合する新規のタンパク質を探索した.HeLa細胞においてこのLRRK2変異タンパク質を過剰発現させプロテオーム解析を行った結果,既知の結合タンパク質にくわえ,新たに多くの核膜構成タンパク質の結合が認められた.また,このLRRK2変異タンパク質を過剰発現することにより核膜の変形が観察された.これらの結果から,2019番目のグリシン残基がセリン残基に変異したLRRK2と核膜とのつながりが示唆された.
ヒトのLRRK2の2019番目のグリシン残基がセリン残基となる変異をもつトランスジェニックマウスでは,成熟ののち神経の新生に異常をきたすことが報告されている9).そこで,このLRRK2変異をもつパーキンソン病患者の皮膚細胞に3つの転写因子Oct3/4,Sox2,Klf4(山中因子)を導入することによりiPS細胞を樹立した.つづいて,樹立したiPS細胞を神経幹細胞に分化させた.神経幹細胞は自己複製能をもつため継代をくり返すことができる.老化を模倣する目的で培養皿においてこの神経幹細胞の継代をくり返したところ,継代数が14をこえるとこのLRRK2変異をもつ神経幹細胞でのみ核膜の変形が観察され,継代が進むにつれその表現型は顕著となった.また,このLRRK2変異タンパク質を過剰発現させることにより,この変異をもたない神経幹細胞においても核膜に異常がみられた.さらに,免疫染色法により,調べた核膜構成タンパク質のうちラミンB1とラミンB2のB型ラミンのみ,変形した核膜において部分的に局在が欠失していることがわかった.免疫共沈降法により,神経幹細胞においてもB型ラミンとLRRK2変異タンパク質は複合体を形成することが確認され,継代を重ねたLRRK2変異をもつ神経幹細胞においてB型ラミンの過剰なリン酸化が観察された.以上の結果より,LRRK2の2019番目のグリシン残基がセリン残基となる変異をもつ神経幹細胞は,継代をくり返すことによりB型ラミンを過剰にリン酸化し,その核膜における局在が部分的に失われ核が変形してしまうことが示唆された.
一方,パーキンソン病の原因のひとつとされるミトコンドリアの異常10) は,継代を重ねたこのLRRK2変異をもつ神経幹細胞においてはみられなかった.また,パーキンソン病患者の皮膚から得た線維芽細胞,あるいは,パーキンソン病患者の皮膚から樹立されたiPS細胞においては,継代を重ねても核膜に異常はみられず,この表現型は神経幹細胞に特異的なものであることが示唆された.
継代を重ね核膜の変形したこのLRRK2変異をもつ神経幹細胞をよりくわしく解析したところ,プロモーター領域において老化したニューロンの指標のひとつとされるヒストンH3の4番目のリジン残基のトリメチル化11) に異常をきたしていることが全ゲノムレベルの解析により明らかになった.また,健常者に由来する神経幹細胞に比べ,クローン増殖力およびニューロンへの分化能が有意に低下していた.興味深いことに,タンパク質分解にかかわるプロテオソームの阻害剤をくわえると,このLRRK2変異をもつ神経幹細胞は継代数に依存することなくアポトーシスによる細胞死が増加した.
これまでの解析の結果はLRRK2の2019番目のグリシン残基がセリン残基となる変異によることを証明するため,筆者らが以前に開発した,安全なアデノウイルスベクターによる高効率な遺伝子ターゲッティング技術8) を用いて,このLRRK2変異をもつiPS細胞において変異遺伝子の修復を行うことにより,遺伝的な背景の同一なLRRK2変異をもたないiPS細胞を作製した.このiPS細胞を神経幹細胞に分化させたところ,LRRK2変異をもつ神経幹細胞にみられた表現型は消失した.同じ技術を用いて,逆に,ヒトのES細胞(embryonic stem cell,胚性幹細胞)にLRRK2変異を導入したところ,このLRRK2変異をもつ神経幹細胞と同様の表現型がみられた.これらの結果から,パーキンソン病の患者に由来する神経幹細胞における核膜の変形など継代に依存的な表現型は,LRRK2の2019番目のグリシン残基がセリン残基となる変異が原因であることが強く示唆された.
LRRK2の2019番目のグリシン残基がセリン残基となる変異は,LRRK2のもつセリン/スレオニンリン酸化活性が過剰にはたらくことでパーキンソン病の原因となっていることが示唆されている10,12).実際に,このLRRK2変異をもつ神経幹細胞では継代に依存してさまざまな基質が過剰にリン酸化されており,これが核膜の変形など表現型の原因になっている可能性が考えられた.そこで,すでに知られているLRRK2によるリン酸化の阻害剤13,14) により処理したところ,継代を重ねたこのLRRK2変異をもつ神経幹細胞においてLRRK2の標的となる基質のリン酸化は減少し核膜の変形など表現型はレスキューされた.このことから,LRRK2の2019番目のグリシン残基がセリン残基となる変異による神経幹細胞でみられる表現型は可逆的であり,薬剤により治療が可能であるため将来的な創薬の標的となりうることが示唆された.
これらin vitroにおいて得られた新しい知見が生体において生じているかどうか確認するため,パーキンソン病の患者と年齢がほぼ同じ健常者の脳組織のスライスを作製し,成人の脳でも神経幹細胞が存在する海馬歯状回において免疫染色法により核膜の形状を調べた.その結果,LRRK2の2019番目のグリシン残基がセリン残基となる変異をもつパーキンソン病の患者では,健常者に比べ核膜の変形が有意に多くみられた.興味深いことに,これ以外の変異をもつパーキンソン病の患者においても中程度に核膜の変形がみられた.このようなほかの変異によるパーキンソン病と核膜との関係については,今後,よりくわしい解析が必要である.以上の結果より,LRRK2の2019番目のグリシン残基がセリン残基となる変異をもつパーキンソン病の患者の神経幹細胞においては,加齢とともに核膜の崩壊が起こりその機能が低下することによりさまざまな症状がひき起こされている可能性が示唆された.
患者から万能細胞をつくりだすiPS技術は,疾患モデルの作製や病因の究明においても非常に有用であり,今回の解析では,in vitroにおいて新たな知見を得て,それを生体においても確認することができた.このようなiPS技術を用いたin vitroからin vivoへの解析法は,今後,ほかの疾患においても同様に行えることが予想され,原因の不明な多くの疾患においてその分子機構の解明されることが期待される.さらに,この研究において成功した遺伝子の修復法を用いることにより変異のない正常な細胞を作製することでき,これを患者自身にもどせば拒絶反応のない細胞移植治療が可能となることから,ほかの遺伝病の治療においても大きな期待がもたれる.今後は,これらの細胞を用いた新規の薬剤のスクリーニングや,遺伝子を修復した細胞を用いた移植治療などの応用研究を行い,一刻も早く多くの疾患の完治が可能となる治療法が確立することを願っている.
略歴:2005年 埼玉大学大学院理工学研究科 修了,2006年 埼玉医科大学 特任研究員,2009年 同 助教を経て,2010年より米国Salk Institute for Biological StudiesにてResearch Associate.
研究テーマ:ヒトの幹細胞における遺伝子の修復技術を用いた,遺伝性疾患の分子機構の解明および治療法の開発.
Juan Carlos Izpisua Belmonte
米国Salk Institute for Biological StudiesにてProfessor.
研究室URL:http://www.salk.edu/labs/belmonte/
© 2012 鈴木啓一郎・Juan Carlos Izpisua Belmonte Licensed under CC 表示 2.1 日本
(米国Salk Institute for Biological Studies,Gene Expression Laboratory)
email:鈴木啓一郎
DOI: 10.7875/first.author.2012.141
Progressive degeneration of human neural stem cells caused by pathogenic LRRK2.
Guang-Hui Liu, Jing Qu, Keiichiro Suzuki, Emmanuel Nivet, Mo Li, Nuria Montserrat, Fei Yi, Xiuling Xu, Sergio Ruiz, Weiqi Zhang, Ulrich Wagner, Audrey Kim, Bing Ren, Ying Li, April Goebl, Jessica Kim, Rupa Devi Soligalla, Ilir Dubova, James Thompson, John Yates III, Concepcion Rodriguez Esteban, Ignacio Sancho-Martinez, Juan Carlos Izpisua Belmonte
Nature, 491, 603-607 (2012)
要 約
核膜の崩壊は多くの遺伝性疾患の原因,あるいは,老化現象のひとつとして知られている.この研究では,加齢にともない発症率の高くなる神経変性疾患であるパーキンソン病における原因遺伝子のひとつLRRK2遺伝子について,もっとも高い頻度でみられる変異をもつ患者に由来する細胞を用い解析した.患者の皮膚細胞からiPS細胞を樹立して神経幹細胞に分化させ,老化を模倣する目的で培養皿において継代をくり返したところ,健常者から同様に分化させた神経幹細胞に比べ,核膜の変形やニューロンへの分化能の低下が有意に観察された.また,これらの神経幹細胞においてみられた表現型は,iPS細胞においてこのLRRK2遺伝子の変異を特異的に修復することにより消失し,逆に,同じ変異をヒトのES細胞に導入することにより再現できたことから,この変異が原因であることが確認された.さらに,この変異をもつパーキンソン病の患者の脳の組織を解析したところ,健常者に比べ核膜の変形が高頻度にみられた.以上の解析により,iPS技術を用いることでパーキンソン病における老化に依存した核膜の崩壊という新たな表現型を発見し,将来的な診断や治療の分子標的としての可能性を示すことができた.
はじめに
核膜は真核生物において核と細胞質とを隔てる,内膜と外膜の2層の脂質からなる構造体であり,内膜の内側には核の構造維持と転写の制御を行う線維状タンパク質であるラミンが存在する.ヒトではA型ラミンおよびC型ラミンをLMNA遺伝子が,B型ラミンであるラミンB1とラミンB2をLMNB1遺伝子とLMNB2遺伝子がそれぞれコードしており,ほかの膜タンパク質とともに核ラミナを形成している.核膜は細胞にとり非常に重要な役割をはたしており,核膜の崩壊はさまざまな遺伝性疾患や老化した細胞において認められている1-5).
この研究では,老化した細胞に観察される核膜の変性と,加齢にともない発症リスクの高まる神経変性疾患のひとつであるパーキンソン病との関係に注目した.パーキンソン病はアルツハイマー病についで世界で2番目に多い神経変性疾患で,神経伝達物質であるドーパミンを産生するニューロンの変性を主体とする進行性の疾患であり,さまざまな運動障害をひき起こす6).しかし,その病因や分子機構についていまだ不明な点が多く,根本的な治療法は皆無である.その要因のひとつとして,これまでヒトにおいてはニューロンを用いた研究が困難であることがあげられてきた.しかしながら,2012年にノーベル医学賞を受賞した山中伸弥らによるiPS細胞(induced pluripotent stem cell,人工多能性幹細胞)の開発により,疾患患者の皮膚細胞よりiPS細胞を樹立し,さらにそれをニューロンに分化させることで,疾患の分子機構の解明や創薬スクリーニングへ利用することが可能になった7).しかし実際には,遺伝的な背景による影響は大きく,たとえ親子に由来する細胞であっても別個体のあいだでの比較はむずかしく,厳密な比較対照のないことがヒトにおける解析のうえでのつぎなる課題となっていた.以前に,筆者らは,ヒト細胞を用いて相同組換えにより染色体において特定の標的遺伝子を自由に改変する技術を開発し8),この技術を用いて同一の遺伝的な背景をもつ遺伝子を修復した細胞を作製した.今回は,これらの技術を組み合わせることにより,パーキンソン病において老化に関連する疾患の分子機構の解明をめざし研究を行った(図1).
1.LRRK2変異タンパク質に結合するタンパク質の探索
加齢にともない症状の現われるパーキンソン病において,変異の割合のもっとも高い,LRRK2の2019番目のグリシン残基がセリン残基となる変異に注目した.この変異ではLRRK2遺伝子のキナーゼドメインに一塩基置換が生じ,LRRK2のもつリン酸化酵素活性が過剰に高くなっている.まず,このLRRK2変異タンパク質に結合する新規のタンパク質を探索した.HeLa細胞においてこのLRRK2変異タンパク質を過剰発現させプロテオーム解析を行った結果,既知の結合タンパク質にくわえ,新たに多くの核膜構成タンパク質の結合が認められた.また,このLRRK2変異タンパク質を過剰発現することにより核膜の変形が観察された.これらの結果から,2019番目のグリシン残基がセリン残基に変異したLRRK2と核膜とのつながりが示唆された.
2.LRRK2変異をもつiPS細胞の樹立と神経幹細胞の解析
ヒトのLRRK2の2019番目のグリシン残基がセリン残基となる変異をもつトランスジェニックマウスでは,成熟ののち神経の新生に異常をきたすことが報告されている9).そこで,このLRRK2変異をもつパーキンソン病患者の皮膚細胞に3つの転写因子Oct3/4,Sox2,Klf4(山中因子)を導入することによりiPS細胞を樹立した.つづいて,樹立したiPS細胞を神経幹細胞に分化させた.神経幹細胞は自己複製能をもつため継代をくり返すことができる.老化を模倣する目的で培養皿においてこの神経幹細胞の継代をくり返したところ,継代数が14をこえるとこのLRRK2変異をもつ神経幹細胞でのみ核膜の変形が観察され,継代が進むにつれその表現型は顕著となった.また,このLRRK2変異タンパク質を過剰発現させることにより,この変異をもたない神経幹細胞においても核膜に異常がみられた.さらに,免疫染色法により,調べた核膜構成タンパク質のうちラミンB1とラミンB2のB型ラミンのみ,変形した核膜において部分的に局在が欠失していることがわかった.免疫共沈降法により,神経幹細胞においてもB型ラミンとLRRK2変異タンパク質は複合体を形成することが確認され,継代を重ねたLRRK2変異をもつ神経幹細胞においてB型ラミンの過剰なリン酸化が観察された.以上の結果より,LRRK2の2019番目のグリシン残基がセリン残基となる変異をもつ神経幹細胞は,継代をくり返すことによりB型ラミンを過剰にリン酸化し,その核膜における局在が部分的に失われ核が変形してしまうことが示唆された.
一方,パーキンソン病の原因のひとつとされるミトコンドリアの異常10) は,継代を重ねたこのLRRK2変異をもつ神経幹細胞においてはみられなかった.また,パーキンソン病患者の皮膚から得た線維芽細胞,あるいは,パーキンソン病患者の皮膚から樹立されたiPS細胞においては,継代を重ねても核膜に異常はみられず,この表現型は神経幹細胞に特異的なものであることが示唆された.
継代を重ね核膜の変形したこのLRRK2変異をもつ神経幹細胞をよりくわしく解析したところ,プロモーター領域において老化したニューロンの指標のひとつとされるヒストンH3の4番目のリジン残基のトリメチル化11) に異常をきたしていることが全ゲノムレベルの解析により明らかになった.また,健常者に由来する神経幹細胞に比べ,クローン増殖力およびニューロンへの分化能が有意に低下していた.興味深いことに,タンパク質分解にかかわるプロテオソームの阻害剤をくわえると,このLRRK2変異をもつ神経幹細胞は継代数に依存することなくアポトーシスによる細胞死が増加した.
3.相同組換えを用いた遺伝的な背景の同一なiPS細胞の樹立と神経幹細胞の解析
これまでの解析の結果はLRRK2の2019番目のグリシン残基がセリン残基となる変異によることを証明するため,筆者らが以前に開発した,安全なアデノウイルスベクターによる高効率な遺伝子ターゲッティング技術8) を用いて,このLRRK2変異をもつiPS細胞において変異遺伝子の修復を行うことにより,遺伝的な背景の同一なLRRK2変異をもたないiPS細胞を作製した.このiPS細胞を神経幹細胞に分化させたところ,LRRK2変異をもつ神経幹細胞にみられた表現型は消失した.同じ技術を用いて,逆に,ヒトのES細胞(embryonic stem cell,胚性幹細胞)にLRRK2変異を導入したところ,このLRRK2変異をもつ神経幹細胞と同様の表現型がみられた.これらの結果から,パーキンソン病の患者に由来する神経幹細胞における核膜の変形など継代に依存的な表現型は,LRRK2の2019番目のグリシン残基がセリン残基となる変異が原因であることが強く示唆された.
4.LRRK2の阻害剤による抑制効果
LRRK2の2019番目のグリシン残基がセリン残基となる変異は,LRRK2のもつセリン/スレオニンリン酸化活性が過剰にはたらくことでパーキンソン病の原因となっていることが示唆されている10,12).実際に,このLRRK2変異をもつ神経幹細胞では継代に依存してさまざまな基質が過剰にリン酸化されており,これが核膜の変形など表現型の原因になっている可能性が考えられた.そこで,すでに知られているLRRK2によるリン酸化の阻害剤13,14) により処理したところ,継代を重ねたこのLRRK2変異をもつ神経幹細胞においてLRRK2の標的となる基質のリン酸化は減少し核膜の変形など表現型はレスキューされた.このことから,LRRK2の2019番目のグリシン残基がセリン残基となる変異による神経幹細胞でみられる表現型は可逆的であり,薬剤により治療が可能であるため将来的な創薬の標的となりうることが示唆された.
5.パーキンソン病の患者における脳組織の解析
これらin vitroにおいて得られた新しい知見が生体において生じているかどうか確認するため,パーキンソン病の患者と年齢がほぼ同じ健常者の脳組織のスライスを作製し,成人の脳でも神経幹細胞が存在する海馬歯状回において免疫染色法により核膜の形状を調べた.その結果,LRRK2の2019番目のグリシン残基がセリン残基となる変異をもつパーキンソン病の患者では,健常者に比べ核膜の変形が有意に多くみられた.興味深いことに,これ以外の変異をもつパーキンソン病の患者においても中程度に核膜の変形がみられた.このようなほかの変異によるパーキンソン病と核膜との関係については,今後,よりくわしい解析が必要である.以上の結果より,LRRK2の2019番目のグリシン残基がセリン残基となる変異をもつパーキンソン病の患者の神経幹細胞においては,加齢とともに核膜の崩壊が起こりその機能が低下することによりさまざまな症状がひき起こされている可能性が示唆された.
おわりに
患者から万能細胞をつくりだすiPS技術は,疾患モデルの作製や病因の究明においても非常に有用であり,今回の解析では,in vitroにおいて新たな知見を得て,それを生体においても確認することができた.このようなiPS技術を用いたin vitroからin vivoへの解析法は,今後,ほかの疾患においても同様に行えることが予想され,原因の不明な多くの疾患においてその分子機構の解明されることが期待される.さらに,この研究において成功した遺伝子の修復法を用いることにより変異のない正常な細胞を作製することでき,これを患者自身にもどせば拒絶反応のない細胞移植治療が可能となることから,ほかの遺伝病の治療においても大きな期待がもたれる.今後は,これらの細胞を用いた新規の薬剤のスクリーニングや,遺伝子を修復した細胞を用いた移植治療などの応用研究を行い,一刻も早く多くの疾患の完治が可能となる治療法が確立することを願っている.
文 献
- Worman, H. J., Ostlund, C. & Wang, Y.: Diseases of the nuclear envelope. Cold Spring Harb. Perspect. Biol., 2, a000760 (2010)[PubMed]
- Chang, K. H., Multani, P. S., Sun, K. H. et al.: Nuclear envelope dispersion triggered by deregulated Cdk5 precedes neuronal death. Mol. Biol. Cell, 22, 1452-1462 (2011)[PubMed]
- Tran, D., Chalhoub, A., Schooley, A. et al.: A mutation in VAPB that causes amyotrophic lateral sclerosis also causes a nuclear envelope defect. J. Cell Sci., 125, 2831-2836 (2012)[PubMed]
- Padiath, Q. S., Saigoh, K., Schiffmann, R. et al.: Lamin B1 duplications cause autosomal dominant leukodystrophy. Nat. Genet., 38, 1114-1123 (2006)[PubMed]
- Woulfe, J. M.: Abnormalities of the nucleus and nuclear inclusions in neurodegenerative disease: a work in progress. Neuropathol. Appl. Neurobiol., 33, 2-42 (2007)[PubMed]
- Jankovic, J.: Parkinson's disease: clinical features and diagnosis. J. Neurol. Neurosurg. Psychiatry, 79, 368-376 (2008)[PubMed]
- Takahashi, K., Tanabe, K., Ohnuki, M. et al.: Induction of pluripotent stem cells from adult human fibroblasts by defined factors. Cell, 131, 861-872 (2007)[PubMed]
- Suzuki, K., Mitsui, K., Aizawa, E. et al.: Highly efficient transient gene expression and gene targeting in primate embryonic stem cells with helper-dependent adenoviral vectors. Proc. Natl. Acad. Sci. USA, 105, 13781-13786 (2008)[PubMed]
- Winner, B., Melrose, H. L., Zhao, C. et al.: Adult neurogenesis and neurite outgrowth are impaired in LRRK2 G2019S mice. Neurobiol. Dis., 41, 706-716 (2011)[PubMed]
- Cookson, M. R.: The role of leucine-rich repeat kinase 2 (LRRK2) in Parkinson's disease. Nat. Rev. Neurosci., 11, 791-797 (2010)[PubMed]
- Cheung, I., Shulha, H. P., Jiang, Y. et al.: Developmental regulation and individual differences of neuronal H3K4me3 epigenomes in the prefrontal cortex. Proc. Natl. Acad. Sci. USA, 107, 8824-8829 (2010)[PubMed]
- Cookson, M. R. & Bandmann, O.: Parkinson's disease: insights from pathways. Hum. Mol. Genet., 19, R21-27 (2010)[PubMed]
- Deng, X., Dzamko, N., Prescott, A. et al.: Characterization of a selective inhibitor of the Parkinson's disease kinase LRRK2. Nat. Chem. Biol., 7, 203-205 (2011)[PubMed]
- Rudenko, I. N., Chia, R., Cookson, M. R.: Is inhibition of kinase activity the only therapeutic strategy for LRRK2-associated Parkinson's disease? BMC Med., 10, 20 (2012)[PubMed]
著者プロフィール
略歴:2005年 埼玉大学大学院理工学研究科 修了,2006年 埼玉医科大学 特任研究員,2009年 同 助教を経て,2010年より米国Salk Institute for Biological StudiesにてResearch Associate.
研究テーマ:ヒトの幹細胞における遺伝子の修復技術を用いた,遺伝性疾患の分子機構の解明および治療法の開発.
Juan Carlos Izpisua Belmonte
米国Salk Institute for Biological StudiesにてProfessor.
研究室URL:http://www.salk.edu/labs/belmonte/
© 2012 鈴木啓一郎・Juan Carlos Izpisua Belmonte Licensed under CC 表示 2.1 日本