サルマラリア原虫のゲノム配列の解読は三日熱マラリア原虫および関連するサルマラリア原虫族に対する理解を深めた
橘 真一郎・田邉和裄
(大阪大学微生物病研究所 マラリア学研究グループ)
email:橘 真一郎,田邉和裄
DOI: 10.7875/first.author.2012.107
Plasmodium cynomolgi genome sequences provide insight into Plasmodium vivax and the monkey malaria clade.
Shin-Ichiro Tachibana, Steven A. Sullivan, Satoru Kawai, Shota Nakamura, Hyunjae R. Kim, Naohisa Goto, Nobuko Arisue, Nirianne M. Q. Palacpac, Hajime Honma, Masanori Yagi, Takahiro Tougan, Yuko Katakai, Osamu Kaneko, Toshihiro Mita, Kiyoshi Kita, Yasuhiro Yasutomi, Patrick L. Sutton, Rimma Shakhbatyan, Toshihiro Horii, Teruo Yasunaga, John W. Barnwell, Ananias A. Escalante, Jane M. Carlton, Kazuyuki Tanabe
Nature Genetics, 44, 1051-1055 (2012)
アジアに生息する旧世界サルを宿主とするサルマラリア原虫Plasmodium cynomolgiは,ヒトのマラリアの主要な原因となる種である三日熱マラリア原虫と系統的にもっとも近縁な種で,この2種のマラリア原虫は多くの生物学的および遺伝学的な特徴を共有している.今回,筆者らは,3株のP. cynomolgiのゲノム塩基配列を解読し,ゲノムの全域にわたる1塩基多型,マイクロサテライト,コピー数多型を同定し,遺伝的多様性地図を作製した.さらに,三日熱マラリア原虫および別のサルマラリア原虫P. knowlesiとのゲノム比較解析を行い,これら3種のマラリア原虫のゲノムにおけるおもな違いは,多重遺伝子ファミリーにおけるコピー数の違いにあることを明らかにした.そこにはマラリア原虫の宿主特異性に関与する多重遺伝子ファミリーが含まれており,そのコピー数の種における違いが宿主域を決めている可能性が示唆された.
マラリアはAnopheles属のカ(図1a)により媒介され,宿主の体内に侵入したマラリア原虫が赤血球において増殖することにより高熱や貧血をひき起こす感染症である.ヒトにおいてマラリアの原因となる種は4種あり,そのうち,三日熱マラリア原虫Plasmodium vivaxは毎年約1億人の感染者をだし,アフリカ以外の地域においてマラリアの原因となる主要な種となっている.三日熱マラリア原虫は肝臓での休眠期をもつため数カ月から数年後に再発することがある.また,近年は薬剤耐性株が現われていることからその対策が重要となっている.三日熱マラリア原虫はアカゲザルやカニクイザルなどアジアに生息する旧世界サルを宿主とするサルマラリア原虫族と系統的に近く,数十万年前にサルからヒトへと宿主を換え,現在ではサルへの感染能を失っている1-3).
三日熱マラリア原虫はその医学的な重要性にもかかわらず,血液において存在量の小さい網状赤血球(未熟な赤血球)に寄生するため培養が非常に困難であること,および,感染実験動物(サル)が限定されていることから,研究はあまり進んでおらず“放置されたマラリア原虫”と称されてきた4).2008年,三日熱マラリア原虫とともに,人獣共通感染性であるサルマラリア原虫P. knowlesiのゲノム塩基配列が解読されたが5,6),P. knowlesiは三日熱マラリア原虫とは系統的にやや遠縁で,ゲノムの構造および表現型も異なるため,三日熱マラリア原虫のモデル種としては利用できない.一方,サルマラリア原虫の一種P. cynomolgi(図1b)は三日熱マラリア原虫にもっとも近縁であり,ヒトへの感染能および肝臓での休眠期をもつ点を含め,三日熱マラリア原虫と共通する多くの生物学的および遺伝学的な特徴をもち,三日熱マラリア原虫の特徴を解明するための重要なモデル種と位置づけられている.そこで今回,筆者らは,P. cynomolgiのゲノム塩基配列を解読することにより,三日熱マラリア原虫の研究モデル種としてゲノム情報リソースの充実を図るとともに,三日熱マラリア原虫およびP. knowlesiとのゲノム比較解析を行い,三日熱マラリア原虫およびサルマラリア原虫族のゲノムの特徴を解析した.
P. cynomolgiのゲノム塩基配列の解読はB株(マレーシア産)をもとに進めた.Roche社のGS FLX(Titanium)およびIllumina社のGAIIにより得たシングルリード約4.3 Gbと,Sanger法により得たペアエンドリード約6.8 Mbを利用したアセンブリー,および,PCR法による断片配列のあいだの連関情報の取得により,染色体の数と同じ14本のスーパーコンティグおよび1649本の断片配列,計26.2 Mbを得た.
P. cynomolgiのゲノムはGC含量,染色体の構造,セントロメアの位置など,ゲノムの特徴の多くが三日熱マラリア原虫およびP. knowlesiのゲノムと類似しており,遺伝子の位置も14本の染色体の全域にわたり高度に保存されていた.P. cynomolgiのゲノムからは全部で5722個の遺伝子が同定されたが,そのうち,染色体における位置が判明した遺伝子につき3種のマラリア原虫のあいだで比較したところ,9割の遺伝子について染色体における位置が共通して保存されていた.残る1割の遺伝子の多くは,遺伝子重複によりコピー数の増加した多重遺伝子ファミリーにより構成されていた.つまり,3種のマラリア原虫のあいだのゲノムの主要な違いは,多重遺伝子ファミリーに起こった遺伝子重複イベントの違いに起因すると考えられた.現在,同定されている3種のマラリア原虫のもつ多重遺伝子ファミリーは26種あり,それぞれのコピー数を比較すると,P. cynomolgiと三日熱マラリア原虫とのあいだではコピー数は非常に類似していることが明らかになった.このようなP. cynomolgiと三日熱マラリア原虫とのゲノムの類似性は系統関係から予測されたことではあったが,三日熱マラリア原虫のモデル種としてのP. cynomolgiの有用性を明確に示すものであった.
マラリア原虫が宿主の赤血球へ侵入するためには,原虫のもつリガンドと赤血球の表面にある受容体との特異的な結合が必須である.今回のゲノム比較解析において非常に重要な発見は,サルマラリア原虫族の赤血球への侵入の際にリガンドとして機能するタンパク質をコードする多重遺伝子ファミリー,DBP(Duffy binding protein)遺伝子ファミリー,および,RBP/NBP(reticulocyte binding protein/normocyte binding protein)遺伝子ファミリーのコピー数において,種のあいだで違いのあったことであった.つまり,この違いが宿主域や侵入する赤血球の種類を決めている可能性が浮上した.
DBPはヒトとサルの赤血球の表面にあるケモカイン受容体のひとつ,Duffy抗原受容体に特異的に結合するタンパク質として知られている.今回のゲノム比較解析により,ヒトにしか寄生できない三日熱マラリア原虫のもつDBP遺伝子ファミリーの遺伝子コピー数は1個であるのに対し,サルとヒトに寄生できる2種のサルマラリア原虫のもつDBP遺伝子ファミリーは複数個の遺伝子コピーをもつことが明らかになった.この発見はDBP遺伝子ファミリーの遺伝子コピーの数により宿主域の決まる可能性を示唆していた.さらにこの可能性は,サルにしか寄生できないほか2種のサルマラリア原虫P. fieldiおよびP. simiovaleのもつDBP遺伝子ファミリーの遺伝子コピー数も1個であったことからも支持された.しかしながら,最終的な結論はそれぞれのマラリア原虫に由来するDBPとヒトおよびサルの赤血球との結合試験の結果を待つ必要がある.
RBP/NBPは赤血球の表面の標的受容体はまだ同定されていないが,赤血球への侵入に関与することが示唆されている7).RBP/NBP遺伝子ファミリーは系統的に3つのグループ,RBP/NBP-1,RBP/NBP-2およびRBP/NBP-3に分かれ5),これら3つのグループへの遺伝子の分化は種の分化よりもまえに起こっている.解析の結果,P. cynomolgiは3つのグループすべてのRBP/NBP遺伝子ファミリーをもっていたが,三日熱マラリア原虫ではRBP/NBP-3,P. knowlesiではRBP/NBP-1が偽遺伝子化により失われていた.このことから,RBP/NBP遺伝子ファミリーの3つのグループへの遺伝子重複および消失というイベントは3種のマラリア原虫の種分化のあとに起こり,そのイベントの違いにより,侵入する赤血球の種類を含む,種に特異的な侵入機構を獲得したものと考えられた.
すべてのマラリア原虫にはくり返し配列に富むpir(Plasmodium-interspersed repeat)遺伝子ファミリーが存在し,コードするタンパク質は感染した赤血球の表面に現われ,宿主による免疫応答を回避する役割を担うと推定されている.この遺伝子ファミリーは,三日熱マラリア原虫ではvir(vivax-interspersed repeat)遺伝子ファミリーとよばれ319個の遺伝子が含まれる.同様に,P. knowlesiでは70個の遺伝子からなるkir(knowlesi-interspersed repeat)遺伝子ファミリーが存在する.今回,P. cynomolgiのゲノムから265個の遺伝子からなるcyir(cynomolgi-interspersed repeat)遺伝子ファミリーを同定することができた.そのうち254個のcyir遺伝子ファミリーはvir遺伝子ファミリーと相同な配列をもち,かつ,三日熱マラリア原虫と同様に染色体の両端にあるサブテロメア領域に位置していた.興味深いことに,残り11個のcyir遺伝子ファミリーは,vir遺伝子ファミリーとは構造の異なるkir遺伝子ファミリーと高い相同性を示した.さらに,それらcyir遺伝子ファミリーは染色体のなかよりに位置し,宿主の免疫回避にかかわるタンパク質であるCD99の遺伝子と相同な配列をもつ点でもkir遺伝子ファミリーと共通していた.また,抗原変異に関与しP. knowlesiに特異的でかつ242個と最大の多重遺伝子ファミリーを構成するSICAvar(schizont infected cell agglutination variant)遺伝子ファミリーのホモログが,P. cynomolgiから2個,三日熱マラリア原虫から1個みつかった.これらの発見は,pir遺伝子ファミリーおよびSICAvar遺伝子ファミリーが3種のマラリア原虫の祖先種においてすでに存在し,種分化ののち,種ごとに遺伝子重複および消失というイベントをへて,種に特異的な多重遺伝子ファミリーを形成したことを示唆していた.
肝臓での休眠期をもつマラリア原虫は,サルマラリア原虫族のうちごく一部に限定される.三日熱マラリア原虫が肝臓休眠期をもち,マラリアの治療において重要な意味をもつことから,その分子基盤の解明は重要な課題のひとつとなっているがまったく不明である.P. cynomolgiも肝臓休眠期をもつことから,その制御に関与する候補遺伝子の探索を行った.今回,解読したP. cynomolgiを含む,ゲノムの解読されている7種のマラリア原虫のゲノム配列情報を利用し,2つの異なる観点から探索を行った.1つ目は,機能が未知で,かつ,肝臓休眠期をもつマラリア原虫にのみ存在するという観点で,絞り込みの結果,3つの推定遺伝子を同定した.2つ目は,ほかの生物種において休眠の制御に関与することが示されている遺伝子のホモログで,三日熱マラリア原虫とP. cynomolgiにおいて肝臓休眠期の直前の発育期(スポロゾイト期)に発現する遺伝子であるという観点で,機能が既知の9つの遺伝子を同定した.この9つの遺伝子には細胞周期の移行に関与するキナーゼをコードする遺伝子が含まれていた.これは,肝臓休眠期はスポロゾイト期に特異的に発現したタンパク質のリン酸化により制御されている可能性を示唆した.候補遺伝子の同定は,肝臓休眠期の分子基盤の解明にむけた実験的なアプローチの幕開けを示すものである.
P. cynomolgiのゲノム情報リソースの拡充を目的に,B株のほか,Berok株(マレーシア産)およびCambodian株(カンボジア産)についてもゲノム解読を行い,1塩基多型(single nucleotide polymorphism:SNP),マイクロサテライト,および,コピー数多型(copy number variation:CNV)を同定し,ゲノムの全域にわたる遺伝的多様性地図を作製した.これら3株のあいだのゲノム比較解析により,約18万箇所のSNP(151 bpあたり1個)を同定した.これは熱帯熱マラリア原虫P. falciparumにみられるSNPの示す多様性のレベル8,9) と類似していた.B株とBerok株のあいだのCNV解析では,1570箇所のCNV(17 kbあたり1個)を同定した.このCNV解析では,さきに述べたRBP/NBP遺伝子ファミリーのグループのひとつRBP/NBP-1において,Berok株のもつrbp遺伝子の数がB株よりも1つ多く重複していることが明らかになった.これは,単一のマラリア原虫種の株のあいだでrbp遺伝子にCNVの存在することを示した最初の例であった.ついで,B株とBerok株とのあいだで,P. cynomolgiにおいてはじめての遺伝子マーカーとなる182箇所の遺伝子間マイクロサテライト多型を同定した.これらはP. cynomolgiの遺伝的な多様性および集団の構造を研究するためのツールとして,今後,活用されるであろう.
P. cynomolgiのゲノム塩基配列の解読は,これまで放置されてきた三日熱マラリア原虫の研究モデル系を構築するうえで必要不可欠なものである.今回の三日熱マラリア原虫を含むサルマラリア原虫族のゲノム比較解析は,マラリア原虫の種特異性に関する生物学的および遺伝学的な理解を深め,三日熱マラリアの撲滅へとつながる新たな予防法および治療法の開発を推進させるであろう.
略歴:2004年 大阪市立大学大学院理学研究科 修了,中央農業総合研究センター 契約研究員,大阪大学微生物病研究所 特任研究員を経て,2011年より京都大学生命科学系キャリアパス形成ユニット 特定研究員.
研究テーマ:嗅覚感受性の可塑的な制御を担う神経の機構.
抱負:現在は,ショウジョウバエをモデルに嗅覚馴化のしくみを研究している.どのような研究テーマであっても,社会に還元し貢献できる成果をあげることを目標にしている.
田邉 和裄(Kazuyuki Tanabe)
大阪大学微生物病研究所 招へい教授.
研究室URL:http://www.biken.osaka-u.ac.jp/lab/protozool/index.html
© 2012 橘 真一郎・田邉和裄 Licensed under CC 表示 2.1 日本
(大阪大学微生物病研究所 マラリア学研究グループ)
email:橘 真一郎,田邉和裄
DOI: 10.7875/first.author.2012.107
Plasmodium cynomolgi genome sequences provide insight into Plasmodium vivax and the monkey malaria clade.
Shin-Ichiro Tachibana, Steven A. Sullivan, Satoru Kawai, Shota Nakamura, Hyunjae R. Kim, Naohisa Goto, Nobuko Arisue, Nirianne M. Q. Palacpac, Hajime Honma, Masanori Yagi, Takahiro Tougan, Yuko Katakai, Osamu Kaneko, Toshihiro Mita, Kiyoshi Kita, Yasuhiro Yasutomi, Patrick L. Sutton, Rimma Shakhbatyan, Toshihiro Horii, Teruo Yasunaga, John W. Barnwell, Ananias A. Escalante, Jane M. Carlton, Kazuyuki Tanabe
Nature Genetics, 44, 1051-1055 (2012)
要 約
アジアに生息する旧世界サルを宿主とするサルマラリア原虫Plasmodium cynomolgiは,ヒトのマラリアの主要な原因となる種である三日熱マラリア原虫と系統的にもっとも近縁な種で,この2種のマラリア原虫は多くの生物学的および遺伝学的な特徴を共有している.今回,筆者らは,3株のP. cynomolgiのゲノム塩基配列を解読し,ゲノムの全域にわたる1塩基多型,マイクロサテライト,コピー数多型を同定し,遺伝的多様性地図を作製した.さらに,三日熱マラリア原虫および別のサルマラリア原虫P. knowlesiとのゲノム比較解析を行い,これら3種のマラリア原虫のゲノムにおけるおもな違いは,多重遺伝子ファミリーにおけるコピー数の違いにあることを明らかにした.そこにはマラリア原虫の宿主特異性に関与する多重遺伝子ファミリーが含まれており,そのコピー数の種における違いが宿主域を決めている可能性が示唆された.
はじめに
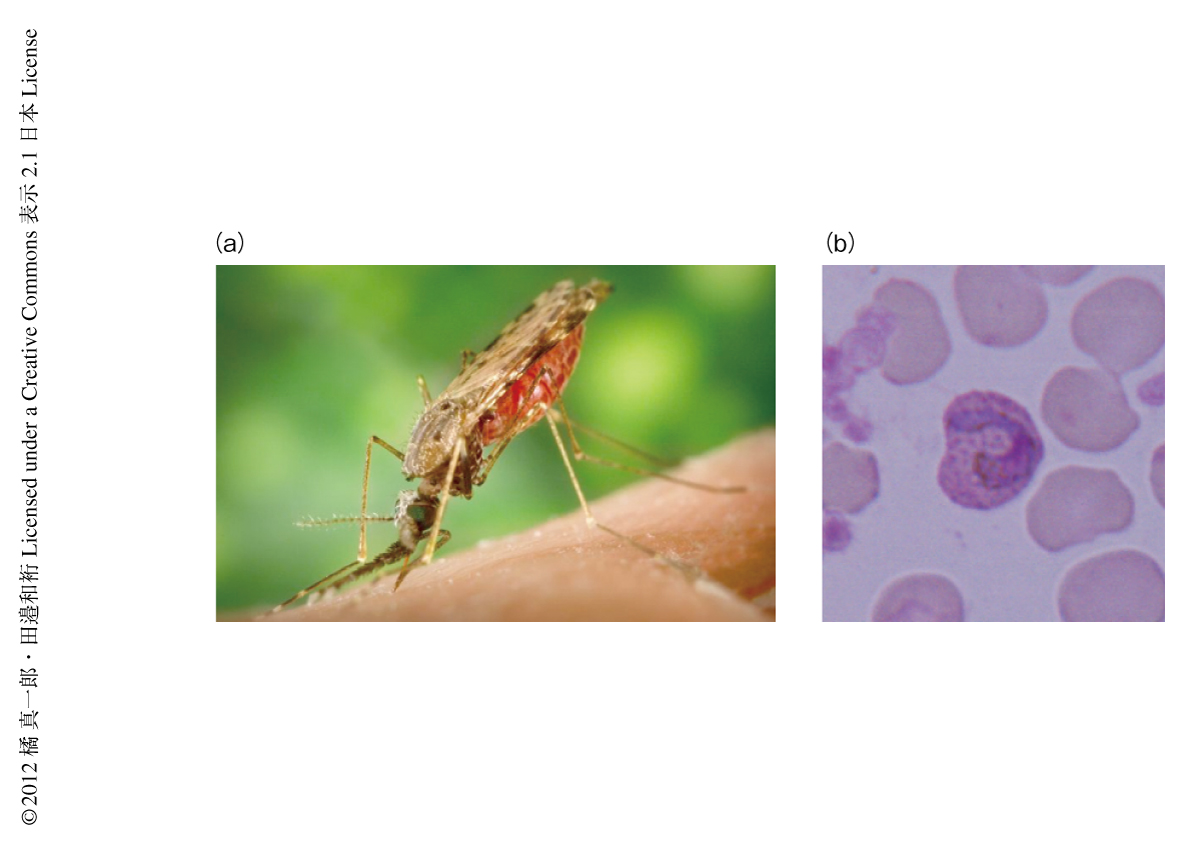
マラリアはAnopheles属のカ(図1a)により媒介され,宿主の体内に侵入したマラリア原虫が赤血球において増殖することにより高熱や貧血をひき起こす感染症である.ヒトにおいてマラリアの原因となる種は4種あり,そのうち,三日熱マラリア原虫Plasmodium vivaxは毎年約1億人の感染者をだし,アフリカ以外の地域においてマラリアの原因となる主要な種となっている.三日熱マラリア原虫は肝臓での休眠期をもつため数カ月から数年後に再発することがある.また,近年は薬剤耐性株が現われていることからその対策が重要となっている.三日熱マラリア原虫はアカゲザルやカニクイザルなどアジアに生息する旧世界サルを宿主とするサルマラリア原虫族と系統的に近く,数十万年前にサルからヒトへと宿主を換え,現在ではサルへの感染能を失っている1-3).
三日熱マラリア原虫はその医学的な重要性にもかかわらず,血液において存在量の小さい網状赤血球(未熟な赤血球)に寄生するため培養が非常に困難であること,および,感染実験動物(サル)が限定されていることから,研究はあまり進んでおらず“放置されたマラリア原虫”と称されてきた4).2008年,三日熱マラリア原虫とともに,人獣共通感染性であるサルマラリア原虫P. knowlesiのゲノム塩基配列が解読されたが5,6),P. knowlesiは三日熱マラリア原虫とは系統的にやや遠縁で,ゲノムの構造および表現型も異なるため,三日熱マラリア原虫のモデル種としては利用できない.一方,サルマラリア原虫の一種P. cynomolgi(図1b)は三日熱マラリア原虫にもっとも近縁であり,ヒトへの感染能および肝臓での休眠期をもつ点を含め,三日熱マラリア原虫と共通する多くの生物学的および遺伝学的な特徴をもち,三日熱マラリア原虫の特徴を解明するための重要なモデル種と位置づけられている.そこで今回,筆者らは,P. cynomolgiのゲノム塩基配列を解読することにより,三日熱マラリア原虫の研究モデル種としてゲノム情報リソースの充実を図るとともに,三日熱マラリア原虫およびP. knowlesiとのゲノム比較解析を行い,三日熱マラリア原虫およびサルマラリア原虫族のゲノムの特徴を解析した.
1.サルマラリア原虫P. cynomolgiのゲノムの特徴
P. cynomolgiのゲノム塩基配列の解読はB株(マレーシア産)をもとに進めた.Roche社のGS FLX(Titanium)およびIllumina社のGAIIにより得たシングルリード約4.3 Gbと,Sanger法により得たペアエンドリード約6.8 Mbを利用したアセンブリー,および,PCR法による断片配列のあいだの連関情報の取得により,染色体の数と同じ14本のスーパーコンティグおよび1649本の断片配列,計26.2 Mbを得た.
P. cynomolgiのゲノムはGC含量,染色体の構造,セントロメアの位置など,ゲノムの特徴の多くが三日熱マラリア原虫およびP. knowlesiのゲノムと類似しており,遺伝子の位置も14本の染色体の全域にわたり高度に保存されていた.P. cynomolgiのゲノムからは全部で5722個の遺伝子が同定されたが,そのうち,染色体における位置が判明した遺伝子につき3種のマラリア原虫のあいだで比較したところ,9割の遺伝子について染色体における位置が共通して保存されていた.残る1割の遺伝子の多くは,遺伝子重複によりコピー数の増加した多重遺伝子ファミリーにより構成されていた.つまり,3種のマラリア原虫のあいだのゲノムの主要な違いは,多重遺伝子ファミリーに起こった遺伝子重複イベントの違いに起因すると考えられた.現在,同定されている3種のマラリア原虫のもつ多重遺伝子ファミリーは26種あり,それぞれのコピー数を比較すると,P. cynomolgiと三日熱マラリア原虫とのあいだではコピー数は非常に類似していることが明らかになった.このようなP. cynomolgiと三日熱マラリア原虫とのゲノムの類似性は系統関係から予測されたことではあったが,三日熱マラリア原虫のモデル種としてのP. cynomolgiの有用性を明確に示すものであった.
2.宿主への侵入に関与する遺伝子ファミリーにおいてみつかった種に特異的な遺伝子欠失
マラリア原虫が宿主の赤血球へ侵入するためには,原虫のもつリガンドと赤血球の表面にある受容体との特異的な結合が必須である.今回のゲノム比較解析において非常に重要な発見は,サルマラリア原虫族の赤血球への侵入の際にリガンドとして機能するタンパク質をコードする多重遺伝子ファミリー,DBP(Duffy binding protein)遺伝子ファミリー,および,RBP/NBP(reticulocyte binding protein/normocyte binding protein)遺伝子ファミリーのコピー数において,種のあいだで違いのあったことであった.つまり,この違いが宿主域や侵入する赤血球の種類を決めている可能性が浮上した.
DBPはヒトとサルの赤血球の表面にあるケモカイン受容体のひとつ,Duffy抗原受容体に特異的に結合するタンパク質として知られている.今回のゲノム比較解析により,ヒトにしか寄生できない三日熱マラリア原虫のもつDBP遺伝子ファミリーの遺伝子コピー数は1個であるのに対し,サルとヒトに寄生できる2種のサルマラリア原虫のもつDBP遺伝子ファミリーは複数個の遺伝子コピーをもつことが明らかになった.この発見はDBP遺伝子ファミリーの遺伝子コピーの数により宿主域の決まる可能性を示唆していた.さらにこの可能性は,サルにしか寄生できないほか2種のサルマラリア原虫P. fieldiおよびP. simiovaleのもつDBP遺伝子ファミリーの遺伝子コピー数も1個であったことからも支持された.しかしながら,最終的な結論はそれぞれのマラリア原虫に由来するDBPとヒトおよびサルの赤血球との結合試験の結果を待つ必要がある.
RBP/NBPは赤血球の表面の標的受容体はまだ同定されていないが,赤血球への侵入に関与することが示唆されている7).RBP/NBP遺伝子ファミリーは系統的に3つのグループ,RBP/NBP-1,RBP/NBP-2およびRBP/NBP-3に分かれ5),これら3つのグループへの遺伝子の分化は種の分化よりもまえに起こっている.解析の結果,P. cynomolgiは3つのグループすべてのRBP/NBP遺伝子ファミリーをもっていたが,三日熱マラリア原虫ではRBP/NBP-3,P. knowlesiではRBP/NBP-1が偽遺伝子化により失われていた.このことから,RBP/NBP遺伝子ファミリーの3つのグループへの遺伝子重複および消失というイベントは3種のマラリア原虫の種分化のあとに起こり,そのイベントの違いにより,侵入する赤血球の種類を含む,種に特異的な侵入機構を獲得したものと考えられた.
3.3種のマラリア原虫がもつ最大の多重遺伝子ファミリーは種に特異的に分化している
すべてのマラリア原虫にはくり返し配列に富むpir(Plasmodium-interspersed repeat)遺伝子ファミリーが存在し,コードするタンパク質は感染した赤血球の表面に現われ,宿主による免疫応答を回避する役割を担うと推定されている.この遺伝子ファミリーは,三日熱マラリア原虫ではvir(vivax-interspersed repeat)遺伝子ファミリーとよばれ319個の遺伝子が含まれる.同様に,P. knowlesiでは70個の遺伝子からなるkir(knowlesi-interspersed repeat)遺伝子ファミリーが存在する.今回,P. cynomolgiのゲノムから265個の遺伝子からなるcyir(cynomolgi-interspersed repeat)遺伝子ファミリーを同定することができた.そのうち254個のcyir遺伝子ファミリーはvir遺伝子ファミリーと相同な配列をもち,かつ,三日熱マラリア原虫と同様に染色体の両端にあるサブテロメア領域に位置していた.興味深いことに,残り11個のcyir遺伝子ファミリーは,vir遺伝子ファミリーとは構造の異なるkir遺伝子ファミリーと高い相同性を示した.さらに,それらcyir遺伝子ファミリーは染色体のなかよりに位置し,宿主の免疫回避にかかわるタンパク質であるCD99の遺伝子と相同な配列をもつ点でもkir遺伝子ファミリーと共通していた.また,抗原変異に関与しP. knowlesiに特異的でかつ242個と最大の多重遺伝子ファミリーを構成するSICAvar(schizont infected cell agglutination variant)遺伝子ファミリーのホモログが,P. cynomolgiから2個,三日熱マラリア原虫から1個みつかった.これらの発見は,pir遺伝子ファミリーおよびSICAvar遺伝子ファミリーが3種のマラリア原虫の祖先種においてすでに存在し,種分化ののち,種ごとに遺伝子重複および消失というイベントをへて,種に特異的な多重遺伝子ファミリーを形成したことを示唆していた.
4.肝臓での休眠期に関与する候補遺伝子の同定
肝臓での休眠期をもつマラリア原虫は,サルマラリア原虫族のうちごく一部に限定される.三日熱マラリア原虫が肝臓休眠期をもち,マラリアの治療において重要な意味をもつことから,その分子基盤の解明は重要な課題のひとつとなっているがまったく不明である.P. cynomolgiも肝臓休眠期をもつことから,その制御に関与する候補遺伝子の探索を行った.今回,解読したP. cynomolgiを含む,ゲノムの解読されている7種のマラリア原虫のゲノム配列情報を利用し,2つの異なる観点から探索を行った.1つ目は,機能が未知で,かつ,肝臓休眠期をもつマラリア原虫にのみ存在するという観点で,絞り込みの結果,3つの推定遺伝子を同定した.2つ目は,ほかの生物種において休眠の制御に関与することが示されている遺伝子のホモログで,三日熱マラリア原虫とP. cynomolgiにおいて肝臓休眠期の直前の発育期(スポロゾイト期)に発現する遺伝子であるという観点で,機能が既知の9つの遺伝子を同定した.この9つの遺伝子には細胞周期の移行に関与するキナーゼをコードする遺伝子が含まれていた.これは,肝臓休眠期はスポロゾイト期に特異的に発現したタンパク質のリン酸化により制御されている可能性を示唆した.候補遺伝子の同定は,肝臓休眠期の分子基盤の解明にむけた実験的なアプローチの幕開けを示すものである.
5.遺伝的多様性地図の作製
P. cynomolgiのゲノム情報リソースの拡充を目的に,B株のほか,Berok株(マレーシア産)およびCambodian株(カンボジア産)についてもゲノム解読を行い,1塩基多型(single nucleotide polymorphism:SNP),マイクロサテライト,および,コピー数多型(copy number variation:CNV)を同定し,ゲノムの全域にわたる遺伝的多様性地図を作製した.これら3株のあいだのゲノム比較解析により,約18万箇所のSNP(151 bpあたり1個)を同定した.これは熱帯熱マラリア原虫P. falciparumにみられるSNPの示す多様性のレベル8,9) と類似していた.B株とBerok株のあいだのCNV解析では,1570箇所のCNV(17 kbあたり1個)を同定した.このCNV解析では,さきに述べたRBP/NBP遺伝子ファミリーのグループのひとつRBP/NBP-1において,Berok株のもつrbp遺伝子の数がB株よりも1つ多く重複していることが明らかになった.これは,単一のマラリア原虫種の株のあいだでrbp遺伝子にCNVの存在することを示した最初の例であった.ついで,B株とBerok株とのあいだで,P. cynomolgiにおいてはじめての遺伝子マーカーとなる182箇所の遺伝子間マイクロサテライト多型を同定した.これらはP. cynomolgiの遺伝的な多様性および集団の構造を研究するためのツールとして,今後,活用されるであろう.
おわりに
P. cynomolgiのゲノム塩基配列の解読は,これまで放置されてきた三日熱マラリア原虫の研究モデル系を構築するうえで必要不可欠なものである.今回の三日熱マラリア原虫を含むサルマラリア原虫族のゲノム比較解析は,マラリア原虫の種特異性に関する生物学的および遺伝学的な理解を深め,三日熱マラリアの撲滅へとつながる新たな予防法および治療法の開発を推進させるであろう.
文 献
- Cornejo, O. E. & Escalante, A. A.: The origin and age of Plasmodium vivax. Trends Parasitol., 22, 558-563 (2006)[PubMed]
- Escalante, A. A., Cornejo, O. E., Freeland, D. E. et al.: A monkey’s tale: the origin of Plasmodium vivax as a human malaria parasite. Proc. Natl. Acad. Sci. USA, 102, 1980-1985 (2005)[PubMed]
- Mu, J., Joy, D. A., Duan, J. et al.: Host switch leads to emergence of Plasmodium vivax malaria in humans. Mol. Biol. Evol., 22, 1686-1693 (2005)[PubMed]
- Carlton, J. M., Sina, B. J. & Adams, J. H.: Why is Plasmodium vivax a neglected tropical disease? PLoS Negl. Trop. Dis., 5, e1160 (2011)[PubMed]
- Carlton, J. M., Adams, J. H., Silva, J. C. et al.: Comparative genomics of the neglected human malaria parasite Plasmodium vivax. Nature, 455, 757-763 (2008)[PubMed]
- Pain, A., Bohme, U., Berry, A. E. et al.: The genome of the simian and human malaria parasite Plasmodium knowlesi. Nature, 455, 799-803 (2008)[PubMed]
- Galinski, M. R., Medina, C. C., Ingravallo, P. et al.: A reticulocyte-binding protein complex of Plasmodium vivax merozoites. Cell, 69, 1213-1226 (1992)[PubMed]
- Mu, J., Awadalla, P., Duan, J. et al.: Genome-wide variation and identification of vaccine targets in the Plasmodium falciparum genome. Nat. Genet., 39, 126-130 (2007)[PubMed]
- Volkman, S. K., Sabeti, P. C., DeCaprio, D. et al.: A genome-wide map of diversity in Plasmodium falciparum. Nat. Genet., 39, 113-119 (2007)[PubMed]
著者プロフィール
略歴:2004年 大阪市立大学大学院理学研究科 修了,中央農業総合研究センター 契約研究員,大阪大学微生物病研究所 特任研究員を経て,2011年より京都大学生命科学系キャリアパス形成ユニット 特定研究員.
研究テーマ:嗅覚感受性の可塑的な制御を担う神経の機構.
抱負:現在は,ショウジョウバエをモデルに嗅覚馴化のしくみを研究している.どのような研究テーマであっても,社会に還元し貢献できる成果をあげることを目標にしている.
田邉 和裄(Kazuyuki Tanabe)
大阪大学微生物病研究所 招へい教授.
研究室URL:http://www.biken.osaka-u.ac.jp/lab/protozool/index.html
© 2012 橘 真一郎・田邉和裄 Licensed under CC 表示 2.1 日本