細胞の創傷治癒においてプロテアソームによるタンパク質分解により細胞極性のダイナミックな切替えが起こる
河野恵子・David Pellman
(米国Dana-Farber Cancer Institute,Department of Pediatric Oncology)
email:河野恵子
DOI: 10.7875/first.author.2012.103
Proteasomal degradation resolves competition between cell polarization and cellular wound healing.
Keiko Kono, Yasushi Saeki, Satoshi Yoshida, Keiji Tanaka, David Pellman
Cell, 150, 151-164 (2012)
細胞膜における局所的な損傷を修復する細胞の創傷治癒の機構は進化的に保存されている.細胞の創傷治癒におけるひとつの側面は,細胞骨格および極性輸送を損傷部位にむけ再構築することである.近年,細胞創傷治癒に関与するタンパク質は精力的に同定されつつあるが,それらはまだ一貫した反応として統合されていない.筆者らは,出芽酵母をモデルとし,レーザーにより局所的な損傷をあたえる新たな実験系を用いて,娘細胞に局在していた極性制御タンパク質が脱局在し,やがて,損傷部位に蓄積することを見い出した.この局在の変化にはプロテインキナーゼCに依存的なタンパク質分解が必要であった.この分子機構によりアクチン線維の重合にはたらくタンパク質であるBni1,および,極性輸送を制御するエクソシスト複合体の構成タンパク質Sec3が分解された.この分解により娘細胞における細胞極性と損傷部位における細胞極性との競合が解消され,安定した修復が保証されるものと思われた.
創傷治癒(wound-healing)ときくと,大部分の研究者は組織レベルでの創傷治癒,すなわち,スクラッチによりできた傷が細胞遊走により閉じられるプロセスを想起するのではないだろうか.筆者らが取り組んだ現象は,それよりプリミティブな“1細胞レベルでの創傷治癒”である.
実験室の細胞培養環境においてはあまり問題にならないが,細胞が研究室の外で増殖する場合には,外界との境界である細胞膜や細胞壁は機械的な刺激にさらされ,しばしば傷つくことになる.細胞はそのような傷を修復する分子機構をもっている.傷のまわりにアクチンやミオシン,微小管やRho型GTPaseなどがリング状にあつまり,そのリングが収縮することにより細胞質分裂とよく似たしくみで細胞の表面に空いた穴は閉じられる1).これは,細胞が傷ついたときのみならず多様な生物学的プロセスにおいて起こる現象であり,受精も一種の細胞創傷治癒であるといえよう.細胞創傷治癒の欠損はさまざまな疾病の原因となる.一例をあげれば,細胞膜の損傷修復に必要なジスフェルリンに遺伝的な欠損があると筋ジストロフィー症を発症し2),心臓の拍動にともなって日常的に生じる細胞膜の損傷を修復できず徐々に心臓が弱りやがて死にいたる.近年,細胞膜あるいは細胞壁の修復機構に関与するタンパク質は精力的に同定されつつあるものの,それらの相互関係や損傷部位にリクルートされるしくみの詳細は不明であった.その一因は,遺伝学的な解析のむずかしい生物がモデルとして用いられてきたためであろう.そこで筆者らは,この分野に遺伝学的な手法をもちこむことを考えた.
強力な遺伝学的ツールである出芽酵母(Saccharomyces cerevisiae)においては,細胞創傷治癒に類似した分子機構が報告されていた.出芽酵母を温和な熱ショック,界面活性剤,pHの変化,浸透圧の変化,酸化ストレスなど細胞壁や細胞膜に損傷をあたえるような条件におくと,30分以内にアクチン細胞骨格は極性を失って一時的に増殖を停止するが,2~3時間のうちに損傷を修復して増殖を再開する3).この現象には,cell wall integrity経路とよばれる,Rho型GTPaseであるRho1やプロテインキナーゼCであるPkc1を含むシグナル伝達経路が必要であり,現象もその制御タンパク質も高等真核生物の細胞創傷治癒に類似している.しかし,このストレス応答反応が高等真核生物のように細胞の表面の小さな穴を局所的に修復できるかどうかは未知であった.
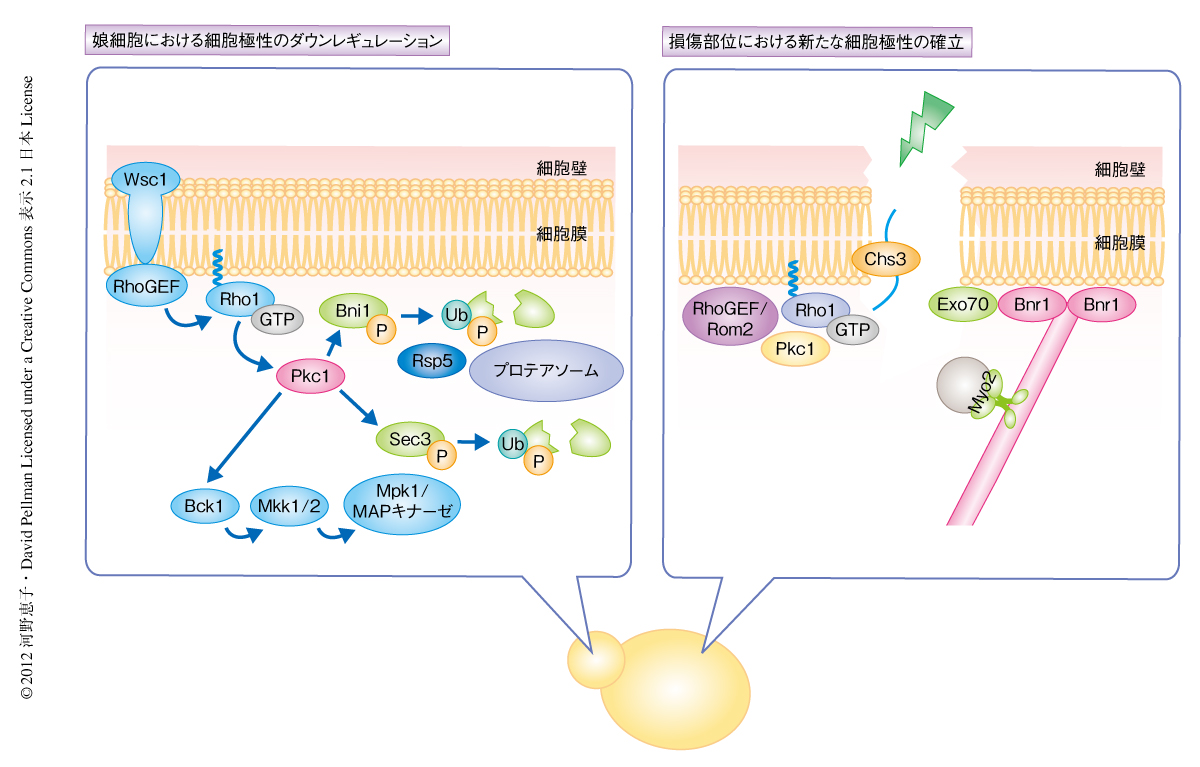
そこで筆者らは,出芽酵母の表面の微細な領域にレーザーにより穴を開けるという実験系を確立し,さまざまな極性制御タンパク質と蛍光タンパク質GFPとの融合タンパク質が損傷部位にリクルートされるかどうかを生細胞イメージング法により観察した(図1).すると,通常の増殖条件では娘細胞に局在していたPkc1やV型ミオシンをはじめとする多数の極性制御タンパク質は,レーザー照射ののちすぐに脱局在し,やがて,損傷部位に蓄積した.損傷部位では新たな細胞壁が合成された.つまり,出芽酵母にもほかの真核生物と同様に,細胞の表面の微細な領域の損傷を修復する分子機構が存在していた.さらに,出芽酵母における細胞創傷治癒では,娘細胞における細胞極性のダウンレギュレーション,損傷部位における新たな細胞極性の確立,というダイナミックな細胞極性の切替えの起こっていることが明らかになった.
娘細胞において細胞極性のダウンレギュレーションの起こる分子機構を検討した.細胞極性がダウンレギュレーションされるためには,出芽酵母において極性決定の鍵となるアクチン細胞骨格の制御タンパク質がダウンレギュレーションされる必要がある.実際に,細胞の表面に損傷をあたえる複数の条件において,アクチン線維の重合にはたらくタンパク質フォーミンのひとつBni1 4) がタンパク質レベルにおいてすみやかに減少することが見い出された.さらに,この減少の主要な要因はタンパク質分解であり,それにはcell wall integrity経路を構成するRho1やPkc1は必要だが,Pkc1の下流のMAPキナーゼカスケードは必要ではなかった.
細胞におけるすみやかで選択的な分解はプロテアソームにより行われることが多い.Bni1も例外ではなく,その分解にはプロテアソームが必要であった.Bni1に直接に結合しこれをユビキチン化するユビキチンリガーゼを同定したいと考え,さまざまな文献を調べたところ,ストレス応答経路やcell wall integrity経路に関係するユビキチンリガーゼとしてRsp5がうかびあがってきた.そこで,このRsp5の関与を検討したところ,確かにBni1の分解にはRsp5の機能が必要であった.
ここまで,Bni1の分解に必要なタンパク質がいくつか同定されたので,Bni1において,その分解に十分なアミノ酸配列を調べた.ドメインの欠損により検討した結果,Bni1のN末端側642残基が分解に十分であることが明らかになった.このN末端側642残基はRsp5の機能が低下した細胞ではリン酸化されていたが,Pkc1の機能が低下した細胞ではリン酸化されていなかった.質量分析により,Bni1のもつ複数のプロテインキナーゼCによるリン酸化コンセンサス部位が確かにリン酸化されていることが確認されたので,Bni1はPkc1の基質であることが示唆された.Bni1のN末端側642アミノ酸残基とRsp5の基質認識ドメイン5) との結合について検討したところ,Pkc1に依存してリン酸化されたBni1の断片のみRsp5の基質認識ドメインとの結合が検出された.Rsp5の基質認識ドメインはPYモチーフとよばれるプロリン残基とチロシン残基を含む配列を認識する.Bni1のN末端側642残基のもつこのPYモチーフに変異を導入すると,Rsp5の基質認識ドメインとの結合は失われ,細胞の表面に損傷をあたえたときのBni1の分解も抑制された.さらに,in vitroにおいて,Bni1のN末端側642残基はRsp5によりユビキチン化されることが確認された.以上を考えあわせると,Bni1はPkc1によりリン酸化されてから,ユビキチンリガーゼRsp5によりユビキチン化をうけ,プロテアソームにより分解されると考えられた.
つづいて,Bni1分解の重要性を検討した.N末端側の一部(87~343アミノ酸残基)を欠失したBni1は分解されにくくなり,細胞の表面に損傷をあたえたときのアクチンの脱局在の効率は低下した.そのような細胞においてレーザーにより細胞の表面に損傷をあたえる実験を行ったところ,細胞極性はほんの一瞬だけ,娘細胞から損傷部位へと切り替わったものの,すぐにもとにもどってしまった.つまり,娘細胞への細胞極性と損傷部位への細胞極性とは競合しており,Bni1が分解されると競合が解消して安定的な細胞創傷治癒が可能になると考えられた.
ここで,論理に不整合性が生じる.Pkc1やRsp5の機能が低下した細胞では損傷により細胞死がひき起こされたのに対し,Bni1を分解されにくくした細胞では損傷をあたえても細胞増殖がほんの少し遅くなるだけで致死にはならなかった.つまり,Bni1を安定化しても細胞創傷治癒がまったく起こらないわけではないらしい.このことは,ここに並行した経路が存在する,つまり,Pkc1の下流で分解される極性制御タンパク質はBni1以外にも存在すると考えると説明がつく.そこで,Bni1と同じくRho型GTPaseと関係の深い極性制御タンパク質をいくつか選び出して検討したところ,極性輸送を制御するエクソシスト複合体の構成タンパク質であるSec3も,Pkc1に依存して分解されることが明らかになった.Bni1により重合が促進されるアクチン細胞骨格は極性輸送の線路ともいうべき構造体であることを考えると,Bni1とSec3,この2つの分解が遺伝学的に並行な事象であるというのは納得がいった.さらに解析を進めたところ,Sec3の分解に必要な領域はBni1の場合と同じくN末端側であった.そこで,このN末端側のドメインを取り除いてBni1とSec3の両方を分解されにくくし,レーザーにより細胞の表面に損傷をあたえたところ,細胞極性の切替えは完全に遮断され(つまり,極性制御タンパク質は娘細胞の先端に局在しつづけ),細胞創傷治癒を行うことができず細胞は死にいたった.つまり,Bni1とSec3の分解は細胞極性の切替えとそののちの細胞創傷治癒に必須であった(図2).興味深いことに,Bni1もSec3も,Pkc1と同じくRho1の標的である.したがって,この制御をいい換えれば,Pkc1はそれ自体と同じくRho1の標的であるBni1とSec3の分解を誘導することにより,Rho1からPkc1自体へのシグナルを強めているのかもしれない.
もうひとつ興味深いのは,娘細胞における細胞極性のダウンレギュレーション,損傷部位における新たな細胞極性の確立,という2つのステップにおいて,類似する機能をもつタンパク質の交替が起こるようにみえたことである.具体的にいうと,フォーミンであるBni1は娘細胞における細胞極性のダウンレギュレーションにより分解され,もうひとつのフォーミンBnr1は損傷部位へとリクルートされた.さらに,エクソシスト複合体の構成タンパク質であるSec3は娘細胞における細胞極性のダウンレギュレーションにより分解され,同じくエクソシスト複合体の構成タンパク質であるExo70は損傷部位へとリクルートされた.つまり,娘細胞における細胞極性と損傷部位における細胞極性は,異なるタンパク質により制御されていた.なぜ,このような交替が必要なのか? Sec3をもたないエクソシスト複合体は完全なエクソシスト複合体とどのような違いがあるのか? 細胞周期との関係は? そもそも,細胞創傷治癒のトリガーとなるのはどの分子なのか? さらには,細胞創傷治癒ののち,どのように通常の増殖状態にもどるのか? これらの問いはいまだ手つかずのまま残されている.
筆者らは,出芽酵母は真核生物に保存された細胞創傷治癒の分子機構を理解するためのパワフルな遺伝学的なツールになりうることを示した.もちろん,生物ごと細胞ごとに分子機構の詳細は異なるに違いないが,原始的な単細胞真核生物における創傷治癒を理解することは現象の根本的な概念をうきぼりにし,高等真核生物の細胞創傷治癒を理解する一助になると信じている.
略歴:2005年 東京大学大学院新領域創成科学研究科 修了,同年 米国Dana-Farber Cancer Instituteポスドクを経て,2012年より名古屋市立大学大学院医学研究科 講師.
研究テーマ:細胞内外のシグナルに応答した細胞極性の制御.
David Pellman
米国Dana-Farber Cancer InstituteにてProfessor.
研究室URL:http://research.dfci.harvard.edu/pellmanlab/
© 2012 河野恵子・David Pellman Licensed under CC 表示 2.1 日本
(米国Dana-Farber Cancer Institute,Department of Pediatric Oncology)
email:河野恵子
DOI: 10.7875/first.author.2012.103
Proteasomal degradation resolves competition between cell polarization and cellular wound healing.
Keiko Kono, Yasushi Saeki, Satoshi Yoshida, Keiji Tanaka, David Pellman
Cell, 150, 151-164 (2012)
要 約
細胞膜における局所的な損傷を修復する細胞の創傷治癒の機構は進化的に保存されている.細胞の創傷治癒におけるひとつの側面は,細胞骨格および極性輸送を損傷部位にむけ再構築することである.近年,細胞創傷治癒に関与するタンパク質は精力的に同定されつつあるが,それらはまだ一貫した反応として統合されていない.筆者らは,出芽酵母をモデルとし,レーザーにより局所的な損傷をあたえる新たな実験系を用いて,娘細胞に局在していた極性制御タンパク質が脱局在し,やがて,損傷部位に蓄積することを見い出した.この局在の変化にはプロテインキナーゼCに依存的なタンパク質分解が必要であった.この分子機構によりアクチン線維の重合にはたらくタンパク質であるBni1,および,極性輸送を制御するエクソシスト複合体の構成タンパク質Sec3が分解された.この分解により娘細胞における細胞極性と損傷部位における細胞極性との競合が解消され,安定した修復が保証されるものと思われた.
はじめに
創傷治癒(wound-healing)ときくと,大部分の研究者は組織レベルでの創傷治癒,すなわち,スクラッチによりできた傷が細胞遊走により閉じられるプロセスを想起するのではないだろうか.筆者らが取り組んだ現象は,それよりプリミティブな“1細胞レベルでの創傷治癒”である.
実験室の細胞培養環境においてはあまり問題にならないが,細胞が研究室の外で増殖する場合には,外界との境界である細胞膜や細胞壁は機械的な刺激にさらされ,しばしば傷つくことになる.細胞はそのような傷を修復する分子機構をもっている.傷のまわりにアクチンやミオシン,微小管やRho型GTPaseなどがリング状にあつまり,そのリングが収縮することにより細胞質分裂とよく似たしくみで細胞の表面に空いた穴は閉じられる1).これは,細胞が傷ついたときのみならず多様な生物学的プロセスにおいて起こる現象であり,受精も一種の細胞創傷治癒であるといえよう.細胞創傷治癒の欠損はさまざまな疾病の原因となる.一例をあげれば,細胞膜の損傷修復に必要なジスフェルリンに遺伝的な欠損があると筋ジストロフィー症を発症し2),心臓の拍動にともなって日常的に生じる細胞膜の損傷を修復できず徐々に心臓が弱りやがて死にいたる.近年,細胞膜あるいは細胞壁の修復機構に関与するタンパク質は精力的に同定されつつあるものの,それらの相互関係や損傷部位にリクルートされるしくみの詳細は不明であった.その一因は,遺伝学的な解析のむずかしい生物がモデルとして用いられてきたためであろう.そこで筆者らは,この分野に遺伝学的な手法をもちこむことを考えた.
1.出芽酵母は細胞創傷治癒に類似した分子機構をもつ
強力な遺伝学的ツールである出芽酵母(Saccharomyces cerevisiae)においては,細胞創傷治癒に類似した分子機構が報告されていた.出芽酵母を温和な熱ショック,界面活性剤,pHの変化,浸透圧の変化,酸化ストレスなど細胞壁や細胞膜に損傷をあたえるような条件におくと,30分以内にアクチン細胞骨格は極性を失って一時的に増殖を停止するが,2~3時間のうちに損傷を修復して増殖を再開する3).この現象には,cell wall integrity経路とよばれる,Rho型GTPaseであるRho1やプロテインキナーゼCであるPkc1を含むシグナル伝達経路が必要であり,現象もその制御タンパク質も高等真核生物の細胞創傷治癒に類似している.しかし,このストレス応答反応が高等真核生物のように細胞の表面の小さな穴を局所的に修復できるかどうかは未知であった.
そこで筆者らは,出芽酵母の表面の微細な領域にレーザーにより穴を開けるという実験系を確立し,さまざまな極性制御タンパク質と蛍光タンパク質GFPとの融合タンパク質が損傷部位にリクルートされるかどうかを生細胞イメージング法により観察した(図1).すると,通常の増殖条件では娘細胞に局在していたPkc1やV型ミオシンをはじめとする多数の極性制御タンパク質は,レーザー照射ののちすぐに脱局在し,やがて,損傷部位に蓄積した.損傷部位では新たな細胞壁が合成された.つまり,出芽酵母にもほかの真核生物と同様に,細胞の表面の微細な領域の損傷を修復する分子機構が存在していた.さらに,出芽酵母における細胞創傷治癒では,娘細胞における細胞極性のダウンレギュレーション,損傷部位における新たな細胞極性の確立,というダイナミックな細胞極性の切替えの起こっていることが明らかになった.
2.細胞の損傷によりフォーミンBni1はプロテアソームに依存して分解される
娘細胞において細胞極性のダウンレギュレーションの起こる分子機構を検討した.細胞極性がダウンレギュレーションされるためには,出芽酵母において極性決定の鍵となるアクチン細胞骨格の制御タンパク質がダウンレギュレーションされる必要がある.実際に,細胞の表面に損傷をあたえる複数の条件において,アクチン線維の重合にはたらくタンパク質フォーミンのひとつBni1 4) がタンパク質レベルにおいてすみやかに減少することが見い出された.さらに,この減少の主要な要因はタンパク質分解であり,それにはcell wall integrity経路を構成するRho1やPkc1は必要だが,Pkc1の下流のMAPキナーゼカスケードは必要ではなかった.
細胞におけるすみやかで選択的な分解はプロテアソームにより行われることが多い.Bni1も例外ではなく,その分解にはプロテアソームが必要であった.Bni1に直接に結合しこれをユビキチン化するユビキチンリガーゼを同定したいと考え,さまざまな文献を調べたところ,ストレス応答経路やcell wall integrity経路に関係するユビキチンリガーゼとしてRsp5がうかびあがってきた.そこで,このRsp5の関与を検討したところ,確かにBni1の分解にはRsp5の機能が必要であった.
ここまで,Bni1の分解に必要なタンパク質がいくつか同定されたので,Bni1において,その分解に十分なアミノ酸配列を調べた.ドメインの欠損により検討した結果,Bni1のN末端側642残基が分解に十分であることが明らかになった.このN末端側642残基はRsp5の機能が低下した細胞ではリン酸化されていたが,Pkc1の機能が低下した細胞ではリン酸化されていなかった.質量分析により,Bni1のもつ複数のプロテインキナーゼCによるリン酸化コンセンサス部位が確かにリン酸化されていることが確認されたので,Bni1はPkc1の基質であることが示唆された.Bni1のN末端側642アミノ酸残基とRsp5の基質認識ドメイン5) との結合について検討したところ,Pkc1に依存してリン酸化されたBni1の断片のみRsp5の基質認識ドメインとの結合が検出された.Rsp5の基質認識ドメインはPYモチーフとよばれるプロリン残基とチロシン残基を含む配列を認識する.Bni1のN末端側642残基のもつこのPYモチーフに変異を導入すると,Rsp5の基質認識ドメインとの結合は失われ,細胞の表面に損傷をあたえたときのBni1の分解も抑制された.さらに,in vitroにおいて,Bni1のN末端側642残基はRsp5によりユビキチン化されることが確認された.以上を考えあわせると,Bni1はPkc1によりリン酸化されてから,ユビキチンリガーゼRsp5によりユビキチン化をうけ,プロテアソームにより分解されると考えられた.
3.細胞の損傷により誘導されるBni1分解の意義
つづいて,Bni1分解の重要性を検討した.N末端側の一部(87~343アミノ酸残基)を欠失したBni1は分解されにくくなり,細胞の表面に損傷をあたえたときのアクチンの脱局在の効率は低下した.そのような細胞においてレーザーにより細胞の表面に損傷をあたえる実験を行ったところ,細胞極性はほんの一瞬だけ,娘細胞から損傷部位へと切り替わったものの,すぐにもとにもどってしまった.つまり,娘細胞への細胞極性と損傷部位への細胞極性とは競合しており,Bni1が分解されると競合が解消して安定的な細胞創傷治癒が可能になると考えられた.
4.エクソシスト複合体の構成タンパク質Sec3も細胞の損傷ののち分解される
ここで,論理に不整合性が生じる.Pkc1やRsp5の機能が低下した細胞では損傷により細胞死がひき起こされたのに対し,Bni1を分解されにくくした細胞では損傷をあたえても細胞増殖がほんの少し遅くなるだけで致死にはならなかった.つまり,Bni1を安定化しても細胞創傷治癒がまったく起こらないわけではないらしい.このことは,ここに並行した経路が存在する,つまり,Pkc1の下流で分解される極性制御タンパク質はBni1以外にも存在すると考えると説明がつく.そこで,Bni1と同じくRho型GTPaseと関係の深い極性制御タンパク質をいくつか選び出して検討したところ,極性輸送を制御するエクソシスト複合体の構成タンパク質であるSec3も,Pkc1に依存して分解されることが明らかになった.Bni1により重合が促進されるアクチン細胞骨格は極性輸送の線路ともいうべき構造体であることを考えると,Bni1とSec3,この2つの分解が遺伝学的に並行な事象であるというのは納得がいった.さらに解析を進めたところ,Sec3の分解に必要な領域はBni1の場合と同じくN末端側であった.そこで,このN末端側のドメインを取り除いてBni1とSec3の両方を分解されにくくし,レーザーにより細胞の表面に損傷をあたえたところ,細胞極性の切替えは完全に遮断され(つまり,極性制御タンパク質は娘細胞の先端に局在しつづけ),細胞創傷治癒を行うことができず細胞は死にいたった.つまり,Bni1とSec3の分解は細胞極性の切替えとそののちの細胞創傷治癒に必須であった(図2).興味深いことに,Bni1もSec3も,Pkc1と同じくRho1の標的である.したがって,この制御をいい換えれば,Pkc1はそれ自体と同じくRho1の標的であるBni1とSec3の分解を誘導することにより,Rho1からPkc1自体へのシグナルを強めているのかもしれない.
もうひとつ興味深いのは,娘細胞における細胞極性のダウンレギュレーション,損傷部位における新たな細胞極性の確立,という2つのステップにおいて,類似する機能をもつタンパク質の交替が起こるようにみえたことである.具体的にいうと,フォーミンであるBni1は娘細胞における細胞極性のダウンレギュレーションにより分解され,もうひとつのフォーミンBnr1は損傷部位へとリクルートされた.さらに,エクソシスト複合体の構成タンパク質であるSec3は娘細胞における細胞極性のダウンレギュレーションにより分解され,同じくエクソシスト複合体の構成タンパク質であるExo70は損傷部位へとリクルートされた.つまり,娘細胞における細胞極性と損傷部位における細胞極性は,異なるタンパク質により制御されていた.なぜ,このような交替が必要なのか? Sec3をもたないエクソシスト複合体は完全なエクソシスト複合体とどのような違いがあるのか? 細胞周期との関係は? そもそも,細胞創傷治癒のトリガーとなるのはどの分子なのか? さらには,細胞創傷治癒ののち,どのように通常の増殖状態にもどるのか? これらの問いはいまだ手つかずのまま残されている.
おわりに
筆者らは,出芽酵母は真核生物に保存された細胞創傷治癒の分子機構を理解するためのパワフルな遺伝学的なツールになりうることを示した.もちろん,生物ごと細胞ごとに分子機構の詳細は異なるに違いないが,原始的な単細胞真核生物における創傷治癒を理解することは現象の根本的な概念をうきぼりにし,高等真核生物の細胞創傷治癒を理解する一助になると信じている.
文 献
- Sonnemann, K. J. & Bement, W. M.: Wound repair: toward understanding and integration of single-cell and multicellular wound responses. Annu. Rev. Cell Dev. Biol., 27, 237-263 (2011)[PubMed]
- Bashir, R., Britton, S., Strachan, T. et al.: A gene related to Caenorhabditis elegans spermatogenesis factor fer-1 is mutated in limb-girdle muscular dystrophy type 2B. Nat. Genet., 20, 37-42 (1998)[PubMed]
- Levin, D. E.: Regulation of cell wall biogenesis in Saccharomyces cerevisiae: the cell wall integrity signaling pathway. Genetics, 189, 1145-1175 (2011)[PubMed]
- Goode, B. L. & Eck, M. J.: Mechanism and function of formins in the control of actin assembly. Annu. Rev. Biochem., 76, 593-627 (2007)[PubMed]
- Wang, G., Yang, J. & Huibregtse, J. M.: Functional domains of the Rsp5 ubiquitin-protein ligase. Mol. Cell. Biol., 19, 342-352 (1999)[PubMed]
著者プロフィール
略歴:2005年 東京大学大学院新領域創成科学研究科 修了,同年 米国Dana-Farber Cancer Instituteポスドクを経て,2012年より名古屋市立大学大学院医学研究科 講師.
研究テーマ:細胞内外のシグナルに応答した細胞極性の制御.
David Pellman
米国Dana-Farber Cancer InstituteにてProfessor.
研究室URL:http://research.dfci.harvard.edu/pellmanlab/
© 2012 河野恵子・David Pellman Licensed under CC 表示 2.1 日本