NMDA受容体におけるMg2+ブロックはCREBに依存性の長期記憶に関連する遺伝子の発現誘導に必須である
宮下知之・齊藤 実
(東京都医学総合研究所 学習記憶プロジェクト)
email:齊藤 実
DOI: 10.7875/first.author.2012.079
Mg2+ block of Drosophila NMDA receptors is required for long-term memory formation and CREB-dependent gene expression.
Tomoyuki Miyashita, Yoshiaki Oda, Junjiro Horiuchi, Jerry C. P. Yin, Takako Morimoto, Minoru Saitoe
Neuron, 74, 887-898 (2012)
NMDA受容体はMg2+ブロックという機構をもち,これにより,シナプス後細胞は興奮していないときにはNMDA受容体を介したCa2+の流入が抑制されている.これまで,NMDA受容体は連合学習の成立や長期記憶の形成に必要であることが示されてきたが,Mg2+ブロックがこれらにおいてどのような役割をはたしているかは不明であった.筆者らは,Mg2+ブロックを欠損した変異NMDA受容体を発現するトランスジェニックショウジョウバエを作製し,Mg2+ブロックは連合学習の成立には不要だが,長期記憶の形成には必須であることを示す結果を得た.このトランスジェニックショウジョウバエにおいては長期記憶学習に応じ転写因子CREBに依存して上昇する,長期記憶あるいは長期増強に関連する遺伝子の発現が顕著に抑制されていた.興味深いことに,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエの脳においては抑制型CREBの発現が顕著に増加していた.抑制型CREBの発現量と長期記憶の形成阻害とには顕著な正の相関があり,このトランスジェニックショウジョウバエでみられた長期記憶の形成阻害の一因は抑制型CREBの発現上昇にあることが示唆された.こうした結果から,Mg2+ブロックの生理的な役割は学習を行っていない定常状態においてNMDA受容体を介したCa2+の流入を阻止して抑制型CREBの発現を抑制することであり,これにより,長期記憶学習のときにCREBに依存した遺伝子発現は可能となることが示唆された.
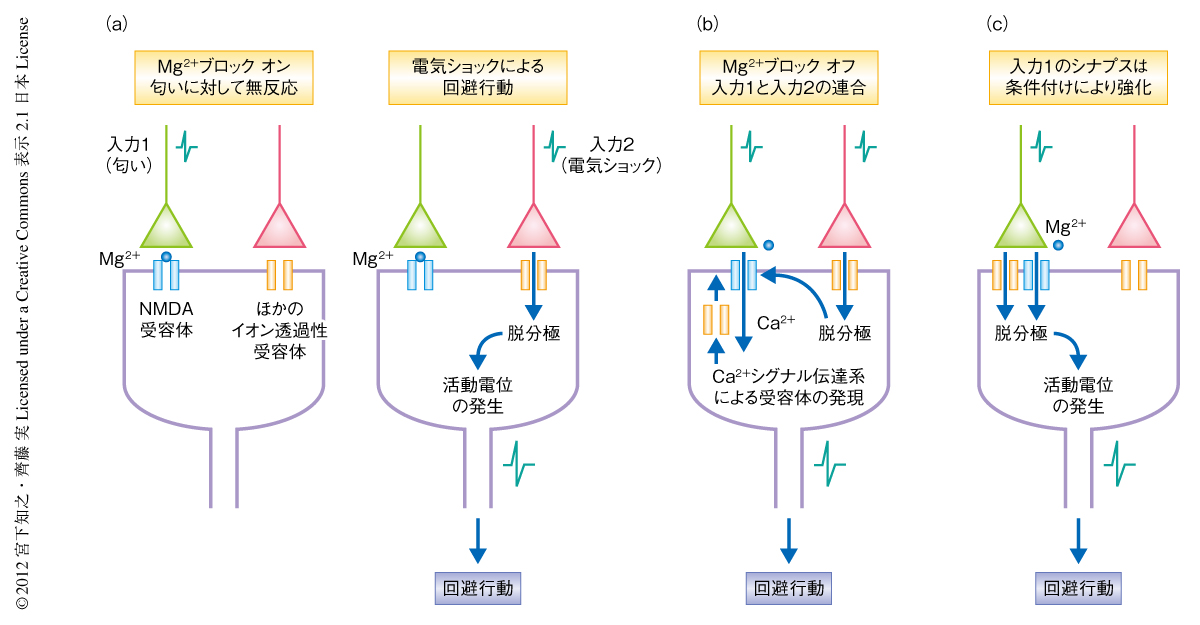
イオン透過型グルタミン酸受容体のひとつNMDA受容体は高いCa2+透過性をもち,細胞におけるシグナル伝達系の起点として重要な役割をはたしている.シナプス後細胞の興奮していないときにはNMDA受容体のイオン通過孔はMg2+によりふさがれていて1,2),グルタミン酸が結合してもCa2+は流入できない(図1).しかし,ほかのイオン透過型受容体の活性化などによりシナプス後細胞が脱分極の状態になるとこのMg2+は外れ,このとき,NMDA受容体にグルタミン酸が結合するとCa2+はシナプス後細胞に流入する.このように,NMDA受容体はMg2+ブロックを介してシナプス前細胞の活動とシナプス後細胞の活動の同期性と非同期性を判別できるため,連合学習において重要な役割を担うと考えられてきた(図1).
ショウジョウバエにおいてNMDA受容体は連合学習の成立と長期記憶の形成に必要である3).しかし,こうした過程にMg2+ブロックはどのように関与しているのか? なぜ非同期性のCa2+流入を抑制する必要があるのか? など,Mg2+ブロックの生理的な役割は不明であった.
NMDA受容体はNR1サブユニットとNR2サブユニットからなるヘテロサブユニット複合体であり,Mg2+ブロックはそれぞれサブユニットの第2膜貫通領域のいわゆる“Mg2+ブロック部位”にあるアスパラギン残基に依存している4,5).このアスパラギン残基をグルタミン残基に置換するとMg2+ブロックは消失する4,6).
ショウジョウバエにおいて,NR1サブユニットのMg2+ブロック部位にあるアスパラギン残基をグルタミン残基に置換した変異体を神経系において発現するトランスジェニックショウジョウバエを作製した.このトランスジェニックショウジョウバエにおいて発現するNMDA受容体の電気生理学的な性質を調べたところ,Mg2+ブロックの顕著な欠損が観察された.哺乳類においてはNR1サブユニットのMg2+ブロック部位に変異を導入するとMg2+ブロックが消失するだけでなくCa2+透過性も減少する.しかし興味深いことに,このトランスジェニックショウジョウバエの発現する変異NMDA受容体においてはMg2+ブロックの消失に相関したCa2+透過性の顕著な減少は観察されなかった.
この結果から,作製されたトランスジェニックショウジョウバエはMg2+ブロックを欠損した変異NMDA受容体を発現していることがわかった.そこで,このトランスジェニックショウジョウバエを用いMg2+ブロックの生理的な役割を,匂い条件付け連合学習課題により調べた.Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエは,NMDA受容体のNR1サブユニットの発現を抑制した変異ショウジョウバエとは異なり,連合学習と短期記憶は正常だった.しかし,間隔を空けて行うくり返し学習による長期記憶学習により形成される長期記憶は,同様に阻害されていた.
Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいては内因性のNMDA受容体NR1サブユニットが残存しているため正常な連合学習が成立した可能性があった.しかし,NMDA受容体NR1サブユニット変異ショウジョウバエにおける連合学習は,Mg2+ブロックを欠失したNMDA受容体NR1サブユニットの発現により回復したことから,連合学習の成立にはMg2+ブロックは関与していないことが示唆された.
従来,Mg2+ブロックは連合学習の成立に必須であり,Mg2+ブロックによる連合性の入力と非連合性の入力との識別がなければ匂い条件付けにおいて特定の匂い刺激に対する連合学習は成立せず,あらゆる匂いに対し記憶の般化(generalization)が起こるものと想像されていた.しかし,調べた範囲において記憶の般化はみられなかった.
長期記憶の形成には長期記憶学習に応じた遺伝子発現が必要である.そこで,stau遺伝子,homer遺伝子,activin遺伝子といった長期記憶あるいは後期の長期増強の形成に必要な遺伝子の発現を長期記憶学習ののち調べたところ,野生型ショウジョウバエでみられるこれら遺伝子の発現上昇は,NMDA受容体NR1サブユニット変異ショウジョウバエのみならず,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいても顕著に抑制されていた.
長期記憶に関連する多くの遺伝子の発現には転写因子CREBの活性が重要な役割をはたしている7).stau遺伝子,homer遺伝子,activin遺伝子の長期記憶学習ののちの発現上昇もCREBに依存性であることがわかった.以上の結果から,Mg2+ブロックは長期記憶学習に応じCREBに依存して,長期記憶に関連する遺伝子が発現誘導されるために必要な機構であることがわかった.
転写因子CREBには転写活性をもつ活性型ともたない抑制型とがあり,学習を行っていない定常状態において抑制型CREBの発現が上昇すると,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエと同様に,長期記憶の形成が特異的に抑制される7).そこで,抑制型CREBの発現を調べたところ,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいては対照となる系統に比べ4倍近くも発現が上昇していた.この抑制型CREBの発現上昇がMg2+ブロックの消失によるものかどうかを調べるため,野生型ショウジョウバエの脳をMg2+の非存在において培養したところやはり抑制型CREBの発現が上昇し,この発現上昇はNMDA受容体の阻害剤により抑制された.
Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいて発現の上昇した抑制型CREBは長期記憶の形成を抑制するに十分なのか,抑制型CREBの発現量と長期記憶の形成阻害との相関を定量的に解析したところ正の相関が認められ,抑制型CREBの4倍近くの発現上昇より長期記憶の形成を顕著に阻害しうることが示された.以上の結果から,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいて学習を行っていない定常状態ではNMDA受容体を介したCa2+流入の抑制の不全が起こり,その結果,抑制型CREBの発現が上昇し長期記憶の形成が阻害されることが示唆された.
Mg2+ブロックはNMDA受容体のHebb型一致検出器(coincidence detector)としての機能をもたらす機構であり,シナプス後細胞における長期増強の誘発や連合学習におけるシナプスの機序を説明するのにきわめて都合のよい性質であると考えられてきた.しかし,今回の結果は,Mg2+ブロックは連合学習の成立ではなく,むしろ,長期記憶を成立させるために必要であることを強く示唆した.
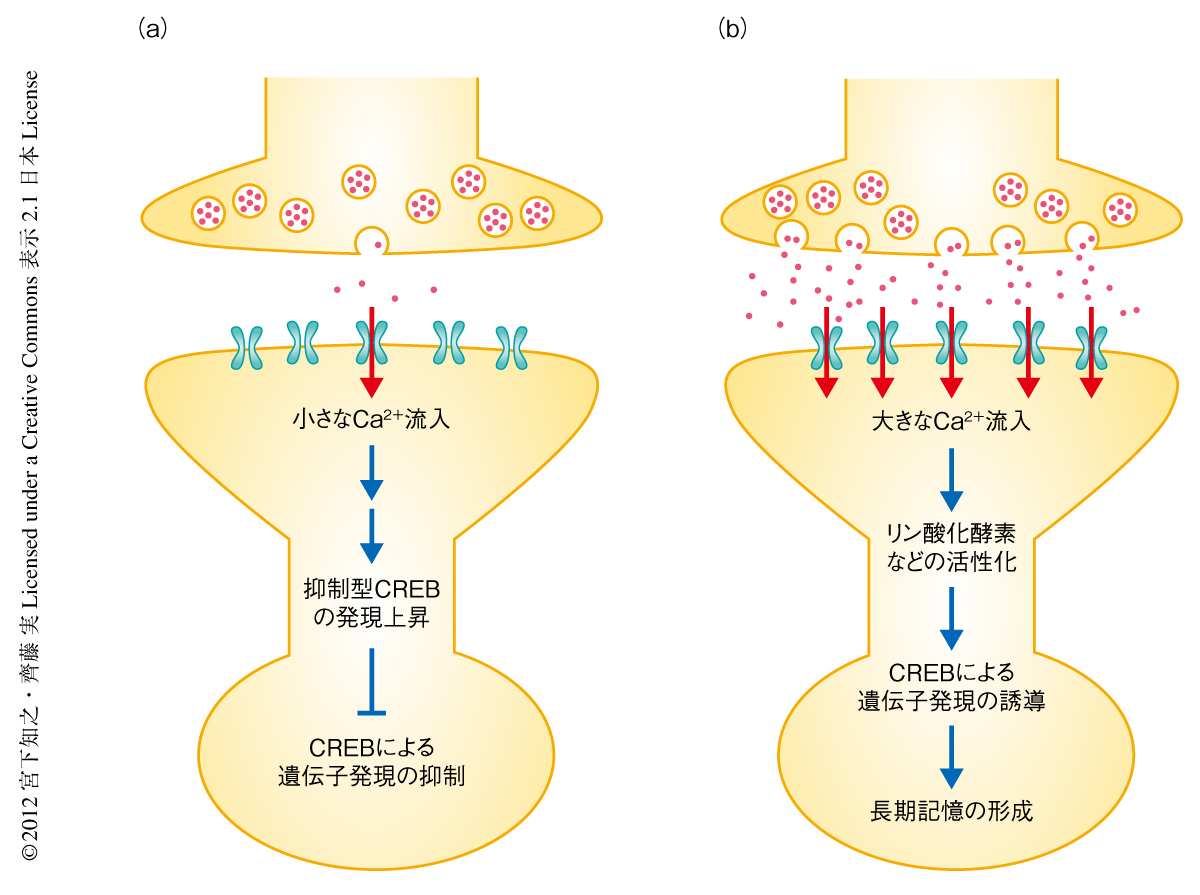
筆者らの結果は,NMDA受容体を介したCa2+の流入は,学習していないとき(非同期性)に起こるか,連合学習のとき(同期性)に起こるかでまったく異なる役割をもつことを示した(図2).非同期性の,おそらく,自発的な開口放出などによる小さなCa2+流入は,なんらかの分子機構により抑制型CREBの発現を上昇させ長期記憶に関連する遺伝子の発現誘導を阻害する.一方,同期性の大きなCa2+流入は連合学習やCREBの活性化に必要なリン酸化酵素の活性を上昇させ,長期記憶に関連する遺伝子の発現をCREB依存性に誘導する.Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいて同期性の入力は正常だが,後者の非同期性のCa2+流入は抑制不全である.一方,NMDA受容体NR1サブユニット変異ショウジョウバエにおいて前者の同期性のCa2+流入は阻害されるが,非同期性のCa2+流入は正常に抑制される.非同期性のCa2+流入により抑制型CREBの発現を増加させるのは何か? この機構の解明がつぎの重要な課題である.
略歴:1994年 東京都神経科学総合研究所 研究員,2000年 日本大学大学院農学研究科にて博士号取得,2011年より東京都医学総合研究所 主任研究員.
研究テーマ:分散効果(spacing effect)を中心とした長期記憶のシグナル伝達経路,老化による記憶障害の分子機構.
齊藤 実(Minoru Saitoe)
東京都医学総合研究所 参事研究員.
研究室URL:http://www.igakuken.or.jp/memory/index.html
© 2012 宮下知之・齊藤 実 Licensed under CC 表示 2.1 日本
(東京都医学総合研究所 学習記憶プロジェクト)
email:齊藤 実
DOI: 10.7875/first.author.2012.079
Mg2+ block of Drosophila NMDA receptors is required for long-term memory formation and CREB-dependent gene expression.
Tomoyuki Miyashita, Yoshiaki Oda, Junjiro Horiuchi, Jerry C. P. Yin, Takako Morimoto, Minoru Saitoe
Neuron, 74, 887-898 (2012)
要 約
NMDA受容体はMg2+ブロックという機構をもち,これにより,シナプス後細胞は興奮していないときにはNMDA受容体を介したCa2+の流入が抑制されている.これまで,NMDA受容体は連合学習の成立や長期記憶の形成に必要であることが示されてきたが,Mg2+ブロックがこれらにおいてどのような役割をはたしているかは不明であった.筆者らは,Mg2+ブロックを欠損した変異NMDA受容体を発現するトランスジェニックショウジョウバエを作製し,Mg2+ブロックは連合学習の成立には不要だが,長期記憶の形成には必須であることを示す結果を得た.このトランスジェニックショウジョウバエにおいては長期記憶学習に応じ転写因子CREBに依存して上昇する,長期記憶あるいは長期増強に関連する遺伝子の発現が顕著に抑制されていた.興味深いことに,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエの脳においては抑制型CREBの発現が顕著に増加していた.抑制型CREBの発現量と長期記憶の形成阻害とには顕著な正の相関があり,このトランスジェニックショウジョウバエでみられた長期記憶の形成阻害の一因は抑制型CREBの発現上昇にあることが示唆された.こうした結果から,Mg2+ブロックの生理的な役割は学習を行っていない定常状態においてNMDA受容体を介したCa2+の流入を阻止して抑制型CREBの発現を抑制することであり,これにより,長期記憶学習のときにCREBに依存した遺伝子発現は可能となることが示唆された.
はじめに
イオン透過型グルタミン酸受容体のひとつNMDA受容体は高いCa2+透過性をもち,細胞におけるシグナル伝達系の起点として重要な役割をはたしている.シナプス後細胞の興奮していないときにはNMDA受容体のイオン通過孔はMg2+によりふさがれていて1,2),グルタミン酸が結合してもCa2+は流入できない(図1).しかし,ほかのイオン透過型受容体の活性化などによりシナプス後細胞が脱分極の状態になるとこのMg2+は外れ,このとき,NMDA受容体にグルタミン酸が結合するとCa2+はシナプス後細胞に流入する.このように,NMDA受容体はMg2+ブロックを介してシナプス前細胞の活動とシナプス後細胞の活動の同期性と非同期性を判別できるため,連合学習において重要な役割を担うと考えられてきた(図1).
ショウジョウバエにおいてNMDA受容体は連合学習の成立と長期記憶の形成に必要である3).しかし,こうした過程にMg2+ブロックはどのように関与しているのか? なぜ非同期性のCa2+流入を抑制する必要があるのか? など,Mg2+ブロックの生理的な役割は不明であった.
1.Mg2+ブロックを欠損した変異NMDA受容体を発現するトランスジェニックショウジョウバエ
NMDA受容体はNR1サブユニットとNR2サブユニットからなるヘテロサブユニット複合体であり,Mg2+ブロックはそれぞれサブユニットの第2膜貫通領域のいわゆる“Mg2+ブロック部位”にあるアスパラギン残基に依存している4,5).このアスパラギン残基をグルタミン残基に置換するとMg2+ブロックは消失する4,6).
ショウジョウバエにおいて,NR1サブユニットのMg2+ブロック部位にあるアスパラギン残基をグルタミン残基に置換した変異体を神経系において発現するトランスジェニックショウジョウバエを作製した.このトランスジェニックショウジョウバエにおいて発現するNMDA受容体の電気生理学的な性質を調べたところ,Mg2+ブロックの顕著な欠損が観察された.哺乳類においてはNR1サブユニットのMg2+ブロック部位に変異を導入するとMg2+ブロックが消失するだけでなくCa2+透過性も減少する.しかし興味深いことに,このトランスジェニックショウジョウバエの発現する変異NMDA受容体においてはMg2+ブロックの消失に相関したCa2+透過性の顕著な減少は観察されなかった.
2.Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいては長期記憶の形成が特異的に阻害される
この結果から,作製されたトランスジェニックショウジョウバエはMg2+ブロックを欠損した変異NMDA受容体を発現していることがわかった.そこで,このトランスジェニックショウジョウバエを用いMg2+ブロックの生理的な役割を,匂い条件付け連合学習課題により調べた.Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエは,NMDA受容体のNR1サブユニットの発現を抑制した変異ショウジョウバエとは異なり,連合学習と短期記憶は正常だった.しかし,間隔を空けて行うくり返し学習による長期記憶学習により形成される長期記憶は,同様に阻害されていた.
Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいては内因性のNMDA受容体NR1サブユニットが残存しているため正常な連合学習が成立した可能性があった.しかし,NMDA受容体NR1サブユニット変異ショウジョウバエにおける連合学習は,Mg2+ブロックを欠失したNMDA受容体NR1サブユニットの発現により回復したことから,連合学習の成立にはMg2+ブロックは関与していないことが示唆された.
従来,Mg2+ブロックは連合学習の成立に必須であり,Mg2+ブロックによる連合性の入力と非連合性の入力との識別がなければ匂い条件付けにおいて特定の匂い刺激に対する連合学習は成立せず,あらゆる匂いに対し記憶の般化(generalization)が起こるものと想像されていた.しかし,調べた範囲において記憶の般化はみられなかった.
3.Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいてはCREBに依存して発現する長期記憶に関連する遺伝子の発現誘導が阻害されている
長期記憶の形成には長期記憶学習に応じた遺伝子発現が必要である.そこで,stau遺伝子,homer遺伝子,activin遺伝子といった長期記憶あるいは後期の長期増強の形成に必要な遺伝子の発現を長期記憶学習ののち調べたところ,野生型ショウジョウバエでみられるこれら遺伝子の発現上昇は,NMDA受容体NR1サブユニット変異ショウジョウバエのみならず,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいても顕著に抑制されていた.
長期記憶に関連する多くの遺伝子の発現には転写因子CREBの活性が重要な役割をはたしている7).stau遺伝子,homer遺伝子,activin遺伝子の長期記憶学習ののちの発現上昇もCREBに依存性であることがわかった.以上の結果から,Mg2+ブロックは長期記憶学習に応じCREBに依存して,長期記憶に関連する遺伝子が発現誘導されるために必要な機構であることがわかった.
4.Mg2+ブロックは学習を行っていないときの抑制型CREBの発現上昇を抑制する
転写因子CREBには転写活性をもつ活性型ともたない抑制型とがあり,学習を行っていない定常状態において抑制型CREBの発現が上昇すると,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエと同様に,長期記憶の形成が特異的に抑制される7).そこで,抑制型CREBの発現を調べたところ,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいては対照となる系統に比べ4倍近くも発現が上昇していた.この抑制型CREBの発現上昇がMg2+ブロックの消失によるものかどうかを調べるため,野生型ショウジョウバエの脳をMg2+の非存在において培養したところやはり抑制型CREBの発現が上昇し,この発現上昇はNMDA受容体の阻害剤により抑制された.
Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいて発現の上昇した抑制型CREBは長期記憶の形成を抑制するに十分なのか,抑制型CREBの発現量と長期記憶の形成阻害との相関を定量的に解析したところ正の相関が認められ,抑制型CREBの4倍近くの発現上昇より長期記憶の形成を顕著に阻害しうることが示された.以上の結果から,Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいて学習を行っていない定常状態ではNMDA受容体を介したCa2+流入の抑制の不全が起こり,その結果,抑制型CREBの発現が上昇し長期記憶の形成が阻害されることが示唆された.
おわりに
Mg2+ブロックはNMDA受容体のHebb型一致検出器(coincidence detector)としての機能をもたらす機構であり,シナプス後細胞における長期増強の誘発や連合学習におけるシナプスの機序を説明するのにきわめて都合のよい性質であると考えられてきた.しかし,今回の結果は,Mg2+ブロックは連合学習の成立ではなく,むしろ,長期記憶を成立させるために必要であることを強く示唆した.
筆者らの結果は,NMDA受容体を介したCa2+の流入は,学習していないとき(非同期性)に起こるか,連合学習のとき(同期性)に起こるかでまったく異なる役割をもつことを示した(図2).非同期性の,おそらく,自発的な開口放出などによる小さなCa2+流入は,なんらかの分子機構により抑制型CREBの発現を上昇させ長期記憶に関連する遺伝子の発現誘導を阻害する.一方,同期性の大きなCa2+流入は連合学習やCREBの活性化に必要なリン酸化酵素の活性を上昇させ,長期記憶に関連する遺伝子の発現をCREB依存性に誘導する.Mg2+ブロック変異NMDA受容体トランスジェニックショウジョウバエにおいて同期性の入力は正常だが,後者の非同期性のCa2+流入は抑制不全である.一方,NMDA受容体NR1サブユニット変異ショウジョウバエにおいて前者の同期性のCa2+流入は阻害されるが,非同期性のCa2+流入は正常に抑制される.非同期性のCa2+流入により抑制型CREBの発現を増加させるのは何か? この機構の解明がつぎの重要な課題である.
文 献
- Mayer, M. L., Westbrook, G. L. & Guthrie, P. B.: Voltage-dependent block by Mg2+ of NMDA responses in spinal cord neurons. Nature, 309, 261-263 (1984)[PubMed]
- Nowak, L., Bregestovski, P., Ascher, P. et al.: Magnesium gates glutamate-activated channels in mouse central neurons. Nature, 307, 462-465 (1984)[PubMed]
- Xia, S., Miyashita, T., Fu, T. F. et al.: NMDA receptors mediate olfactory learning and memory in Drosophila. Curr. Biol., 15, 603-615 (2005)[PubMed]
- Burnashev, N., Schoepfer, R., Monyer, H. et al.: Control by asparagine residues of calcium permeability and magnesium blockade in the NMDA receptor. Science, 257, 1415-1419 (1992)[PubMed]
- Mori, H., Masaki, H., Yamakura, T. et al.: Identification by mutagenesis of a Mg2+-block site of the NMDA receptor channel. Nature, 358, 673-675 (1992)[PubMed]
- Single, F. N., Rozov, A., Burnashev, N. et al.: Dysfunctions in mice by NMDA receptor point mutations NR1(N598Q) and NR1(N598R). J. Neurosci., 20, 2558-2566 (2000)[PubMed]
- Yin, J. C., Wallach, J. S., Del Vecchio, M. et al.: Induction of a dominant negative CREB transgene specifically blocks long-term memory in Drosophila. Cell, 79, 49-58 (1994)[PubMed]
著者プロフィール
略歴:1994年 東京都神経科学総合研究所 研究員,2000年 日本大学大学院農学研究科にて博士号取得,2011年より東京都医学総合研究所 主任研究員.
研究テーマ:分散効果(spacing effect)を中心とした長期記憶のシグナル伝達経路,老化による記憶障害の分子機構.
齊藤 実(Minoru Saitoe)
東京都医学総合研究所 参事研究員.
研究室URL:http://www.igakuken.or.jp/memory/index.html
© 2012 宮下知之・齊藤 実 Licensed under CC 表示 2.1 日本