P2X受容体のATP認識機構およびチャネル活性化機構
服部素之・Eric Gouaux
(米国Oregon Health and Science大学Vollum Institute)
email:服部素之
DOI: 10.7875/first.author.2012.054
Molecular mechanism of ATP binding and ion channel activation in P2X receptors.
Motoyuki Hattori, Eric Gouaux
Nature, 485, 207-212 (2012)
P2X受容体は細胞外のATPにより活性化されるリガンド作動性のイオンチャネルで,細胞外ATPシグナル伝達において中心的な役割をはたす受容体のひとつである.7つのサブタイプがホモ三量体およびヘテロ三量体を構成し,神経伝達,筋肉収縮,痛覚,味覚,炎症反応など,多様な生理現象にかかわることが知られている.しかしながら,その生理学的な重要性にもかかわらず,P2X受容体によるATP認識機構およびチャネル活性化機構の構造基盤はこれまで明らかではなかった.今回,筆者らは,P2X4受容体のATP結合型開状態とアポ型閉状態のX線結晶構造解析,および,それにともなう電気生理学的および生化学的な解析を行った.その結果,ATP結合型構造において新規のATP結合モチーフを見い出すとともに,その立体構造にもとづきP2X受容体によるATPの特異的な認識機構を明らかにした.また,得られたATP結合型開状態とアポ型閉状態の立体構造を比較することで,ATPの結合がどのような構造変化をひき起こしチャネルの開閉へとつながるのか,というチャネル活性化機構につき立体構造にもとづく分子機構を提唱した.
ATPは生命において代謝,生合成,能動輸送などのエネルギー源として広く用いられている.その一方で,神経伝達物質など細胞外におけるシグナル分子としてもATPは機能するという概念は古くから提唱されていたものの1),当時は広く受け入れられた概念ではなかった.そのような状況のなか,いまから約20年前にイオンチャネル型のP2X受容体およびGタンパク質共役型のP2Y受容体2) の2種類の細胞外ATP受容体が遺伝子クローニングされ3),それ以後,細胞外ATPシグナル伝達の研究は飛躍的な進展をみせている4).
P2X受容体は細胞外のATPにより活性化されるリガンド作動性かつ非選択性のカチオンチャネルである.エキソサイトーシスや組織の損傷などにともない細胞外へと放出されたATPにより活性化されたP2X受容体によるイオンの流入は,膜電位の変化やCa2+濃度の変化へとつながり一連の細胞内シグナル伝達をひき起こす.P2X受容体はP2X1からP2X7まで7つのサブタイプに分類され,それぞれのサブタイプがホモ三量体もしくはヘテロ三量体を構成することで,さまざまな生物物理学的および薬理学的な特性をもつ多様な機能を発揮している5).この多様なサブユニット構成をもつP2X受容体は生体において広く発現しており,神経伝達,筋肉収縮,痛覚,味覚,炎症反応など,さまざまな生理現象にかかわることが知られている.それにともない,P2X受容体は神経疾患,心血管疾患,炎症性疾患などに対する新規の治療薬の有望な標的とされている6).その一方で,構造解析にむけた試料の調製が困難である真核生物の膜タンパク質であることから,P2X受容体の高分解能な立体構造情報は近年まで非常にかぎられており,これまで,ゼブラフィッシュに由来するP2X4受容体のアポ型閉状態の立体構造が報告されているのみであった7).そのため,P2X受容体によるATP認識機構やATPの結合にともなうチャネル活性化機構についての立体構造にもとづく理解はきわめてかぎられた状況にあった.
ATP結合型をとるP2X受容体の立体構造を明らかにすべく,ATPの存在のもとP2X受容体の結晶化に適した発現コンストラクトの同定のため,さまざまな生物種に由来するP2X受容体オーソログの発現スクリーニングを行った.その結果,ゼブラフィッシュに由来するP2X4受容体の発現コンストラクトにさらに変異導入を行うことで,ATPの存在下において2.8Å分解能のX線回折像をあたえる良質な結晶を得た.また,生化学的および電気生理学的な解析により,この改良されたコンストラクトはP2X受容体として適切なATP結合能およびチャネル活性を保持していることもあわせて確認した.このような構造解析にむけた発現コンストラクトの機能評価は今回のP2X受容体の構造解析にかぎった話ではなく,それぞれ対象とするタンパク質の構造からどのような生物学的な議論を行いたいかをふまえたうえで,構造解析の前段階から機能評価を行っていく必要があるだろう.また,ATPの非存在下においても結晶化を行い,既知のアポ型構造(3.1Å分解能)より高分解能となる2.9Å分解能のX線回折データを収集した.得られたX線回折データを用い,ATP存在下およびATP非存在下におけるゼブラフィッシュに由来するP2X4受容体につき,分子置換法による構造決定を行った(PDB ID:4DW0,4DW1).
構造決定されたP2X4受容体は比較的大きな可溶性の細胞外ドメインと6回の膜貫通ヘリックスを含む膜貫通ドメインから構成されるホモ三量体を形成していた(図1a).これらのドメイン構成において,細胞外ドメインがATP結合能をもつのに対し,膜貫通ドメインはイオンの透過を担っていた.また,それぞれの単一サブニットは“イルカ”に似た形状をしており(図2a),以後の立体構造の説明には適宜この“イルカモデル”を用いる.ATP存在下およびATP非存在下のそれぞれのサブユニット構造を重ね合わせたところ,全体としてはよく一致していたものの,ATP結合部位および膜貫通ヘリックスにおいて大きな構造変化がみられた(図2a).ここでは,ATP存在下での立体構造,および,ATP存在下とATP非存在下での構造の比較をとおして,P2X受容体によるATP認識機構およびチャネル活性化機構を議論する.
ATPの存在下において構造決定されたP2X4受容体の構造において,以前のアポ型の構造においてはみられなかった有意な電子密度を同定し,電子密度の形状などからこれをATPに相当する電子密度であると結論づけた.このATP結合部位はP2X受容体三量体の細胞外ドメインのそれぞれのサブユニットのあいだに1つずつ存在しており(図1a),その結果,P2X受容体三量体には結晶学的な3回対称性にもとづく3つの等価なATP結合部位が存在していた.
このサブユニットのあいだに位置するATP結合部位は,アルギニン残基やリジン残基など正電荷をもつ多数のアミノ酸残基を含んでいた(図1b).これらのアミノ酸残基はP2X受容体ファミリーにおいて厳密に保存されており,さらに,過去に行われたさまざまな変異体の解析から,いずれのアミノ酸残基もP2X受容体のATP依存的なチャネル活性に重要であることが明らかとなっている.
このサブユニットのあいだに位置する正電荷クラスターは,ATPのそれぞれのリン酸基を非常に強固に認識していた(図1b),その結果,βリン酸およびγリン酸がアデニン環のほうにむかっており,ATPはU字型のような形状をしていた(図1b).これは,ほかの多くのATP結合タンパク質の構造ではATPのそれぞれのリン酸基がアデニン環から遠ざかるようなかたちで直線的に伸びた形状をしていると比較して,非常に特徴的であるといえた.また,この正電荷クラスターによるそれぞれのリン酸基の強固な認識は,ほかのアデノシンリン酸(ADPとAMP)に対し,P2X受容体がATPをどのように特異的に認識しているのかを説明するものであった.
その一方で,ATPのアデニン環はThr189の主鎖のカルボニル基および側鎖,Lys70の主鎖のカルボニル基とのあいだに合計3本の水素結合を形成していた(図1b).このATP結合部位にCTP,GTP,UTPといったほかのヌクレオチド三リン酸を重ね合わせたところ,それぞれのヌクレオチド三リン酸の塩基部分とATP結合部位とのあいだにそれぞれ2本,1本,0本の水素結合が形成可能であると示唆され,これは生化学的な解析ともよく一致していた.このことから,ヌクレオチド三リン酸の塩基部分とATP結合部位とのあいだに形成可能な水素結合の数が塩基特異性には重要であり,とくに,保存されたスレオニン残基がP2X受容体の塩基特異性を決定していることが強く示唆された.
それに対し,ATPのリボースとP2X受容体とのあいだでは,一部に疎水性の相互作用がみられたものの,特異的な水素結合の形成はみられなかった(図1b).また,このリボース環の2位と3位の酸素原子はいずれも溶媒との接触の可能な部位に位置しており(図1b),この部位が修飾されたリボース修飾ATPアナログがP2X受容体の非特異的な作用薬もしくは拮抗薬として作用することと一致した.そのため,今回の構造をもとに新たなリボース修飾ATPアナログをデザインすることで,P2X受容体に対する新規の阻害剤を創出することができるかもしれない.
以前から構造解析されていたアポ型のP2X受容体では,2番目の膜貫通ヘリックスから構成されるイオン透過孔はせまく閉じていた(図1c).それに対し,今回,新たに構造解析されたATP結合型のP2X受容体では,それぞれの膜貫通ヘリックスはイオン透過孔の中心から遠ざかるような構造変化をみせており,その結果,イオン透過孔は大きく開いた形状となっていた(図1c).このイオン透過孔はAla347およびLeu351の付近でもっとも狭くなっており(図1c),その直径はおよそ7Åであった.これは,以前の電気生理学的な解析から示唆されていた開状態のP2X受容体におけるイオン透過孔の大きさとよく一致するものであった.さらに,今回の構造においてはイオン透過孔を構成するアミノ酸残基についても過去の電気生理学的な解析とよく一致しており,それらのことから,今回,構造を決定したATP結合型のP2X受容体は,チャネルの“活性化型開状態”に相当するものであると考えられた.
“ATP結合型開状態”と“アポ型閉状態”の構造を比較することで,ATPの結合により開始されるチャネル活性機構の提唱を試みた(図2b).まず,ATPの結合にともない,“イルカモデル”における“Head”ととなりあうサブユニットの“Dorsal Fin”とから形成されるクレフトが閉じ,ATPを包み込むような構造変化が起こる.その一方で,“Left Flipper”はATP結合部位からはじき出されるような動きを示す.これらATP結合部位を形成するそれぞれのモチーフは,ATP結合部位と膜貫通ドメインとのあいだに位置する“Body”と構造的につながっている.そのため,Left FlipperおよびとなりあうサブユニットのDorsal Finに起こるATPに依存的な構造変化は,両方のサブニットのBodyが外側へ広がるような動きへとつながる.このBodyの構造変化において,Bodyの下半分を構成する“Lower Body”がレバーアームのような動きをみせるのに対し,その上半分を構成する“Upper Body”はほとんど構造変化を示さず,このレバーアーム運動における支点として機能する.さらに,Lower Bodyは膜貫通ドメインと直接につながっているため,Lower Bodyの外側へ広がるような構造変化はイオン透過孔の拡大をひき起こし,チャネルの閉状態から開状態への構造変化,つまり,チャネルの活性化へとつながる.すなわち,ATP結合部位,Lower Body,膜貫通ドメイン,それぞれの構造的な共役により,ATP結合部位における比較的小さな構造変化が膜貫通ドメインにおける大きな構造変化をひき起こすことを可能としている.
この研究では,P2X受容体の立体構造にもとづき,そのATP認識機構を明らかにするとともに,ATPの結合にともなうチャネル活性化機構を提唱した.これらの知見により,細胞外ATPシグナル伝達の開始を保証する分子機構の理解が大きく進展したといえる.また,この研究から得られたATP結合部位などの立体構造情報はP2X受容体を標的とした創薬の促進へとつながることが期待される.
しかしながら,細胞外ATPシグナル伝達の終結の理解に重要なATP結合型不活性状態である“脱感作状態”の立体構造はいまだ明らかになっておらず,P2X受容体を介した細胞外ATPシグナル伝達の開始から終結までの一連のダイナミクスの理解にはさらなる研究の進展が必要だといえる.また,P2X受容体はホモ三量体だけでなくヘテロ三量体を形成することで多様な機能の発現を実現しているものと思われるが,このヘテロ三量体の形成の立体構造にもとづく理解はほぼ皆無である.そのため,P2X受容体の構造生物学はまだまだはじまったばかりといっていい状況にあり,今後の展開に注目していきたい.
略歴:2009年 東京工業大学大学院生命理工学研究科 修了,同年より米国Oregon Health and Science大学 博士研究員.
研究テーマ:イオンチャネルの構造生物学.
抱負:立体構造の解析を出発点として,既知の現象の“説明”にとどまらず,新しい現象の“予測”につながるような研究をしていきたい.
Eric Gouaux
米国Oregon Health and Science大学Senior Scientist.
研究室URL:http://www.ohsu.edu/xd/research/centers-institutes/vollum/faculty/gouauxlab.cfm
© 2012 服部素之・Eric Gouaux Licensed under CC 表示 2.1 日本
(米国Oregon Health and Science大学Vollum Institute)
email:服部素之
DOI: 10.7875/first.author.2012.054
Molecular mechanism of ATP binding and ion channel activation in P2X receptors.
Motoyuki Hattori, Eric Gouaux
Nature, 485, 207-212 (2012)
要 約
P2X受容体は細胞外のATPにより活性化されるリガンド作動性のイオンチャネルで,細胞外ATPシグナル伝達において中心的な役割をはたす受容体のひとつである.7つのサブタイプがホモ三量体およびヘテロ三量体を構成し,神経伝達,筋肉収縮,痛覚,味覚,炎症反応など,多様な生理現象にかかわることが知られている.しかしながら,その生理学的な重要性にもかかわらず,P2X受容体によるATP認識機構およびチャネル活性化機構の構造基盤はこれまで明らかではなかった.今回,筆者らは,P2X4受容体のATP結合型開状態とアポ型閉状態のX線結晶構造解析,および,それにともなう電気生理学的および生化学的な解析を行った.その結果,ATP結合型構造において新規のATP結合モチーフを見い出すとともに,その立体構造にもとづきP2X受容体によるATPの特異的な認識機構を明らかにした.また,得られたATP結合型開状態とアポ型閉状態の立体構造を比較することで,ATPの結合がどのような構造変化をひき起こしチャネルの開閉へとつながるのか,というチャネル活性化機構につき立体構造にもとづく分子機構を提唱した.
はじめに
ATPは生命において代謝,生合成,能動輸送などのエネルギー源として広く用いられている.その一方で,神経伝達物質など細胞外におけるシグナル分子としてもATPは機能するという概念は古くから提唱されていたものの1),当時は広く受け入れられた概念ではなかった.そのような状況のなか,いまから約20年前にイオンチャネル型のP2X受容体およびGタンパク質共役型のP2Y受容体2) の2種類の細胞外ATP受容体が遺伝子クローニングされ3),それ以後,細胞外ATPシグナル伝達の研究は飛躍的な進展をみせている4).
P2X受容体は細胞外のATPにより活性化されるリガンド作動性かつ非選択性のカチオンチャネルである.エキソサイトーシスや組織の損傷などにともない細胞外へと放出されたATPにより活性化されたP2X受容体によるイオンの流入は,膜電位の変化やCa2+濃度の変化へとつながり一連の細胞内シグナル伝達をひき起こす.P2X受容体はP2X1からP2X7まで7つのサブタイプに分類され,それぞれのサブタイプがホモ三量体もしくはヘテロ三量体を構成することで,さまざまな生物物理学的および薬理学的な特性をもつ多様な機能を発揮している5).この多様なサブユニット構成をもつP2X受容体は生体において広く発現しており,神経伝達,筋肉収縮,痛覚,味覚,炎症反応など,さまざまな生理現象にかかわることが知られている.それにともない,P2X受容体は神経疾患,心血管疾患,炎症性疾患などに対する新規の治療薬の有望な標的とされている6).その一方で,構造解析にむけた試料の調製が困難である真核生物の膜タンパク質であることから,P2X受容体の高分解能な立体構造情報は近年まで非常にかぎられており,これまで,ゼブラフィッシュに由来するP2X4受容体のアポ型閉状態の立体構造が報告されているのみであった7).そのため,P2X受容体によるATP認識機構やATPの結合にともなうチャネル活性化機構についての立体構造にもとづく理解はきわめてかぎられた状況にあった.
1.P2X受容体の構造解析とその全体構造
ATP結合型をとるP2X受容体の立体構造を明らかにすべく,ATPの存在のもとP2X受容体の結晶化に適した発現コンストラクトの同定のため,さまざまな生物種に由来するP2X受容体オーソログの発現スクリーニングを行った.その結果,ゼブラフィッシュに由来するP2X4受容体の発現コンストラクトにさらに変異導入を行うことで,ATPの存在下において2.8Å分解能のX線回折像をあたえる良質な結晶を得た.また,生化学的および電気生理学的な解析により,この改良されたコンストラクトはP2X受容体として適切なATP結合能およびチャネル活性を保持していることもあわせて確認した.このような構造解析にむけた発現コンストラクトの機能評価は今回のP2X受容体の構造解析にかぎった話ではなく,それぞれ対象とするタンパク質の構造からどのような生物学的な議論を行いたいかをふまえたうえで,構造解析の前段階から機能評価を行っていく必要があるだろう.また,ATPの非存在下においても結晶化を行い,既知のアポ型構造(3.1Å分解能)より高分解能となる2.9Å分解能のX線回折データを収集した.得られたX線回折データを用い,ATP存在下およびATP非存在下におけるゼブラフィッシュに由来するP2X4受容体につき,分子置換法による構造決定を行った(PDB ID:4DW0,4DW1).
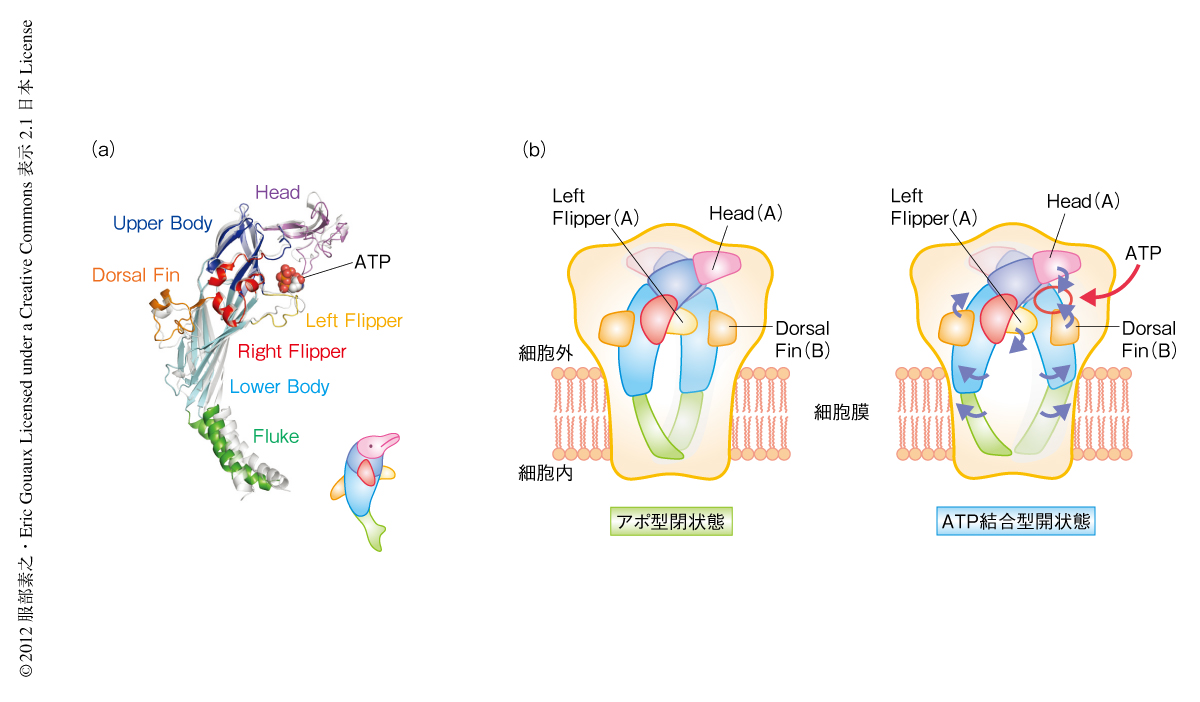
構造決定されたP2X4受容体は比較的大きな可溶性の細胞外ドメインと6回の膜貫通ヘリックスを含む膜貫通ドメインから構成されるホモ三量体を形成していた(図1a).これらのドメイン構成において,細胞外ドメインがATP結合能をもつのに対し,膜貫通ドメインはイオンの透過を担っていた.また,それぞれの単一サブニットは“イルカ”に似た形状をしており(図2a),以後の立体構造の説明には適宜この“イルカモデル”を用いる.ATP存在下およびATP非存在下のそれぞれのサブユニット構造を重ね合わせたところ,全体としてはよく一致していたものの,ATP結合部位および膜貫通ヘリックスにおいて大きな構造変化がみられた(図2a).ここでは,ATP存在下での立体構造,および,ATP存在下とATP非存在下での構造の比較をとおして,P2X受容体によるATP認識機構およびチャネル活性化機構を議論する.
2.ATP結合部位
ATPの存在下において構造決定されたP2X4受容体の構造において,以前のアポ型の構造においてはみられなかった有意な電子密度を同定し,電子密度の形状などからこれをATPに相当する電子密度であると結論づけた.このATP結合部位はP2X受容体三量体の細胞外ドメインのそれぞれのサブユニットのあいだに1つずつ存在しており(図1a),その結果,P2X受容体三量体には結晶学的な3回対称性にもとづく3つの等価なATP結合部位が存在していた.
このサブユニットのあいだに位置するATP結合部位は,アルギニン残基やリジン残基など正電荷をもつ多数のアミノ酸残基を含んでいた(図1b).これらのアミノ酸残基はP2X受容体ファミリーにおいて厳密に保存されており,さらに,過去に行われたさまざまな変異体の解析から,いずれのアミノ酸残基もP2X受容体のATP依存的なチャネル活性に重要であることが明らかとなっている.
このサブユニットのあいだに位置する正電荷クラスターは,ATPのそれぞれのリン酸基を非常に強固に認識していた(図1b),その結果,βリン酸およびγリン酸がアデニン環のほうにむかっており,ATPはU字型のような形状をしていた(図1b).これは,ほかの多くのATP結合タンパク質の構造ではATPのそれぞれのリン酸基がアデニン環から遠ざかるようなかたちで直線的に伸びた形状をしていると比較して,非常に特徴的であるといえた.また,この正電荷クラスターによるそれぞれのリン酸基の強固な認識は,ほかのアデノシンリン酸(ADPとAMP)に対し,P2X受容体がATPをどのように特異的に認識しているのかを説明するものであった.
その一方で,ATPのアデニン環はThr189の主鎖のカルボニル基および側鎖,Lys70の主鎖のカルボニル基とのあいだに合計3本の水素結合を形成していた(図1b).このATP結合部位にCTP,GTP,UTPといったほかのヌクレオチド三リン酸を重ね合わせたところ,それぞれのヌクレオチド三リン酸の塩基部分とATP結合部位とのあいだにそれぞれ2本,1本,0本の水素結合が形成可能であると示唆され,これは生化学的な解析ともよく一致していた.このことから,ヌクレオチド三リン酸の塩基部分とATP結合部位とのあいだに形成可能な水素結合の数が塩基特異性には重要であり,とくに,保存されたスレオニン残基がP2X受容体の塩基特異性を決定していることが強く示唆された.
それに対し,ATPのリボースとP2X受容体とのあいだでは,一部に疎水性の相互作用がみられたものの,特異的な水素結合の形成はみられなかった(図1b).また,このリボース環の2位と3位の酸素原子はいずれも溶媒との接触の可能な部位に位置しており(図1b),この部位が修飾されたリボース修飾ATPアナログがP2X受容体の非特異的な作用薬もしくは拮抗薬として作用することと一致した.そのため,今回の構造をもとに新たなリボース修飾ATPアナログをデザインすることで,P2X受容体に対する新規の阻害剤を創出することができるかもしれない.
3.イオン透過孔
以前から構造解析されていたアポ型のP2X受容体では,2番目の膜貫通ヘリックスから構成されるイオン透過孔はせまく閉じていた(図1c).それに対し,今回,新たに構造解析されたATP結合型のP2X受容体では,それぞれの膜貫通ヘリックスはイオン透過孔の中心から遠ざかるような構造変化をみせており,その結果,イオン透過孔は大きく開いた形状となっていた(図1c).このイオン透過孔はAla347およびLeu351の付近でもっとも狭くなっており(図1c),その直径はおよそ7Åであった.これは,以前の電気生理学的な解析から示唆されていた開状態のP2X受容体におけるイオン透過孔の大きさとよく一致するものであった.さらに,今回の構造においてはイオン透過孔を構成するアミノ酸残基についても過去の電気生理学的な解析とよく一致しており,それらのことから,今回,構造を決定したATP結合型のP2X受容体は,チャネルの“活性化型開状態”に相当するものであると考えられた.
4.チャネル活性化機構
“ATP結合型開状態”と“アポ型閉状態”の構造を比較することで,ATPの結合により開始されるチャネル活性機構の提唱を試みた(図2b).まず,ATPの結合にともない,“イルカモデル”における“Head”ととなりあうサブユニットの“Dorsal Fin”とから形成されるクレフトが閉じ,ATPを包み込むような構造変化が起こる.その一方で,“Left Flipper”はATP結合部位からはじき出されるような動きを示す.これらATP結合部位を形成するそれぞれのモチーフは,ATP結合部位と膜貫通ドメインとのあいだに位置する“Body”と構造的につながっている.そのため,Left FlipperおよびとなりあうサブユニットのDorsal Finに起こるATPに依存的な構造変化は,両方のサブニットのBodyが外側へ広がるような動きへとつながる.このBodyの構造変化において,Bodyの下半分を構成する“Lower Body”がレバーアームのような動きをみせるのに対し,その上半分を構成する“Upper Body”はほとんど構造変化を示さず,このレバーアーム運動における支点として機能する.さらに,Lower Bodyは膜貫通ドメインと直接につながっているため,Lower Bodyの外側へ広がるような構造変化はイオン透過孔の拡大をひき起こし,チャネルの閉状態から開状態への構造変化,つまり,チャネルの活性化へとつながる.すなわち,ATP結合部位,Lower Body,膜貫通ドメイン,それぞれの構造的な共役により,ATP結合部位における比較的小さな構造変化が膜貫通ドメインにおける大きな構造変化をひき起こすことを可能としている.
おわりに
この研究では,P2X受容体の立体構造にもとづき,そのATP認識機構を明らかにするとともに,ATPの結合にともなうチャネル活性化機構を提唱した.これらの知見により,細胞外ATPシグナル伝達の開始を保証する分子機構の理解が大きく進展したといえる.また,この研究から得られたATP結合部位などの立体構造情報はP2X受容体を標的とした創薬の促進へとつながることが期待される.
しかしながら,細胞外ATPシグナル伝達の終結の理解に重要なATP結合型不活性状態である“脱感作状態”の立体構造はいまだ明らかになっておらず,P2X受容体を介した細胞外ATPシグナル伝達の開始から終結までの一連のダイナミクスの理解にはさらなる研究の進展が必要だといえる.また,P2X受容体はホモ三量体だけでなくヘテロ三量体を形成することで多様な機能の発現を実現しているものと思われるが,このヘテロ三量体の形成の立体構造にもとづく理解はほぼ皆無である.そのため,P2X受容体の構造生物学はまだまだはじまったばかりといっていい状況にあり,今後の展開に注目していきたい.
文 献
- Burnstock, G.: Purinergic nerves. Pharmacol. Rev., 24, 509-581 (1972)[PubMed]
- Webb, T. E., Simon, J., Krishek, B. J. et al.: Cloning and functional expression of a brain G-protein-coupled ATP receptor. FEBS Lett., 324, 219-225 (1993)[PubMed]
- Valera, S., Hussy, N., Evans, R. J. et al.: A new class of ligand-gated ion channel defined by P2x receptor for extracellular ATP. Nature, 371, 516-519 (1994)[PubMed]
- Burnstock, G.: Purinergic signalling: Its unpopular beginning, its acceptance and its exciting future. BioEssays, 34, 218-225 (2012)[PubMed]
- Jarvis, M. F. & Khakh, B. S.: ATP-gated P2X cation-channels. Neuropharmacology, 56, 208-215 (2009)[PubMed]
- Coddou, C., Yan, Z., Obsil, T. et al.: Activation and regulation of purinergic P2X receptor channels. Pharmacol. Rev., 63, 641-683 (2011)[PubMed]
- Kawate, T., Michel, J. C., Birdsong, W. T. et al.: Crystal structure of the ATP-gated P2X4 ion channel in the closed state. Nature, 460, 592-598 (2009)[PubMed]
著者プロフィール
略歴:2009年 東京工業大学大学院生命理工学研究科 修了,同年より米国Oregon Health and Science大学 博士研究員.
研究テーマ:イオンチャネルの構造生物学.
抱負:立体構造の解析を出発点として,既知の現象の“説明”にとどまらず,新しい現象の“予測”につながるような研究をしていきたい.
Eric Gouaux
米国Oregon Health and Science大学Senior Scientist.
研究室URL:http://www.ohsu.edu/xd/research/centers-institutes/vollum/faculty/gouauxlab.cfm
© 2012 服部素之・Eric Gouaux Licensed under CC 表示 2.1 日本