細胞老化を誘導するDNA損傷シグナルはユビキチンリガーゼを介したヒストンメチル化酵素の分解を誘導する
高橋暁子・原 英二
(がん研究会がん研究所 がん生物部)
email:原 英二
DOI: 10.7875/first.author.2012.002
DNA damage signaling triggers degradation of histone methyltransferases through APC/CCdh1 in senescent cells.
Akiko Takahashi, Yoshinori Imai, Kimi Yamakoshi, Shinji Kuninaka, Naoko Ohtani, Shin Yoshimoto, Satoshi Hori, Makoto Tachibana, Emma Anderton, Takashi Takeuchi, Yoichi Shinkai, Gordon Peters, Hideyuki Saya, Eiji Hara
Molecular Cell, 45, 123-131 (2012)
細胞老化は発がんの危険性のあるさまざまなストレスにより誘導され,細胞の増殖を不可逆的に停止することでがん抑制機構としてはたらいていることが明らかになってきた.しかし最近になり,細胞が老化すると炎症反応や発がんを誘導する作用を示すさまざまな分泌性タンパク質が高発現するSASP(senescence-associated secretory phenotype)とよばれる現象が起こることが報告された.つまり,細胞老化には,生体にとって異常な細胞の増殖を抑制してがんを防ぐという正の作用と,為害性のある物質を分泌して周辺組織に病態をひき起こすという負の作用の,両方の側面のあることが示唆されている.SASPの誘導を制御することで細胞老化の負の側面を防ぐことが可能であると考えられるが,その誘導機構はほとんど明らかになっていない.今回,筆者らは,DNA損傷シグナルにより活性化したユビキチンリガーゼAPC/CCdh1がヒストンメチル化酵素であるG9a/GLPを分解し,主要なSASP構成因子の遺伝子発現を誘導することを明らかにした.
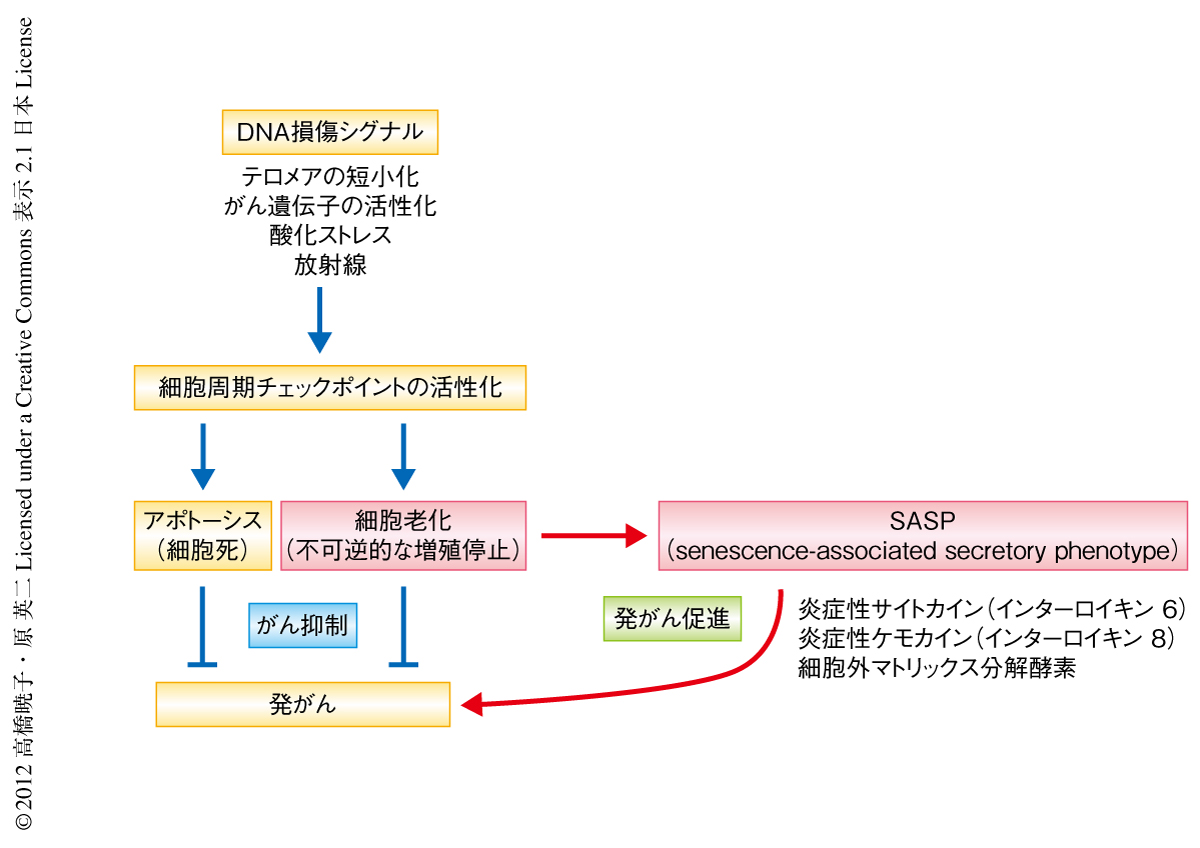
われわれの体を構成している細胞の多くでは細胞分裂の回数に限界があり,加齢とともに細胞もまた老化することが知られている.一部の幹細胞を除き,ヒトの正常な体細胞が示すこの分裂回数の限界(分裂寿命)は“細胞老化”とよばれ,細胞が過度に増殖してがん化することを防いでいるものと考えられている1).また,分裂寿命に達する以前の細胞が発がんの危険性のあるストレス(DNAの損傷,テロメアの短小化,がん遺伝子の活性化など)に曝露された場合にも,すみやかに細胞老化と同様の不可逆的な分裂停止を起こすことが明らかになってきている1).これらの知見から,細胞老化はアポトーシス(プログラムされた細胞死)と同様に,異常をもつ細胞の増殖を抑制する重要ながん抑制機構としてはたらいているものと考えられている1)(図1).しかし,細胞が死滅して体内から除去されるアポトーシスとは異なり,細胞老化を起こした細胞(老化細胞)はすぐには死滅しないため,加齢とともに老化細胞が体内に蓄積していくことが知られている2).一方,加齢にともないがんの発症率も顕著に増加することから,老化細胞の体内への蓄積と発がんの頻度の上昇とのあいだには正の相関があるのではないかと考えられてきた3).
細胞老化の特徴として,細胞増殖を停止すること以外にも,大きく広がった形態やDNA損傷シグナルの活性化など,さまざまな表現型が報告されてきた1).さらに近年,細胞老化により遺伝子の発現プロファイルが大きく変化することも明らかになってきた.なかでも,細胞が老化にともない炎症性サイトカインや炎症性ケモカイン,細胞外マトリックス分解酵素などさまざまな分泌性タンパク質を高発現し,それらを細胞外に分泌するSASP(senescence-associated secretory phenotype)とよばれる現象が注目されている4).これらの分泌性タンパク質(SASPタンパク質)の多くは炎症反応や発がんを促進する作用をもつことが知られており,老化細胞がSASPを介して発がんを促進している可能性も示唆されている5,6)(図1).このため,細胞老化にともなうSASPの誘導機構を解明しその制御方法をみつけることは,炎症やがんなど加齢にともなうさまざまな疾患の発症機序の解明や予防法の開発に役立つものと期待される.
細胞老化の誘導においてはDNA損傷応答が重要な役割を担うことが知られているが1),SASPの誘導にもDNA損傷応答が必要であることが報告されている7).筆者らは,細胞老化を誘導するようなDNA損傷応答が起こると,DNAをメチル化することで遺伝子発現を抑制するDNAメチル化酵素DNMT1の発現レベルが低下することを見い出していた8).そこでまず,このDNMT1の発現低下がSASPタンパク質の発現を誘導するのではないかと考えた.ヒト正常二倍体線維芽細胞においてDNMT1の発現を抑制したところ,予想どおり,インターロイキン6やインターロイキン8など主要なSASPタンパク質をコードする遺伝子(SASP遺伝子)の発現誘導が確認された.しかし不思議なことに,SASP遺伝子の転写制御領域のDNAメチル化にはまったく変化がみられなかったことから,DNMT1はDNAのメチル化以外の分子機構によりSASP遺伝子の発現を抑制していることが示唆された.
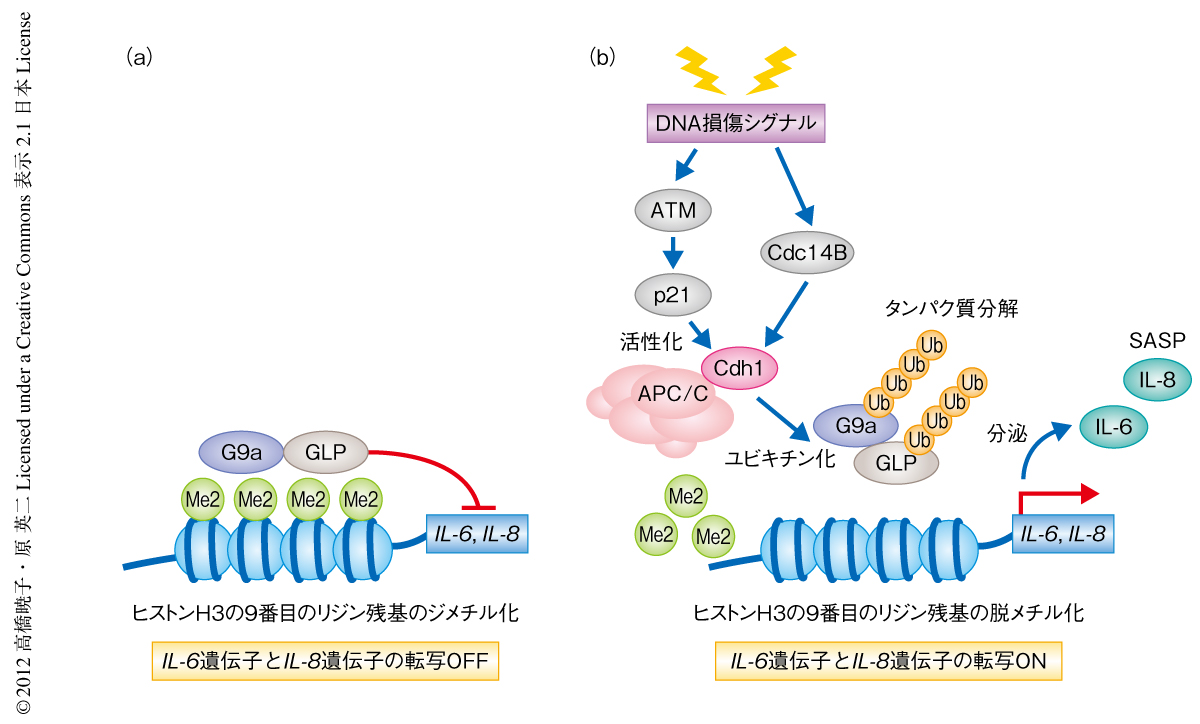
DNMT1には,ユークロマチンにおいて遺伝子発現の抑制をひき起こすヒストンH3の9番目のリジン残基のジメチル化を行うヒストンメチル化酵素G9aと結合し,そのヒストンメチル化活性を促進する作用のあることが報告されている9).そこで,クロマチン免疫沈降法を用いてSASP遺伝子の転写制御領域におけるヒストンH3の9番目のリジン残基のジメチル化レベルを調べたところ,細胞老化により顕著に減少していた.しかし予想に反して,ヒト正常二倍体線維芽細胞ではDNMT1とG9aやGLP(G9aのホモログ)との結合はまったく認められなかったことから,DNMT1の発現レベルの低下がいったいどのようにしてヒストンH3の9番目のリジン残基のジメチル化を抑制したのかという疑問が生じた.そこでさまざまな検討を重ねた結果,DNMT1の発現レベルの低下はDNA損傷応答をひき起こすことでG9a/GLPのプロテアソームに依存的なタンパク質分解が促進され,これによりヒストンH3の9番目のリジン残基のジメチル化レベルが低下することが明らかになった.つまり,DNA損傷応答はDNMT1の発現を抑制するが8),DNMT1の発現レベルの低下はDNA損傷応答をひき起こすため,正のフィードバックによりDNA損傷応答シグナルが持続するようになるものと考えられた.また,継代培養やがん遺伝子の過剰発現などによりヒト正常二倍体線維芽細胞に細胞老化を誘導した場合にもG9a/GLPのタンパク質分解が起こり,DNA損傷応答シグナルを阻害することでこのG9a/GLPの分解が回避されることが明らかになった.以上のことから,細胞老化を誘導するような持続的なDNA損傷応答シグナルの活性化によりG9a/GLPのタンパク質分解が促進され,SASP遺伝子の転写制御領域におけるヒストンH3の9番目のリジン残基のジメチル化レベルの低下をひき起こし,その結果,SASP遺伝子の発現が誘導されるものと考えられた(図2).
つぎに,G9a/GLPにはたらくユビキチンリガーゼを同定するため,DNA損傷応答により活性化されるユビキチンリガーゼに着目して検討を重ねた.その結果,老化細胞においてAPC/CCdh1をノックダウンすることでG9a/GLPのユビキチン化とタンパク質分解が阻害され,ヒストンH3の9番目のリジン残基のジメチル化レベルが低下しSASP遺伝子の発現が抑制されることを見い出した(図2).さらに,このAPC/CCdh1の活性化には,DNA損傷応答における主要なメディエーターであるATMを介したサイクリン依存性キナーゼ阻害タンパク質p21の誘導の経路と,DNA損傷応答により活性化するホスファターゼCdc14Bの経路の,2つの経路によるCdh1の脱リン酸化が重要であることが明らかになった(図2).これらの結果は,細胞老化を起こすようなストレス(テロメアの短小化,がん遺伝子の活性化,過度な酸化ストレスなど)により誘導される恒常的なDNA損傷応答シグナルが,ユビキチンリガーゼであるAPC/CCdh1の活性化をひき起こすことでヒストンメチル化酵素の分解を介してエピジェネティックな遺伝子発現の調節機構に変化を起こすことを示しており,その結果,SASPが起こるものと考えられた.さらに,DNAマイクロアレイを用いた遺伝子発現プロファイル解析を行い,インターロイキン6遺伝子やインターロイキン8遺伝子以外にも多くのSASP遺伝子の発現がAPC/CCdh1により制御されていることを明らかにした.これらのことから,このAPC/CCdh1-G9a/GLP経路がSASPの制御に中心的な役割を担っているものと考えられた.また,培養細胞のみならず,老化したマウスの臓器(肺,脾臓,小腸など)や,発がんストレスにより細胞老化を起こしたパピローマ(乳頭腫)など,老化細胞の存在が確認されているさまざまな組織においてもDNA損傷応答シグナルの亢進とG9a/GLPの発現低下およびSASP遺伝子の発現上昇がみられたことから,この分子機構が生体においてもはたらいていることが示唆された.
今回の研究結果は,細胞老化の副作用ともいうべきSASPがヒストンのメチル化によりエピジェネティックに制御されていることを示したはじめての報告であり,DNA損傷応答がいかにして遺伝子発現のグローバルな変化をひき起こすのか,その分子機構の一端を明らかにしたものである.今後は,がんや炎症など加齢にともなうさまざまな疾患の発症とSASPとのかかわりを追求し,細胞老化の生体における役割をより深く理解するとともに,将来的にSASPを標的とした疾患の発症制御をめざしたい.
略歴:2003年 北海道大学大学院歯学研究科博士課程 修了,2004年 徳島大学ゲノム機能研究センター ポスドクを経て,2007年よりがん研究会がん研究所 研究員.
研究テーマ:細胞老化の生体における機能とその分子機構.
原 英二(Eiji Hara)
がん研究会がん研究所 部長.
研究室URL:http://www.jfcr.or.jp/tci/canbio/index.html
(がん研究会がん研究所 がん生物部)
email:原 英二
DOI: 10.7875/first.author.2012.002
DNA damage signaling triggers degradation of histone methyltransferases through APC/CCdh1 in senescent cells.
Akiko Takahashi, Yoshinori Imai, Kimi Yamakoshi, Shinji Kuninaka, Naoko Ohtani, Shin Yoshimoto, Satoshi Hori, Makoto Tachibana, Emma Anderton, Takashi Takeuchi, Yoichi Shinkai, Gordon Peters, Hideyuki Saya, Eiji Hara
Molecular Cell, 45, 123-131 (2012)
この論文に出現する遺伝子・タンパク質のUniprot ID
ユビキチンリガーゼ, ヒストンメチル化酵素, histone methyltransferases, APC/C, Cdh1(Q9UM11), SASP, senescence associated secretory phenotype, ユビキチンリガーゼAPC/C, G9a(Q96KQ7), GLP(Q9H9B1), 炎症性サイトカイン, 炎症性ケモカイン, 細胞外マトリックス分解酵素, DNAメチル化酵素DNMT1(P26358), DNMT1(P26358), インターロイキン6(P05231), インターロイキン8(P10145), ヒストンH3, ヒストンメチル化酵素G9a(Q96KQ7), ATM(Q13315), サイクリン依存性キナーゼ阻害タンパク質p21(P38936), ホスファターゼCdc14B(O60729), IL-6(P05231), IL-8(P10145), p21(P38936), Cdc14B(O60729)
要 約
細胞老化は発がんの危険性のあるさまざまなストレスにより誘導され,細胞の増殖を不可逆的に停止することでがん抑制機構としてはたらいていることが明らかになってきた.しかし最近になり,細胞が老化すると炎症反応や発がんを誘導する作用を示すさまざまな分泌性タンパク質が高発現するSASP(senescence-associated secretory phenotype)とよばれる現象が起こることが報告された.つまり,細胞老化には,生体にとって異常な細胞の増殖を抑制してがんを防ぐという正の作用と,為害性のある物質を分泌して周辺組織に病態をひき起こすという負の作用の,両方の側面のあることが示唆されている.SASPの誘導を制御することで細胞老化の負の側面を防ぐことが可能であると考えられるが,その誘導機構はほとんど明らかになっていない.今回,筆者らは,DNA損傷シグナルにより活性化したユビキチンリガーゼAPC/CCdh1がヒストンメチル化酵素であるG9a/GLPを分解し,主要なSASP構成因子の遺伝子発現を誘導することを明らかにした.
はじめに
われわれの体を構成している細胞の多くでは細胞分裂の回数に限界があり,加齢とともに細胞もまた老化することが知られている.一部の幹細胞を除き,ヒトの正常な体細胞が示すこの分裂回数の限界(分裂寿命)は“細胞老化”とよばれ,細胞が過度に増殖してがん化することを防いでいるものと考えられている1).また,分裂寿命に達する以前の細胞が発がんの危険性のあるストレス(DNAの損傷,テロメアの短小化,がん遺伝子の活性化など)に曝露された場合にも,すみやかに細胞老化と同様の不可逆的な分裂停止を起こすことが明らかになってきている1).これらの知見から,細胞老化はアポトーシス(プログラムされた細胞死)と同様に,異常をもつ細胞の増殖を抑制する重要ながん抑制機構としてはたらいているものと考えられている1)(図1).しかし,細胞が死滅して体内から除去されるアポトーシスとは異なり,細胞老化を起こした細胞(老化細胞)はすぐには死滅しないため,加齢とともに老化細胞が体内に蓄積していくことが知られている2).一方,加齢にともないがんの発症率も顕著に増加することから,老化細胞の体内への蓄積と発がんの頻度の上昇とのあいだには正の相関があるのではないかと考えられてきた3).
細胞老化の特徴として,細胞増殖を停止すること以外にも,大きく広がった形態やDNA損傷シグナルの活性化など,さまざまな表現型が報告されてきた1).さらに近年,細胞老化により遺伝子の発現プロファイルが大きく変化することも明らかになってきた.なかでも,細胞が老化にともない炎症性サイトカインや炎症性ケモカイン,細胞外マトリックス分解酵素などさまざまな分泌性タンパク質を高発現し,それらを細胞外に分泌するSASP(senescence-associated secretory phenotype)とよばれる現象が注目されている4).これらの分泌性タンパク質(SASPタンパク質)の多くは炎症反応や発がんを促進する作用をもつことが知られており,老化細胞がSASPを介して発がんを促進している可能性も示唆されている5,6)(図1).このため,細胞老化にともなうSASPの誘導機構を解明しその制御方法をみつけることは,炎症やがんなど加齢にともなうさまざまな疾患の発症機序の解明や予防法の開発に役立つものと期待される.
1.DNA損傷応答はヒストンメチル化酵素のユビキチン化を促進する
細胞老化の誘導においてはDNA損傷応答が重要な役割を担うことが知られているが1),SASPの誘導にもDNA損傷応答が必要であることが報告されている7).筆者らは,細胞老化を誘導するようなDNA損傷応答が起こると,DNAをメチル化することで遺伝子発現を抑制するDNAメチル化酵素DNMT1の発現レベルが低下することを見い出していた8).そこでまず,このDNMT1の発現低下がSASPタンパク質の発現を誘導するのではないかと考えた.ヒト正常二倍体線維芽細胞においてDNMT1の発現を抑制したところ,予想どおり,インターロイキン6やインターロイキン8など主要なSASPタンパク質をコードする遺伝子(SASP遺伝子)の発現誘導が確認された.しかし不思議なことに,SASP遺伝子の転写制御領域のDNAメチル化にはまったく変化がみられなかったことから,DNMT1はDNAのメチル化以外の分子機構によりSASP遺伝子の発現を抑制していることが示唆された.
DNMT1には,ユークロマチンにおいて遺伝子発現の抑制をひき起こすヒストンH3の9番目のリジン残基のジメチル化を行うヒストンメチル化酵素G9aと結合し,そのヒストンメチル化活性を促進する作用のあることが報告されている9).そこで,クロマチン免疫沈降法を用いてSASP遺伝子の転写制御領域におけるヒストンH3の9番目のリジン残基のジメチル化レベルを調べたところ,細胞老化により顕著に減少していた.しかし予想に反して,ヒト正常二倍体線維芽細胞ではDNMT1とG9aやGLP(G9aのホモログ)との結合はまったく認められなかったことから,DNMT1の発現レベルの低下がいったいどのようにしてヒストンH3の9番目のリジン残基のジメチル化を抑制したのかという疑問が生じた.そこでさまざまな検討を重ねた結果,DNMT1の発現レベルの低下はDNA損傷応答をひき起こすことでG9a/GLPのプロテアソームに依存的なタンパク質分解が促進され,これによりヒストンH3の9番目のリジン残基のジメチル化レベルが低下することが明らかになった.つまり,DNA損傷応答はDNMT1の発現を抑制するが8),DNMT1の発現レベルの低下はDNA損傷応答をひき起こすため,正のフィードバックによりDNA損傷応答シグナルが持続するようになるものと考えられた.また,継代培養やがん遺伝子の過剰発現などによりヒト正常二倍体線維芽細胞に細胞老化を誘導した場合にもG9a/GLPのタンパク質分解が起こり,DNA損傷応答シグナルを阻害することでこのG9a/GLPの分解が回避されることが明らかになった.以上のことから,細胞老化を誘導するような持続的なDNA損傷応答シグナルの活性化によりG9a/GLPのタンパク質分解が促進され,SASP遺伝子の転写制御領域におけるヒストンH3の9番目のリジン残基のジメチル化レベルの低下をひき起こし,その結果,SASP遺伝子の発現が誘導されるものと考えられた(図2).
2.DNA損傷応答により活性化したユビキチンリガーゼAPC/CCdh1がG9a/GLPのユビキチン化をひき起こす
つぎに,G9a/GLPにはたらくユビキチンリガーゼを同定するため,DNA損傷応答により活性化されるユビキチンリガーゼに着目して検討を重ねた.その結果,老化細胞においてAPC/CCdh1をノックダウンすることでG9a/GLPのユビキチン化とタンパク質分解が阻害され,ヒストンH3の9番目のリジン残基のジメチル化レベルが低下しSASP遺伝子の発現が抑制されることを見い出した(図2).さらに,このAPC/CCdh1の活性化には,DNA損傷応答における主要なメディエーターであるATMを介したサイクリン依存性キナーゼ阻害タンパク質p21の誘導の経路と,DNA損傷応答により活性化するホスファターゼCdc14Bの経路の,2つの経路によるCdh1の脱リン酸化が重要であることが明らかになった(図2).これらの結果は,細胞老化を起こすようなストレス(テロメアの短小化,がん遺伝子の活性化,過度な酸化ストレスなど)により誘導される恒常的なDNA損傷応答シグナルが,ユビキチンリガーゼであるAPC/CCdh1の活性化をひき起こすことでヒストンメチル化酵素の分解を介してエピジェネティックな遺伝子発現の調節機構に変化を起こすことを示しており,その結果,SASPが起こるものと考えられた.さらに,DNAマイクロアレイを用いた遺伝子発現プロファイル解析を行い,インターロイキン6遺伝子やインターロイキン8遺伝子以外にも多くのSASP遺伝子の発現がAPC/CCdh1により制御されていることを明らかにした.これらのことから,このAPC/CCdh1-G9a/GLP経路がSASPの制御に中心的な役割を担っているものと考えられた.また,培養細胞のみならず,老化したマウスの臓器(肺,脾臓,小腸など)や,発がんストレスにより細胞老化を起こしたパピローマ(乳頭腫)など,老化細胞の存在が確認されているさまざまな組織においてもDNA損傷応答シグナルの亢進とG9a/GLPの発現低下およびSASP遺伝子の発現上昇がみられたことから,この分子機構が生体においてもはたらいていることが示唆された.
おわりに
今回の研究結果は,細胞老化の副作用ともいうべきSASPがヒストンのメチル化によりエピジェネティックに制御されていることを示したはじめての報告であり,DNA損傷応答がいかにして遺伝子発現のグローバルな変化をひき起こすのか,その分子機構の一端を明らかにしたものである.今後は,がんや炎症など加齢にともなうさまざまな疾患の発症とSASPとのかかわりを追求し,細胞老化の生体における役割をより深く理解するとともに,将来的にSASPを標的とした疾患の発症制御をめざしたい.
文 献
- Kuilman, T., Michaloglou, C., Mooi, W. J. et al.: The essence of senescence. Genes Dev., 24, 2463-2479 (2010)[PubMed]
- Herbig, U., Ferreira, M., Condel, L. et al.: Cellular senescence in aging primates. Science, 311, 1257 (2006)[PubMed]
- Campisi, J.: Senescent cells, tumor suppression, and organismal aging: good citizens, bad neighbors. Cell, 120, 513-522 (2005)[PubMed]
- Rodier, F. & Campisi, J.: Four faces of cellular senescence. J. Cell Biol., 192, 547-556 (2011)[PubMed]
- Sparmann, A. & Bar-Sagi, D.: Ras-induced interleukin-8 expression plays a critical role in tumor growth and angiogenesis. Cancer Cell, 6, 447-458 (2004)[PubMed]
- Ancrile, B., Lim, K. H. & Counter, C. M.: Oncogenic Ras-induced secretion of IL6 is required for tumorigenesis. Genes Dev., 21, 1714-1719 (2007)[PubMed]
- Rodier, F., Coppe, J. P., Patil, C. K. et al.: Persistent DNA damage signalling triggers senescence-associated inflammatory cytokine secretion. Nat. Cell Biol., 11, 973-979 (2009)[PubMed]
- Yamakoshi, K., Takahashi, A., Hirota, F. et al.: Real-time in vivo imaging of p16Ink4a reveals cross talk with p53. J. Cell Biol., 186, 393-407 (2009)[PubMed]
- Esteve, P. O., Chin, H. G., Smallwood, A. et al.: Direct interaction between DNMT1 and G9a coordinates DNA and histone methylation during replication. Genes Dev., 20, 3089-3103 (2006)[PubMed]
著者プロフィール
略歴:2003年 北海道大学大学院歯学研究科博士課程 修了,2004年 徳島大学ゲノム機能研究センター ポスドクを経て,2007年よりがん研究会がん研究所 研究員.
研究テーマ:細胞老化の生体における機能とその分子機構.
原 英二(Eiji Hara)
がん研究会がん研究所 部長.
研究室URL:http://www.jfcr.or.jp/tci/canbio/index.html
© 2012 高橋暁子・原 英二 Licensed under CC 表示 2.1 日本