TLR3-mTOR複合体2シグナルによるヘルペス脳炎の制御
佐藤亮太・三宅健介
(東京大学医科学研究所 感染遺伝学分野)
email:佐藤亮太,三宅健介
DOI: 10.7875/first.author.2018.098
Combating herpesvirus encephalitis by potentiating a TLR3-mTORC2 axis.
Ryota Sato, Akihisa Kato, Takahiko Chimura, Shin-Ichiroh Saitoh, Takuma Shibata, Yusuke Murakami, Ryutaro Fukui, Kaiwen Liu, Yun Zhang, Jun Arii, Ge-Hong Sun-Wada, Yoh Wada, Tsuneo Ikenoue, Glen N. Barber, Toshiya Manabe, Yasushi Kawaguchi, Kensuke Miyake
Nature Immunology, 19, 1071-1082 (2018)
Toll様受容体(Toll-like receptor:TLR)のひとつであるTLR3は,脳における単純ヘルペスウイルス1型に対する感染防御に不可欠な2本鎖RNAのセンサーである.しかし,TLR3の応答を制御する機構や脳においてTLR3が機能する細胞については不明だった.この研究において,筆者らは,TLR3がニューロンおよびアストロサイトにおける単純ヘルペスウイルス1型に対する感染防御に必要であることを明らかにした.また,単純ヘルペスウイルス1型の感染において,TLR3が代謝のセンサーであるmTOR複合体2と結合し活性化されることにより,ケモカインの発現およびTLR3の細胞の辺縁部への輸送がひき起こされた.このTLR3の細胞内輸送により,mTOR複合体1を含むI型インターフェロンの発現に関連するタンパク質の活性化が可能になった.マウスを用いた単純ヘルペスウイルス1型の感染実験において,mTORの阻害剤によるTLR3応答の阻害により生存率が低下した.また,アゴニスト性の抗TLR3抗体によりTLR3応答は増強され生存率は改善した.これらの結果から,TLR3-mTOR複合体2シグナルが単純ヘルペス脳炎に対する治療の標的になりうることが示唆された.
自然免疫のセンサーであるToll様受容体(Toll-like receptor:TLR)は細菌やウイルスを構成する物質を認識しそれらの侵入をふせぐ1).Toll様受容体のひとつであるTLR3は,細胞内の小胞に局在し2本鎖RNAを感知することによりI型インターフェロンやケモカインの発現を促進する.ヒトにおいて,TLR3,TLR3を制御するタンパク質,あるいは,I型インターフェロンの発現に関連するタンパク質における変異は,単純ヘルペスウイルス1型によりひき起こされる単純ヘルペス脳炎に対する感受性を上昇させる2,3).このことから,脳におけるTLR3に依存性のI型インターフェロンの発現が単純ヘルペス脳炎に対する応答に必要であることが知られていた.中枢神経系においては,ミクログリアにおけるcGAS-STING経路の活性化が単純ヘルペスウイルス1型に対する感染防御にかかわる4).ミクログリアに由来するI型インターフェロンは,アストロサイトにおけるTLR3の発現を誘導して単純ヘルペスウイルス1型に対する応答を促進する.単純ヘルペスウイルス1型はニューロンに感染するが,ニューロンにおけるTLR3の発現や単純ヘルペスウイルス1型に対する応答については十分に理解されていなかった.生体におけるヘルペスウイルスに対する防御機構を理解するうえで,ヘルペスウイルスに対しTLR3が応答する細胞の解明や,TLR3をとおしたI型インターフェロンの発現シグナルの詳細な制御機構の解明は重要な課題である.
これまでに,Toll様受容体の細胞内輸送はI型インターフェロンシグナルの活性化に重要であることが報告されている.CD11aの活性化に依存するTLR7の輸送やAP-3依存性のTLR9の輸送は,シグナルタンパク質との相互作用を促進することによりI型インターフェロンの発現を制御する5,6).しかし,TLR3の輸送についてはほとんど知られていなかった.また,Toll様受容体によるI型インターフェロンの発現の誘導においては,代謝のセンサーであるmTORの活性も重要である.細胞の代謝,増殖,活性化をつかさどるmTORは,2つの複合体,mTOR複合体1およびmTOR複合体2の構成タンパク質である7).mTOR複合体1は栄養素を感知し,翻訳,核酸および脂質の合成,リソソームの生合成およびオートファジーに影響を及ぼす.mTOR複合体2はPI3Kの下流において活性化され,細胞骨格のリモデリング,増殖および生存を制御する.mTOR複合体1はToll様受容体の応答におけるI型インターフェロンの発現の誘導に必要であることが報告されている8).一方,Toll様受容体の応答におけるmTOR複合体2の役割については不明であった.
この研究において,筆者らは,単純ヘルペスウイルス1型の感染におけるmTOR複合体2によるTLR3応答の制御機構を明らかにした.さらに,TLR3応答の増強が単純ヘルペス脳炎の治療の標的になりうることが示された.
TLR3ノックアウトマウスを用いた単純ヘルペスウイルス1型の感染実験において,野生型のマウスと比べTLR3ノックアウトマウスは生存率が低下した.また,TLR3ノックアウトマウスにおいては野生型のマウスと比べ脳におけるウイルスの力価が高く,感染により発現するI型インターフェロンの量も少なかったことから,ヒトと同じく,マウスにおいてもTLR3応答が単純ヘルペス脳炎に対する抵抗性に重要であることが示された.
中枢神経系における単純ヘルペスウイルス1型に対する応答について検証した.マウスの大脳皮質から得たニューロンにおいて,抗TLR3抗体を用いてTLR3の発現が検出された.TLR3のリガンドであるpoly(I:C) は,単純ヘルペス脳炎において白血球の遊走に必須のケモカインであるCCL5,および,I型インターフェロンであるインターフェロンβの発現を誘導した.一方,cGAS-STING経路のリガンドであるcGAMPあるいはISDはCCL5およびインターフェロンβの発現を誘導しなかったことから,ニューロンにおいてcGAS-STING経路は機能しないことがわかった.単純ヘルペスウイルス1型の感染におけるインターフェロンβの発現はTLR3に依存していたことから,TLR3がニューロンにおいて単純ヘルペスウイルス1型の主要なセンサーとしてはたらくことが強く示唆された.同様に,大脳皮質から得たミクログリアおよびアストロサイトにおけるTLR3の発現は,ニューロンよりもはるかに高かった.アストロサイトにおいてはTLR3のリガンドあるいはcGAS-STING経路のリガンドによる刺激に依存してCCL5が発現した.単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現は,TLR3を欠損したアストロサイトおよびSTINGを欠損したアストロサイトにおいて低下した.これらの結果から,TLR3応答およびcGAS-STING経路の両方が,アストロサイトにおいて単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現に必要であることが示唆された.
一方,ミクログリアにおける単純ヘルペスウイルス1型に依存的なCCL5およびインターフェロンβの発現は,STINGを欠損したミクログリアにおいては消失したが,TLR3を欠損したミクログリアにおいては消失しなかった.これらの結果から,これまでの報告と同様,アストロサイトやニューロンとは対照的に,cGAS-STING経路がミクログリアにおける単純ヘルペスウイルス1型のセンサーであることが示唆された.TLR3ノックアウトマウスを用いた単純ヘルペスウイルス1型の感染実験の結果とあわせて,ミクログリアにおけるcGAS-STING経路だけでなく,ニューロンやアストロサイトにおけるTLR3応答が単純ヘルペスウイルス1型に対する感染防御に重要であることが示された.
Toll様受容体とmTORとの関連性について,2つのmTOR阻害剤を使用することにより検証した.ラパマイシンはmTOR複合体1のみを阻害し,Torin1はmTOR複合体1およびmTOR複合体2の両方を阻害する.ニューロンおよびアストロサイトにおいて,TLR3のリガンドの刺激に依存的なCCL5の発現はTorin1により阻害されたが,ラパマイシンによっては阻害されなかった.これらの結果から,ニューロンおよびアストロサイトにおいて,TLR3に依存的なCCL5の発現のシグナル伝達に,mTOR複合体1は不要であるがmTOR複合体2は必須であることが示された.
TLR3およびTLR3を制御するタンパク質であるUnc93B1を強制発現させたNIH3T3細胞およびマウス胎仔線維芽細胞を用いて,TLR3応答におけるmTOR複合体1およびmTOR複合体2の役割についてさらに解析した.下流のシグナル伝達経路の生化学的な解析により,mTOR複合体2の下流のタンパク質であるAktやPKCの活性化がTLR3のリガンドの刺激に依存的に検出されたことから,TLR3の下流においてmTOR複合体2が活性化することが示唆された.Torin1により,これらの活性化だけでなく,CCL5の発現に必要なp65,p38,Erk1/Erk2のリン酸化も消失した.また,mTOR複合体2の構成タンパク質であるRICTORを欠損したマウス胎仔線維芽細胞において,TLR3のリガンドの刺激に依存的なCCL5の発現およびp38,p65,Aktのリン酸化が消失した.これらの結果から,TLR3応答にはmTOR複合体2の活性化が必要であることが示唆された.
インターフェロンβの発現について検討した.ニューロンおよびマウス胎仔線維芽細胞において,単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現はラパマイシンおよびTorin1により阻害された.生化学的な解析において,単純ヘルペスウイルス1型の感染は,mTOR,RICTOR,AktのようなmTOR複合体2に関連するタンパク質だけでなく,mTOR複合体1に関連するRAPTORやS6のリン酸化を促進した.RICTORを欠損したマウス胎仔線維芽細胞において単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現が低下したことから,mTOR複合体1およびmTOR複合体2の両方の活性化が単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現に必要であることが示唆された.
近接リガーゼ反応アッセイ(proximity ligation assay:PLA)や共免疫沈降実験により,TLR3はリガンドによる刺激に依存的に,mTOR,RICTOR,CCL5の発現に関連する重要なタンパク質であるTRAF6と結合することが示された.Torin1はTLR3とmTORおよびTRAF6との結合を阻害したことから,mTOR複合体2の活性化がTLR3とmTOR複合体2あるいはTRAF6とのあいだの結合に必要であることが示唆された.インターフェロンβの発現が高い単純ヘルペスウイルス1型の感染において,TLR3はmTOR,RICTOR,TRAF6にくわえ,I型インターフェロンの発現に関連する重要なタンパク質であるRAPTORやTRAF3と結合した.マウス胎仔線維芽細胞あるいはニューロンにおけるTLR3のリガンドの刺激によるインターフェロンβの発現の上昇は非常に弱く,TLR3とRAPTORあるいはTRAF3との結合ははるかに弱かった.対照的に,ミクログリアや骨髄由来マクロファージにおいてはTLR3のリガンドの刺激によるインターフェロンβの発現の上昇が強く,TLR3とRAPTORあるいはTRAF3との結合も検出された.これらの結果から,TLR3による刺激に依存性のインターフェロンβの発現は,TLR3とI型インターフェロンシグナルの発現に関連するタンパク質との結合の強弱により決定されることが示唆された.
mTOR複合体2はPKCをリン酸化してアクチンの重合などの細胞骨格のリモデリングをひき起こすことが知られている9).TLR3のリガンドの刺激によるPKCα/PKCβおよびPKCδのリン酸化はアクチンおよび微小管の重合をひき起こした.Torin1およびPKC阻害剤はこれらの変化をすべて阻害したことから,細胞骨格のリモデリングがTLR3-mTOR複合体2-PKC経路によりひき起こされることが示唆された.ほかの核酸センサーの細胞内輸送はインターフェロンβの発現と関連のあることから,細胞骨格のリモデリングがTLR3の輸送に影響し,インターフェロンβの発現に影響をおよぼしうると仮定した.TLR3はリソソームのマーカーであるLAMP-1および低分子量GTPaseであるRab7aと共局在しており,定常な状態ではTLR3は核の周囲に存在するが,TLR3のリガンドの刺激により細胞の周縁部へと輸送された.この細胞の辺縁部へのTLR3およびLAMP-1の輸送は,PKC阻害剤,Torin1,微小管の重合の阻害剤によりほとんど完全に阻害されたが,ラパマイシンではほとんど阻害されなかった.さらに,RICTORを欠損したマウス胎仔線維芽細胞においても,TLR3のリガンドの刺激に依存的なTLR3の細胞内輸送は消失した.これらの結果から,TLR3-mTOR複合体2-PKCシグナルにより微小管の重合が起こり,TLR3を含むリソソームの輸送がひき起こされることが示唆された.
Rab7aは一般的にリソソームと微小管とのあいだを媒介することが知られている10).したがって,TLR3の細胞内輸送におけるRab7aの役割について調べた.その結果,TLR3はRab7aとつねに共局在するだけでなく,TLR3とRab7aは刺激の有無にかかわらず結合することが示された.Rab7aを欠損したマウス胎仔線維芽細胞においてTLR3のリガンドの刺激に依存的なTLR3の細胞内輸送は野生型のマウス胎仔線維芽細胞と比べ有意に損なわれたことから,TLR3を含むリソソームが重合した微小管と相互作用するRab7aを介して輸送されることが示唆された.単純ヘルペスウイルス1型に感染した細胞においても同様に,単純ヘルペスウイルス1型に感染するとTLR3-mTOR複合体2-PKCシグナルにより微小管の重合を起こり,Rab7aに依存的なTLR3を含むリソソームの細胞内輸送をひき起こすことが明らかにされた.
TLR3の細胞内輸送とTLR3応答の関連性について検証を進めた.TLR3の細胞内輸送が消失するPKC阻害剤により処理したマウス胎仔線維芽細胞およびRICTORを欠損したマウス胎仔線維芽細胞において,TLR3のリガンドの刺激に依存的なCCL5の発現は変化せず,単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現は低下した.これらの結果から,TLR3の細胞内輸送が単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現に必要であることが示唆された.I型インターフェロンの発現に関連する重要なタンパク質であるTRAF3とTLR3との共局在を共焦点顕微鏡により調べたところ,TLR3はリガンドによる刺激あるいは単純ヘルペスウイルス1型への感染によりTRAF3との共局在を示した.TLR3とTRAF3の共局在は単純ヘルペスウイルス1型への感染において有意に高く結合が検出されたのに対し,TLR3のリガンドによる刺激においてTLR3とTRAF3の結合は検出されなかった.これらの結果から,単純ヘルペスウイルス1型への感染におけるTLR3の細胞内輸送により,TLR3はTRAF3およびmTOR複合体1のようなI型インターフェロンの発現に関連するタンパク質に接近し相互作用が可能になり,インターフェロンβの発現が誘導されることが示された.
ニューロンにおける内在性のTLR3の細胞内輸送について検討した.マウス胎仔線維芽細胞と同様に,ニューロンにおいてTLR3は刺激のまえには核の周囲に局在し,TLR3のリガンドによる刺激あるいは単純ヘルペスウイルス1型の感染により樹状突起にそって輸送された.このTLR3の細胞内輸送はTorin1の処理により阻害された.mTORの阻害剤であるTorin1の処理はTLR3のリガンドの刺激によるCCL5およびインターフェロンβの発現の上昇を阻害したのに対し,mTORの活性化剤である8-CPT-2Me-cAMPの処理はTLR3のリガンドの刺激によるCCL5およびインターフェロンβの発現の上昇を増強した.これらの結果から,マウス胎仔線維芽細胞と同様に,ニューロンにおけるTLR3応答においてmTOR複合体1およびmTOR複合体2が重要な役割を担うことが示唆された.
生体において単純ヘルペスウイルス1型に対する防御におけるmTORの重要性について検証した.Torin1のマウスの頭蓋内への投与は毒性を示さなかったが,中枢神経系におけるmTOR,RICTOR,および,mTORの下流のタンパク質であるAktのリン酸化を阻害した.野生型のマウスを用いた単純ヘルペスウイルス1型の感染実験において,Torin1の処理により生存率は低下,中枢神経系におけるウイルスの収量が有意に増加し,感染に依存的なCCL5およびインターフェロンβの発現の上昇は低減した.TLR3ノックアウトマウスにおいてTorin1の処理による生存率の変化はなかったことから,TLR3-mTORシグナルは中枢神経系における単純ヘルペスウイルス1型に対する感染防御に重要な役割をもつことが明らかにされた.
中枢神経系における単純ヘルペスウイルス1型に対する感染防御にTLR3-mTORシグナルが重要であることを考えると,中枢神経系におけるTLR3応答の増大は単純ヘルペス脳炎の治療に効果のある可能性がある.以前に筆者らが構築したアゴニスト性の抗TLR3モノクローナル抗体は,マクロファージにおいてTLR3応答を増強したことから11),同様の実験をニューロンにおいて実施した.その結果,この抗TLR3抗体は,ニューロンにおいてもTLR3のリガンドの刺激によるCCL5の発現の上昇,および,単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現の上昇を増強した.そこで,抗TLR3抗体を単純ヘルペスウイルス1型とともに野生型のマウスの頭蓋内に投与したところ生存率が改善された.また,抗TLR3抗体は中枢神経系におけるウイルスの収量を減少させ,単純ヘルペスウイルス1型の感染に依存的なCCL5およびインターフェロンβの発現の上昇を増強した.抗TLR3抗体はTorin1を処理したマウスおよびインターフェロンα受容体1ノックアウトマウスを救済することはできなかったことから,抗TLR3抗体はTLR3-mTOR複合体2-インターフェロンβシグナルに作用することが示唆された.これらの結果から,TLR3-mTOR複合体2シグナルが単純ヘルペスウイルス1型に対する感染防御を増強し,単純ヘルペス脳炎の治療の標的になりうることが示唆された.
この研究において,単純ヘルペスウイルス1型に対する感染防御においてニューロンにおけるTLR3応答が重要であることが示唆された(図1).また,代謝のセンサーであるmTOR複合体2がTLR3応答のマスター制御因子であることが見い出された.mTOR複合体2はリガンドにより刺激されたTLR3と結合して活性化され,CCL5の発現およびTLR3の核の周囲から細胞の辺縁部までのRab7aに依存的な輸送を促進した.TLR3の細胞内輸送はTLR3とI型インターフェロン発現に関連するタンパク質との結合を可能にすることによりI型インターフェロンの発現を促進した.したがって,mTOR複合体2はケモカインの発現,I型インターフェロンの発現,細胞内輸送といったTLR3応答のすべてを制御することが明らかにされた.マウスを用いた感染実験により,TLR3-mTOR複合体2-インターフェロンシグナルが単純ヘルペスウイルス1型に対する感染防御において重要であることが示唆された.今後は,さらに研究を発展させ,TLR3-mTORシグナルが単純ヘルペス脳炎の治療の標的として選択肢のひとつになるようにしたいと考えている.
略歴:2015年 東京大学大学院医学系研究科 修了,東京大学医科学研究所 特任研究員を経て,2018年より同 特任助教.
研究テーマ:自然免疫応答の制御機構
関心事:神経系における免疫学および代謝免疫学.
三宅 健介(Kensuke Miyake)
東京大学医科学研究所 教授.
研究室URL:http://www.ims.u-tokyo.ac.jp/kanseniden/
© 2018 佐藤亮太・三宅健介 Licensed under CC 表示 2.1 日本
(東京大学医科学研究所 感染遺伝学分野)
email:佐藤亮太,三宅健介
DOI: 10.7875/first.author.2018.098
Combating herpesvirus encephalitis by potentiating a TLR3-mTORC2 axis.
Ryota Sato, Akihisa Kato, Takahiko Chimura, Shin-Ichiroh Saitoh, Takuma Shibata, Yusuke Murakami, Ryutaro Fukui, Kaiwen Liu, Yun Zhang, Jun Arii, Ge-Hong Sun-Wada, Yoh Wada, Tsuneo Ikenoue, Glen N. Barber, Toshiya Manabe, Yasushi Kawaguchi, Kensuke Miyake
Nature Immunology, 19, 1071-1082 (2018)
要 約
Toll様受容体(Toll-like receptor:TLR)のひとつであるTLR3は,脳における単純ヘルペスウイルス1型に対する感染防御に不可欠な2本鎖RNAのセンサーである.しかし,TLR3の応答を制御する機構や脳においてTLR3が機能する細胞については不明だった.この研究において,筆者らは,TLR3がニューロンおよびアストロサイトにおける単純ヘルペスウイルス1型に対する感染防御に必要であることを明らかにした.また,単純ヘルペスウイルス1型の感染において,TLR3が代謝のセンサーであるmTOR複合体2と結合し活性化されることにより,ケモカインの発現およびTLR3の細胞の辺縁部への輸送がひき起こされた.このTLR3の細胞内輸送により,mTOR複合体1を含むI型インターフェロンの発現に関連するタンパク質の活性化が可能になった.マウスを用いた単純ヘルペスウイルス1型の感染実験において,mTORの阻害剤によるTLR3応答の阻害により生存率が低下した.また,アゴニスト性の抗TLR3抗体によりTLR3応答は増強され生存率は改善した.これらの結果から,TLR3-mTOR複合体2シグナルが単純ヘルペス脳炎に対する治療の標的になりうることが示唆された.
はじめに
自然免疫のセンサーであるToll様受容体(Toll-like receptor:TLR)は細菌やウイルスを構成する物質を認識しそれらの侵入をふせぐ1).Toll様受容体のひとつであるTLR3は,細胞内の小胞に局在し2本鎖RNAを感知することによりI型インターフェロンやケモカインの発現を促進する.ヒトにおいて,TLR3,TLR3を制御するタンパク質,あるいは,I型インターフェロンの発現に関連するタンパク質における変異は,単純ヘルペスウイルス1型によりひき起こされる単純ヘルペス脳炎に対する感受性を上昇させる2,3).このことから,脳におけるTLR3に依存性のI型インターフェロンの発現が単純ヘルペス脳炎に対する応答に必要であることが知られていた.中枢神経系においては,ミクログリアにおけるcGAS-STING経路の活性化が単純ヘルペスウイルス1型に対する感染防御にかかわる4).ミクログリアに由来するI型インターフェロンは,アストロサイトにおけるTLR3の発現を誘導して単純ヘルペスウイルス1型に対する応答を促進する.単純ヘルペスウイルス1型はニューロンに感染するが,ニューロンにおけるTLR3の発現や単純ヘルペスウイルス1型に対する応答については十分に理解されていなかった.生体におけるヘルペスウイルスに対する防御機構を理解するうえで,ヘルペスウイルスに対しTLR3が応答する細胞の解明や,TLR3をとおしたI型インターフェロンの発現シグナルの詳細な制御機構の解明は重要な課題である.
これまでに,Toll様受容体の細胞内輸送はI型インターフェロンシグナルの活性化に重要であることが報告されている.CD11aの活性化に依存するTLR7の輸送やAP-3依存性のTLR9の輸送は,シグナルタンパク質との相互作用を促進することによりI型インターフェロンの発現を制御する5,6).しかし,TLR3の輸送についてはほとんど知られていなかった.また,Toll様受容体によるI型インターフェロンの発現の誘導においては,代謝のセンサーであるmTORの活性も重要である.細胞の代謝,増殖,活性化をつかさどるmTORは,2つの複合体,mTOR複合体1およびmTOR複合体2の構成タンパク質である7).mTOR複合体1は栄養素を感知し,翻訳,核酸および脂質の合成,リソソームの生合成およびオートファジーに影響を及ぼす.mTOR複合体2はPI3Kの下流において活性化され,細胞骨格のリモデリング,増殖および生存を制御する.mTOR複合体1はToll様受容体の応答におけるI型インターフェロンの発現の誘導に必要であることが報告されている8).一方,Toll様受容体の応答におけるmTOR複合体2の役割については不明であった.
この研究において,筆者らは,単純ヘルペスウイルス1型の感染におけるmTOR複合体2によるTLR3応答の制御機構を明らかにした.さらに,TLR3応答の増強が単純ヘルペス脳炎の治療の標的になりうることが示された.
1.ニューロンにおけるTLR3応答は単純ヘルペスウイルス1型に対する感染防御に不可欠である
TLR3ノックアウトマウスを用いた単純ヘルペスウイルス1型の感染実験において,野生型のマウスと比べTLR3ノックアウトマウスは生存率が低下した.また,TLR3ノックアウトマウスにおいては野生型のマウスと比べ脳におけるウイルスの力価が高く,感染により発現するI型インターフェロンの量も少なかったことから,ヒトと同じく,マウスにおいてもTLR3応答が単純ヘルペス脳炎に対する抵抗性に重要であることが示された.
中枢神経系における単純ヘルペスウイルス1型に対する応答について検証した.マウスの大脳皮質から得たニューロンにおいて,抗TLR3抗体を用いてTLR3の発現が検出された.TLR3のリガンドであるpoly(I:C) は,単純ヘルペス脳炎において白血球の遊走に必須のケモカインであるCCL5,および,I型インターフェロンであるインターフェロンβの発現を誘導した.一方,cGAS-STING経路のリガンドであるcGAMPあるいはISDはCCL5およびインターフェロンβの発現を誘導しなかったことから,ニューロンにおいてcGAS-STING経路は機能しないことがわかった.単純ヘルペスウイルス1型の感染におけるインターフェロンβの発現はTLR3に依存していたことから,TLR3がニューロンにおいて単純ヘルペスウイルス1型の主要なセンサーとしてはたらくことが強く示唆された.同様に,大脳皮質から得たミクログリアおよびアストロサイトにおけるTLR3の発現は,ニューロンよりもはるかに高かった.アストロサイトにおいてはTLR3のリガンドあるいはcGAS-STING経路のリガンドによる刺激に依存してCCL5が発現した.単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現は,TLR3を欠損したアストロサイトおよびSTINGを欠損したアストロサイトにおいて低下した.これらの結果から,TLR3応答およびcGAS-STING経路の両方が,アストロサイトにおいて単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現に必要であることが示唆された.
一方,ミクログリアにおける単純ヘルペスウイルス1型に依存的なCCL5およびインターフェロンβの発現は,STINGを欠損したミクログリアにおいては消失したが,TLR3を欠損したミクログリアにおいては消失しなかった.これらの結果から,これまでの報告と同様,アストロサイトやニューロンとは対照的に,cGAS-STING経路がミクログリアにおける単純ヘルペスウイルス1型のセンサーであることが示唆された.TLR3ノックアウトマウスを用いた単純ヘルペスウイルス1型の感染実験の結果とあわせて,ミクログリアにおけるcGAS-STING経路だけでなく,ニューロンやアストロサイトにおけるTLR3応答が単純ヘルペスウイルス1型に対する感染防御に重要であることが示された.
2.mTORシグナルの活性化はTLR3応答に必要である
Toll様受容体とmTORとの関連性について,2つのmTOR阻害剤を使用することにより検証した.ラパマイシンはmTOR複合体1のみを阻害し,Torin1はmTOR複合体1およびmTOR複合体2の両方を阻害する.ニューロンおよびアストロサイトにおいて,TLR3のリガンドの刺激に依存的なCCL5の発現はTorin1により阻害されたが,ラパマイシンによっては阻害されなかった.これらの結果から,ニューロンおよびアストロサイトにおいて,TLR3に依存的なCCL5の発現のシグナル伝達に,mTOR複合体1は不要であるがmTOR複合体2は必須であることが示された.
TLR3およびTLR3を制御するタンパク質であるUnc93B1を強制発現させたNIH3T3細胞およびマウス胎仔線維芽細胞を用いて,TLR3応答におけるmTOR複合体1およびmTOR複合体2の役割についてさらに解析した.下流のシグナル伝達経路の生化学的な解析により,mTOR複合体2の下流のタンパク質であるAktやPKCの活性化がTLR3のリガンドの刺激に依存的に検出されたことから,TLR3の下流においてmTOR複合体2が活性化することが示唆された.Torin1により,これらの活性化だけでなく,CCL5の発現に必要なp65,p38,Erk1/Erk2のリン酸化も消失した.また,mTOR複合体2の構成タンパク質であるRICTORを欠損したマウス胎仔線維芽細胞において,TLR3のリガンドの刺激に依存的なCCL5の発現およびp38,p65,Aktのリン酸化が消失した.これらの結果から,TLR3応答にはmTOR複合体2の活性化が必要であることが示唆された.
インターフェロンβの発現について検討した.ニューロンおよびマウス胎仔線維芽細胞において,単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現はラパマイシンおよびTorin1により阻害された.生化学的な解析において,単純ヘルペスウイルス1型の感染は,mTOR,RICTOR,AktのようなmTOR複合体2に関連するタンパク質だけでなく,mTOR複合体1に関連するRAPTORやS6のリン酸化を促進した.RICTORを欠損したマウス胎仔線維芽細胞において単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現が低下したことから,mTOR複合体1およびmTOR複合体2の両方の活性化が単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現に必要であることが示唆された.
近接リガーゼ反応アッセイ(proximity ligation assay:PLA)や共免疫沈降実験により,TLR3はリガンドによる刺激に依存的に,mTOR,RICTOR,CCL5の発現に関連する重要なタンパク質であるTRAF6と結合することが示された.Torin1はTLR3とmTORおよびTRAF6との結合を阻害したことから,mTOR複合体2の活性化がTLR3とmTOR複合体2あるいはTRAF6とのあいだの結合に必要であることが示唆された.インターフェロンβの発現が高い単純ヘルペスウイルス1型の感染において,TLR3はmTOR,RICTOR,TRAF6にくわえ,I型インターフェロンの発現に関連する重要なタンパク質であるRAPTORやTRAF3と結合した.マウス胎仔線維芽細胞あるいはニューロンにおけるTLR3のリガンドの刺激によるインターフェロンβの発現の上昇は非常に弱く,TLR3とRAPTORあるいはTRAF3との結合ははるかに弱かった.対照的に,ミクログリアや骨髄由来マクロファージにおいてはTLR3のリガンドの刺激によるインターフェロンβの発現の上昇が強く,TLR3とRAPTORあるいはTRAF3との結合も検出された.これらの結果から,TLR3による刺激に依存性のインターフェロンβの発現は,TLR3とI型インターフェロンシグナルの発現に関連するタンパク質との結合の強弱により決定されることが示唆された.
3.インターフェロンβの発現はmTOR複合体2-PKC経路に依存的なTLR3の細胞内輸送に依存する
mTOR複合体2はPKCをリン酸化してアクチンの重合などの細胞骨格のリモデリングをひき起こすことが知られている9).TLR3のリガンドの刺激によるPKCα/PKCβおよびPKCδのリン酸化はアクチンおよび微小管の重合をひき起こした.Torin1およびPKC阻害剤はこれらの変化をすべて阻害したことから,細胞骨格のリモデリングがTLR3-mTOR複合体2-PKC経路によりひき起こされることが示唆された.ほかの核酸センサーの細胞内輸送はインターフェロンβの発現と関連のあることから,細胞骨格のリモデリングがTLR3の輸送に影響し,インターフェロンβの発現に影響をおよぼしうると仮定した.TLR3はリソソームのマーカーであるLAMP-1および低分子量GTPaseであるRab7aと共局在しており,定常な状態ではTLR3は核の周囲に存在するが,TLR3のリガンドの刺激により細胞の周縁部へと輸送された.この細胞の辺縁部へのTLR3およびLAMP-1の輸送は,PKC阻害剤,Torin1,微小管の重合の阻害剤によりほとんど完全に阻害されたが,ラパマイシンではほとんど阻害されなかった.さらに,RICTORを欠損したマウス胎仔線維芽細胞においても,TLR3のリガンドの刺激に依存的なTLR3の細胞内輸送は消失した.これらの結果から,TLR3-mTOR複合体2-PKCシグナルにより微小管の重合が起こり,TLR3を含むリソソームの輸送がひき起こされることが示唆された.
Rab7aは一般的にリソソームと微小管とのあいだを媒介することが知られている10).したがって,TLR3の細胞内輸送におけるRab7aの役割について調べた.その結果,TLR3はRab7aとつねに共局在するだけでなく,TLR3とRab7aは刺激の有無にかかわらず結合することが示された.Rab7aを欠損したマウス胎仔線維芽細胞においてTLR3のリガンドの刺激に依存的なTLR3の細胞内輸送は野生型のマウス胎仔線維芽細胞と比べ有意に損なわれたことから,TLR3を含むリソソームが重合した微小管と相互作用するRab7aを介して輸送されることが示唆された.単純ヘルペスウイルス1型に感染した細胞においても同様に,単純ヘルペスウイルス1型に感染するとTLR3-mTOR複合体2-PKCシグナルにより微小管の重合を起こり,Rab7aに依存的なTLR3を含むリソソームの細胞内輸送をひき起こすことが明らかにされた.
TLR3の細胞内輸送とTLR3応答の関連性について検証を進めた.TLR3の細胞内輸送が消失するPKC阻害剤により処理したマウス胎仔線維芽細胞およびRICTORを欠損したマウス胎仔線維芽細胞において,TLR3のリガンドの刺激に依存的なCCL5の発現は変化せず,単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現は低下した.これらの結果から,TLR3の細胞内輸送が単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現に必要であることが示唆された.I型インターフェロンの発現に関連する重要なタンパク質であるTRAF3とTLR3との共局在を共焦点顕微鏡により調べたところ,TLR3はリガンドによる刺激あるいは単純ヘルペスウイルス1型への感染によりTRAF3との共局在を示した.TLR3とTRAF3の共局在は単純ヘルペスウイルス1型への感染において有意に高く結合が検出されたのに対し,TLR3のリガンドによる刺激においてTLR3とTRAF3の結合は検出されなかった.これらの結果から,単純ヘルペスウイルス1型への感染におけるTLR3の細胞内輸送により,TLR3はTRAF3およびmTOR複合体1のようなI型インターフェロンの発現に関連するタンパク質に接近し相互作用が可能になり,インターフェロンβの発現が誘導されることが示された.
4.TLR3-mTORシグナルは単純ヘルペスウイルス1型に対する感染防御にはたらく
ニューロンにおける内在性のTLR3の細胞内輸送について検討した.マウス胎仔線維芽細胞と同様に,ニューロンにおいてTLR3は刺激のまえには核の周囲に局在し,TLR3のリガンドによる刺激あるいは単純ヘルペスウイルス1型の感染により樹状突起にそって輸送された.このTLR3の細胞内輸送はTorin1の処理により阻害された.mTORの阻害剤であるTorin1の処理はTLR3のリガンドの刺激によるCCL5およびインターフェロンβの発現の上昇を阻害したのに対し,mTORの活性化剤である8-CPT-2Me-cAMPの処理はTLR3のリガンドの刺激によるCCL5およびインターフェロンβの発現の上昇を増強した.これらの結果から,マウス胎仔線維芽細胞と同様に,ニューロンにおけるTLR3応答においてmTOR複合体1およびmTOR複合体2が重要な役割を担うことが示唆された.
生体において単純ヘルペスウイルス1型に対する防御におけるmTORの重要性について検証した.Torin1のマウスの頭蓋内への投与は毒性を示さなかったが,中枢神経系におけるmTOR,RICTOR,および,mTORの下流のタンパク質であるAktのリン酸化を阻害した.野生型のマウスを用いた単純ヘルペスウイルス1型の感染実験において,Torin1の処理により生存率は低下,中枢神経系におけるウイルスの収量が有意に増加し,感染に依存的なCCL5およびインターフェロンβの発現の上昇は低減した.TLR3ノックアウトマウスにおいてTorin1の処理による生存率の変化はなかったことから,TLR3-mTORシグナルは中枢神経系における単純ヘルペスウイルス1型に対する感染防御に重要な役割をもつことが明らかにされた.
5.抗TLR抗体によるTLR3応答の増強は単純ヘルペス脳炎に対する抵抗性を示す
中枢神経系における単純ヘルペスウイルス1型に対する感染防御にTLR3-mTORシグナルが重要であることを考えると,中枢神経系におけるTLR3応答の増大は単純ヘルペス脳炎の治療に効果のある可能性がある.以前に筆者らが構築したアゴニスト性の抗TLR3モノクローナル抗体は,マクロファージにおいてTLR3応答を増強したことから11),同様の実験をニューロンにおいて実施した.その結果,この抗TLR3抗体は,ニューロンにおいてもTLR3のリガンドの刺激によるCCL5の発現の上昇,および,単純ヘルペスウイルス1型の感染に依存的なインターフェロンβの発現の上昇を増強した.そこで,抗TLR3抗体を単純ヘルペスウイルス1型とともに野生型のマウスの頭蓋内に投与したところ生存率が改善された.また,抗TLR3抗体は中枢神経系におけるウイルスの収量を減少させ,単純ヘルペスウイルス1型の感染に依存的なCCL5およびインターフェロンβの発現の上昇を増強した.抗TLR3抗体はTorin1を処理したマウスおよびインターフェロンα受容体1ノックアウトマウスを救済することはできなかったことから,抗TLR3抗体はTLR3-mTOR複合体2-インターフェロンβシグナルに作用することが示唆された.これらの結果から,TLR3-mTOR複合体2シグナルが単純ヘルペスウイルス1型に対する感染防御を増強し,単純ヘルペス脳炎の治療の標的になりうることが示唆された.
おわりに
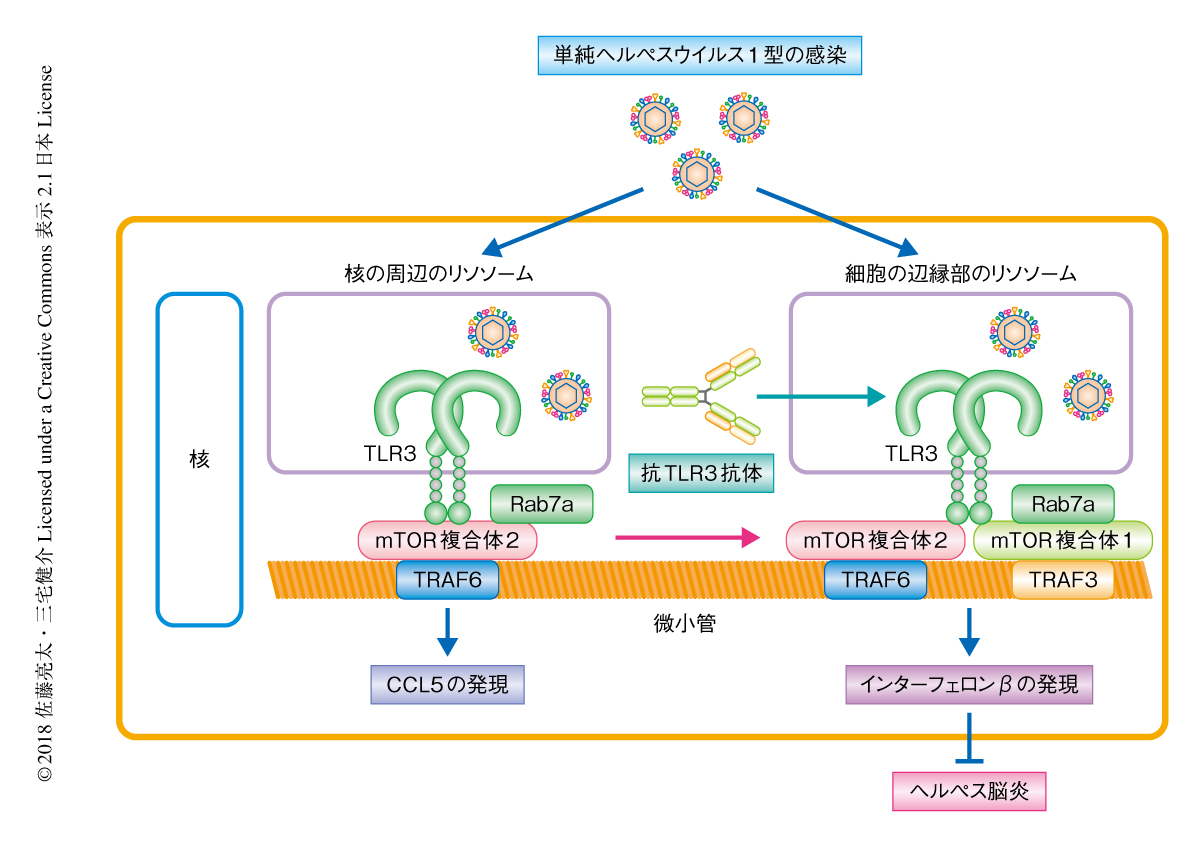
この研究において,単純ヘルペスウイルス1型に対する感染防御においてニューロンにおけるTLR3応答が重要であることが示唆された(図1).また,代謝のセンサーであるmTOR複合体2がTLR3応答のマスター制御因子であることが見い出された.mTOR複合体2はリガンドにより刺激されたTLR3と結合して活性化され,CCL5の発現およびTLR3の核の周囲から細胞の辺縁部までのRab7aに依存的な輸送を促進した.TLR3の細胞内輸送はTLR3とI型インターフェロン発現に関連するタンパク質との結合を可能にすることによりI型インターフェロンの発現を促進した.したがって,mTOR複合体2はケモカインの発現,I型インターフェロンの発現,細胞内輸送といったTLR3応答のすべてを制御することが明らかにされた.マウスを用いた感染実験により,TLR3-mTOR複合体2-インターフェロンシグナルが単純ヘルペスウイルス1型に対する感染防御において重要であることが示唆された.今後は,さらに研究を発展させ,TLR3-mTORシグナルが単純ヘルペス脳炎の治療の標的として選択肢のひとつになるようにしたいと考えている.
文 献
- Kawai, T. & Akira, S.: The role of pattern-recognition receptors in innate immunity: update on Toll-like receptors. Nat. Immunol., 11, 373-384 (2010)[PubMed]
- Zhang, S. Y., Jouanguy, E., Sancho-Shimizu, V. et al.: Human Toll-like receptor-dependent induction of interferons in protective immunity to viruses. Immunol. Rev., 220, 225-236 (2007)[PubMed]
- Zhang, S. Y. & Casanova, J. L.: Inborn errors underlying herpes simplex encephalitis: from TLR3 to IRF3. J. Exp. Med., 212, 1342 (2015)[PubMed]
- Reinert, L. S., Lopusna, K., Winther, H. et al.: Sensing of HSV-1 by the cGAS-STING pathway in microglia orchestrates antiviral defence in the CNS. Nat. Commun., 7, 13348 (2016)[PubMed]
- Saitoh, S. I., Abe, F., Kanno, A. et al.: TLR7 mediated viral recognition results in focal type I interferon secretion by dendritic cells. Nat. Commun., 8, 1592 (2017)[PubMed]
- Sasai, M., Linehan, M. M. & Iwasaki, A.: Bifurcation of Toll-like receptor 9 signaling by adaptor protein 3. Science, 329, 1530-1534 (2010)[PubMed] [新着論文レビュー]
- Saxton, R. A. & Sabatini, D. M.: mTOR signaling in growth, metabolism, and disease. Cell, 168, 960-976 (2017)[PubMed]
- Cao, W., Manicassamy, S., Tang, H. et al.: Toll-like receptor-mediated induction of type I interferon in plasmacytoid dendritic cells requires the rapamycin-sensitive PI(3)K-mTOR-p70S6K pathway. Nat. Immunol., 9, 1157-1164 (2008)[PubMed]
- Gan, X., Wang. J., Wang, C. et al.: PRR5L degradation promotes mTORC2-mediated PKC1-δ phosphorylation and cell migration downstream of Gα12. Nat. Cell Biol., 14, 686-696 (2012)[PubMed]
- Pankiv, S., Alemu, E. A., Brech, A. et al.: FYCO1 is a Rab7 effector that binds to LC3 and PI3P to mediate microtubule plus end-directed vesicle transport. J. Cell Biol., 188, 253-269 (2010)[PubMed]
- Murakami, Y., Fukui, R., Motoi, Y. et al.: Roles of the cleaved N-terminal TLR3 fragment and cell surface TLR3 in double-stranded RNA sensing. J. Immunol., 193, 5208-5217 (2014)[PubMed]
活用したデータベースにかかわるキーワードと統合TVへのリンク
著者プロフィール
略歴:2015年 東京大学大学院医学系研究科 修了,東京大学医科学研究所 特任研究員を経て,2018年より同 特任助教.
研究テーマ:自然免疫応答の制御機構
関心事:神経系における免疫学および代謝免疫学.
三宅 健介(Kensuke Miyake)
東京大学医科学研究所 教授.
研究室URL:http://www.ims.u-tokyo.ac.jp/kanseniden/
© 2018 佐藤亮太・三宅健介 Licensed under CC 表示 2.1 日本