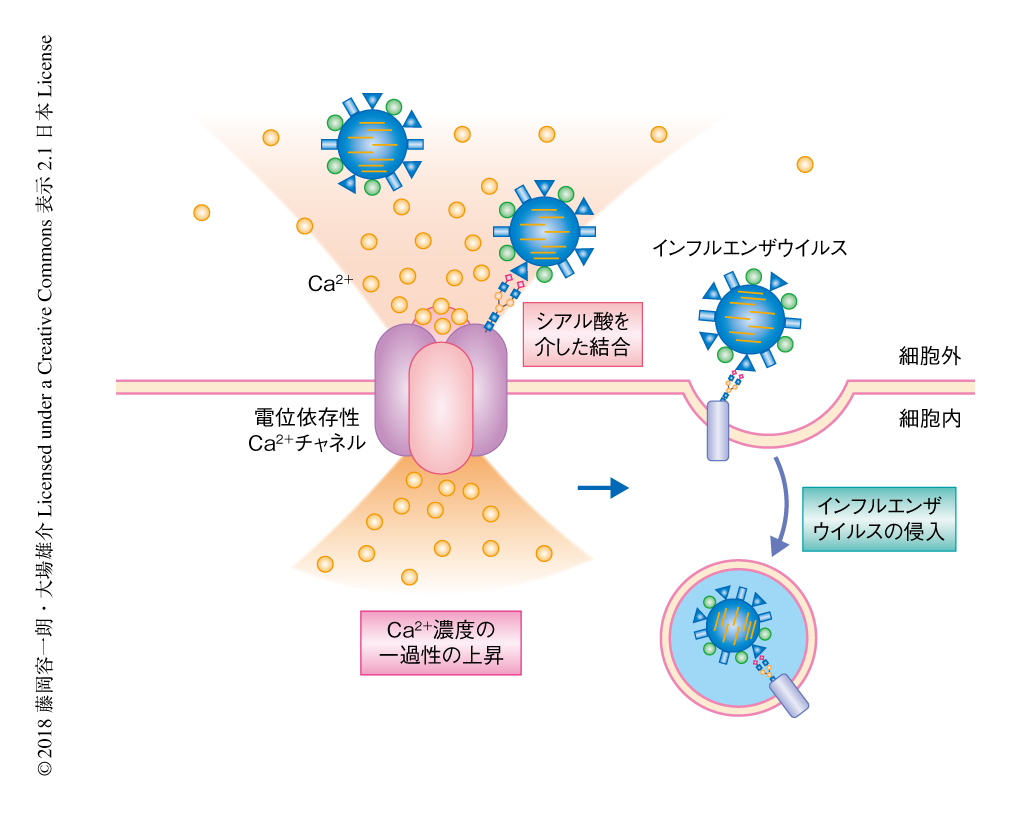
インフルエンザウイルスはHAタンパク質とシアル酸により修飾された電位依存性Ca2+チャネルとの結合を介して宿主細胞に侵入する
藤岡容一朗・大場雄介
(北海道大学大学院医学研究院 細胞生理学教室)
email:藤岡容一朗,大場雄介
DOI: 10.7875/first.author.2018.059
A sialylated voltage-dependent Ca2+ channel binds hemagglutinin and mediates influenza A virus entry into mammalian cells.
Yoichiro Fujioka, Shinya Nishide, Toyoyuki Ose, Tadaki Suzuki, Izumi Kato, Hideo Fukuhara, Mari Fujioka, Kosui Horiuchi, Aya O. Satoh, Prabha Nepal, Sayaka Kashiwagi, Jing Wang, Mika Horiguchi, Yuko Sato, Sarad Paudel, Asuka Nanbo, Tadaaki Miyazaki, Hideki Hasegawa, Katsumi Maenaka, Yusuke Ohba
Cell Host & Microbe, 23, 775-785.e5 (2018)
A型インフルエンザウイルスの宿主細胞への侵入はウイルスの表層にあるHAタンパク質と宿主細胞の表面にあるシアル酸との結合からはじまる.しかし,その鍵となるシアル酸により修飾された受容体タンパク質はいまだ同定されていない.この研究において,筆者らは,電位依存性Ca2+チャネルのひとつCav1.2がその鍵となるタンパク質であることを発見した.また,HAタンパク質とCav1.2との結合による細胞内Ca2+濃度の上昇を介してインフルエンザウイルスの宿主細胞への侵入および感染は促進されることが見い出された.Ca2+チャネル阻害薬はin vitro,in vivo,ex vivoにおいてインフルエンザウイルスの感染を抑制し,Cav1.2のノックダウンによりin vitroにおいてインフルエンザウイルスの侵入および感染は抑制された.さらに,Cav1.2のノックダウンにより抑制されたインフルエンザウイルスの感染は,野生型のCav1.2の発現により回復したが,シアル酸により修飾されない変異型のCav1.2の発現では回復は認められなかった.以上から,シアル酸により修飾された電位依存性Ca2+チャネルCav1.2がインフルエンザウイルスの宿主細胞への侵入において鍵となる受容体タンパク質であることが明らかにされた.
インフルエンザは季節的な流行をくり返し,ときにパンデミックをひき起こす1).A型インフルエンザウイルスは表層にあるHAタンパク質と宿主細胞の表面にあるシアル酸により修飾されたタンパク質との結合を介して吸着し,エンドサイトーシスにより宿主細胞へと取り込まれる.宿主細胞に取り込まれたインフルエンザウイルスは初期エンドソームをへて後期エンドソームへと移行し,pHの低下に依存したエンドソーム膜との膜融合によりウイルスRNAを宿主細胞へと放出する.宿主細胞の核において複製されたウイルスRNAと細胞質において合成されたウイルスタンパク質が細胞膜の近傍において集積すると,細胞膜から出芽してエンベロープにおおわれたインフルエンザウイルスが細胞外で再構成される.しかし,再構成されたインフルエンザウイルスは細胞膜にあるシアル酸により修飾されたタンパク質と結合し細胞膜に係留された状態でとどまる.インフルエンザウイルスが宿主細胞から遊離するためには,ウイルスのもつノイラミニダーゼによりその結合を切断することが必要である.タミフルやリレンザなどの既存の抗インフルエンザ薬はノイラミニダーゼの活性を抑制することによりインフルエンザウイルスの遊離を抑制するのが作用機序である.
インフルエンザウイルスがシアル酸と結合することが報告されてから60年近く,エンドサイトーシスにより宿主細胞に取り込まれることが見い出されてから40年以上が経過した現在においても2,3),インフルエンザウイルスの宿主細胞への侵入の機構の全貌は解明されておらず,とくに,鍵となる受容体タンパク質は同定されていない.筆者らの研究グループは,インフルエンザウイルスは宿主細胞に吸着すると細胞内Ca2+濃度の一過性の上昇をひき起こし,それにともない生じるエンドサイトーシスにより宿主細胞に取り込まれることを報告した4).さらに,Ca2+濃度の一過性の上昇およびインフルエンザウイルスの感染には細胞外から細胞内へのCa2+の流入が重要であることも示唆された.そこで,細胞膜に局在する電位依存性Ca2+チャネルがインフルエンザウイルスの感染による細胞内Ca2+濃度の一過性の上昇に関与するのではないかと考えた.
Ca2+チャネルがインフルエンザウイルスの感染の過程に関与するかどうかを検討するため,Ca2+チャネル阻害薬の効果について評価した.イヌの腎臓尿細管上皮細胞に由来するMDCK細胞に既知のCa2+チャネル阻害薬であるアムロジピン,ベラパミル,ジルチアゼムを処理したところ,いずれもインフルエンザウイルスの感染を抑制した.また,ほかの細胞株においても同様の感染の抑制が認められた.
この3種類のCa2+チャネル阻害薬のうち,ジルチアゼムの効果がもっとも高かったことから,ジルチアゼムがインフルエンザウイルスの感染に依存的な細胞内Ca2+濃度の一過性の上昇を抑制するかどうか検討した.FRETを利用したCa2+センサーであるCameleon 5) を用いてCos-1細胞において細胞内Ca2+濃度を測定したところ,Ca2+チャネル阻害薬の非存在下においてみられたインフルエンザウイルスの感染に依存した細胞内Ca2+濃度の上昇が,Ca2+チャネル阻害薬の存在下においてほぼ完全に消失した.また,インフルエンザウイルスの宿主細胞への侵入について評価するため,宿主細胞に取り込まれたのち後期エンドソームに存在するインフルエンザウイルスを定量した.インフルエンザウイルスに感染させたCos-1細胞を1時間後に固定し,インフルエンザウイルスおよび後期エンドソームをそれぞれ蛍光免疫染色法により可視化し,後期エンドソームに存在するインフルエンザウイルスを定量したところ,Ca2+チャネル阻害薬の非存在下においては後期エンドソームに存在するインフルエンザウイルスが多く認められたのに対し,Ca2+チャネル阻害薬の存在下においては後期エンドソームに存在するインフルエンザウイルスが約60%減少した.以上の結果から,Ca2+チャネル阻害薬はインフルエンザウイルスの感染に依存的な細胞内Ca2+濃度の上昇,インフルエンザウイルスの侵入および感染を抑制することが示された.
電位依存性Ca2+チャネルにはいくつかのファミリーが存在する.なかでも,L型Ca2+チャネルは呼吸上皮組織を含むヒトの組織において普遍的に発現することが知られている6).いくつかの細胞株においてL型Ca2+チャネルであるCav1.1~Cav1.4をコードするmRNAのコピー数を調べたところ,Cav1.2をコードするmRNAがもっとも多かったことからCav1.2に注目した.siRNA法によりCav1.2をノックダウンしたところ,インフルエンザウイルスの感染に依存した細胞内Ca2+濃度の上昇が抑制された.また,Cav1.2のノックダウンによりインフルエンザウイルスの宿主細胞への侵入および感染が抑制された.以上の結果から,Ca2+チャネル阻害薬によるインフルエンザウイルスの感染の抑制は,Ca2+チャネル以外に対するオフターゲット効果によるものではなく,電位依存性Ca2+チャネル(とくに,Cav1.2)を抑制したためであることが示された.
インフルエンザウイルスはどのようにしてCav1.2を介して細胞内Ca2+濃度を上昇させるのだろうか? Cos-1細胞において細胞内Ca2+濃度をモニターしつつ蛍光色素により標識したインフルエンザウイルスを感染させたところ,インフルエンザウイルスが吸着した付近でCa2+濃度の小規模な上昇が生じ,それにひきつづいて細胞の全体においてCa2+濃度の上昇が起こることが観察された.このことから,インフルエンザウイルスが宿主細胞のCav1.2と直接的に結合しCa2+の小規模な流入をひき起こしているのではないかと考えた.そこで,メンブレンバインディングアッセイ7) によりインフルエンザウイルスとCav1.2との相互作用について調べた.精製したCa2+チャネルを含む細胞膜の画分をあらかじめCav1.2に対する抗体をコートしたプレートに添加してCav1.2を固定し,そこにインフルエンザウイルスを添加し吸着したインフルエンザウイルスをウェスタンブロット法により検出した.その結果,インフルエンザウイルスの吸着は全長のCav1.2の発現により亢進し,シアル酸を分解する酵素の処理により部分的に減弱した.これらのことから,これまでの報告どおり,インフルエンザウイルスはシアル酸により修飾されたCav1.2を介して宿主細胞と結合すると考えられた.一方,Ca2+キレートの処理によりインフルエンザウイルスの吸着に変化はなかったことから,Ca2+はインフルエンザウイルスと宿主細胞との結合には関与しないことが示された.
さきの結果から,インフルエンザウイルスの表面に存在するシアル酸結合タンパク質であるHAタンパク質と,宿主細胞の細胞膜に存在するCav1.2との相互作用が示唆された.そこで,HAタンパク質とCav1.2との相互作用を免疫沈降法により検証したところ共沈降が確認された.さらに,Cav1.2のC末端側の領域がHAタンパク質と相互作用することが明らかにされた.Cav1.2のC末端側の領域にはシアル酸により修飾される2つのAsnのあることが報告されている8).そこで,このAsnをGlnに置換したシアル酸により修飾されない変異型のCav1.2を作製してHAタンパク質との相互作用について検証したところ,予想どおり,相互作用は野生型のCav1.2と比べ減弱した.さらに,Cav1.2のノックダウンにより抑制された細胞内Ca2+濃度の上昇およびインフルエンザウイルスの感染は,野生型のCav1.2を発現させることにより対照のレベルにまで回復したが,シアル酸により修飾されない変異型のCav1.2の発現では回復は認められなかった.以上の結果から,シアル酸を介したCav1.2とHAタンパク質との相互作用が,インフルエンザウイルスによる細胞内Ca2+濃度の上昇および感染に重要であることが示された.
生体におけるCa2+チャネル阻害薬によるインフルエンザウイルスの感染の抑制について検証した.まず,インフルエンザウイルスの標的である呼吸上皮組織においてCa2+チャネルが発現しているかどうかを免疫組織染色法により調べたところ,マウスの上気道である鼻腔,気管,気管支の上皮細胞,また,肺においては肺胞上皮細胞および肺胞マクロファージにCa2+チャネルの発現が認められた.さらに,それらの細胞へのインフルエンザウイルスの感染もあわせて確認された.そこで,マウスにおいてCa2+チャネル阻害薬の効果について検証した.インフルエンザウイルスが感染したのちに鼻腔において増殖したインフルエンザウイルスの量を測定したところ,Ca2+チャネル阻害薬の投与により有意に抑制された.Ca2+チャネル阻害薬の投与による効果は,予防的な投与としてインフルエンザウイルスの感染の前の投与,および,治療的な投与としてインフルエンザウイルスの感染の後の投与において,ともに認められた.また,マウスにより高い力価のインフルエンザウイルスを感染させて健康状態をモニターしたところ,Ca2+チャネル阻害薬を投与しない場合には体重がいちじるしく減少し5日目には全例が死亡したのに対し,Ca2+チャネル阻害薬を投与した場合には一過性の体重の減少ののち回復し生存期間が延長した.以上の結果から,Ca2+チャネル阻害薬によるin vivoにおけるインフルエンザウイルスの感染の抑制が認められた.
ヒトの呼吸器系におけるCa2+チャネル阻害薬によるインフルエンザウイルスの感染の抑制について検証するためex vivo実験系を用いた.気道上皮細胞株であるBEAS-2B細胞をマトリゲルを用いて3次元培養すると,条件により肺胞を模倣するスフェロイドや気道上皮組織を模倣する単層構造が形成されることが知られている9).これらの呼吸組織を模倣した3次元培養においても,Ca2+チャネル阻害薬はインフルエンザウイルスの感染を抑制した.以上から,Ca2+チャネル阻害薬は,in vitro,in vivo,ex vivoにおいてインフルエンザウイルスの感染を抑制することが示された.
この研究において,電位依存性Ca2+チャネルがインフルエンザウイルスの宿主細胞への侵入において鍵となる受容体タンパク質であることが明らかにされた(図1).そして,Ca2+チャネル阻害薬によりin vivoおよびex vivoにおいてインフルエンザウイルスの感染が抑制された.これらの成果は,ウイルスに対する既存の治療法における耐性株の出現という問題について,新たな対抗手段を提供する可能性がある.すなわち,薬剤耐性の獲得は核におけるウイルスRNAの複製の際に起こることがわかっているが,電位依存性Ca2+チャネルを標的とした治療は薬剤耐性の獲得よりもまえの過程であるウイルスの侵入の過程を抑制することから,薬剤耐性の起こりにくい新しい概念にもとづく治療法の開発につながることが期待される.
しかし,現在,処方されている高血圧治療薬としてのCa2+チャネル阻害薬(カルシウム拮抗薬)をそのままのかたちで抗ウイルス薬として使用することはむずかしい.まず,高血圧治療薬としての本来の作用,すなわち,血圧の低下が副作用として認められるのは必至である.また,経口投与では対象の臓器となる肺や気道に薬剤が分布しないという薬物動態の問題もある.これら問題点は,ドラッグデリバリー系の開発により薬剤を呼吸上皮組織に特異的に到達させることにより解決される可能性がある.一方,電位依存性Ca2+チャネルそれ自体の機能は抑制せずウイルスのHAタンパク質との相互作用のみを阻害する化合物の同定も有用であろう.これらの課題が解決されれば,薬剤耐性が起こりにくく,かつ,副作用も少ない理想的な創薬につながると期待される.
略歴:2008年 東京大学大学院総合文化研究科 修了,同年 北海道大学大学院医学研究科 博士研究員,2014年 同 特任助教を経て,2018年より北海道大学大学院医学研究院 講師.
研究テーマ:生細胞イメージング法を用いた細胞内シグナル伝達系の時空間制御の解明.
抱負:自分がおもしろいと思うだけでなく,おもしろいと思ってもらえる研究をしていきたい.
大場 雄介(Yusuke Ohba)
北海道大学大学院医学研究院 教授.
研究室URL:http://cp.med.hokudai.ac.jp
© 2018 藤岡容一朗・大場雄介 Licensed under CC 表示 2.1 日本
(北海道大学大学院医学研究院 細胞生理学教室)
email:藤岡容一朗,大場雄介
DOI: 10.7875/first.author.2018.059
A sialylated voltage-dependent Ca2+ channel binds hemagglutinin and mediates influenza A virus entry into mammalian cells.
Yoichiro Fujioka, Shinya Nishide, Toyoyuki Ose, Tadaki Suzuki, Izumi Kato, Hideo Fukuhara, Mari Fujioka, Kosui Horiuchi, Aya O. Satoh, Prabha Nepal, Sayaka Kashiwagi, Jing Wang, Mika Horiguchi, Yuko Sato, Sarad Paudel, Asuka Nanbo, Tadaaki Miyazaki, Hideki Hasegawa, Katsumi Maenaka, Yusuke Ohba
Cell Host & Microbe, 23, 775-785.e5 (2018)
この論文に出現する遺伝子・タンパク質のUniprot ID
HAタンパク質(P03451), hemagglutinin(P03451), Cav1.2(Q13936), ノイラミニダーゼ(Q1K9Q1), Cav1.1(Q13698), Cav1.4(O60840)
要 約
A型インフルエンザウイルスの宿主細胞への侵入はウイルスの表層にあるHAタンパク質と宿主細胞の表面にあるシアル酸との結合からはじまる.しかし,その鍵となるシアル酸により修飾された受容体タンパク質はいまだ同定されていない.この研究において,筆者らは,電位依存性Ca2+チャネルのひとつCav1.2がその鍵となるタンパク質であることを発見した.また,HAタンパク質とCav1.2との結合による細胞内Ca2+濃度の上昇を介してインフルエンザウイルスの宿主細胞への侵入および感染は促進されることが見い出された.Ca2+チャネル阻害薬はin vitro,in vivo,ex vivoにおいてインフルエンザウイルスの感染を抑制し,Cav1.2のノックダウンによりin vitroにおいてインフルエンザウイルスの侵入および感染は抑制された.さらに,Cav1.2のノックダウンにより抑制されたインフルエンザウイルスの感染は,野生型のCav1.2の発現により回復したが,シアル酸により修飾されない変異型のCav1.2の発現では回復は認められなかった.以上から,シアル酸により修飾された電位依存性Ca2+チャネルCav1.2がインフルエンザウイルスの宿主細胞への侵入において鍵となる受容体タンパク質であることが明らかにされた.
はじめに
インフルエンザは季節的な流行をくり返し,ときにパンデミックをひき起こす1).A型インフルエンザウイルスは表層にあるHAタンパク質と宿主細胞の表面にあるシアル酸により修飾されたタンパク質との結合を介して吸着し,エンドサイトーシスにより宿主細胞へと取り込まれる.宿主細胞に取り込まれたインフルエンザウイルスは初期エンドソームをへて後期エンドソームへと移行し,pHの低下に依存したエンドソーム膜との膜融合によりウイルスRNAを宿主細胞へと放出する.宿主細胞の核において複製されたウイルスRNAと細胞質において合成されたウイルスタンパク質が細胞膜の近傍において集積すると,細胞膜から出芽してエンベロープにおおわれたインフルエンザウイルスが細胞外で再構成される.しかし,再構成されたインフルエンザウイルスは細胞膜にあるシアル酸により修飾されたタンパク質と結合し細胞膜に係留された状態でとどまる.インフルエンザウイルスが宿主細胞から遊離するためには,ウイルスのもつノイラミニダーゼによりその結合を切断することが必要である.タミフルやリレンザなどの既存の抗インフルエンザ薬はノイラミニダーゼの活性を抑制することによりインフルエンザウイルスの遊離を抑制するのが作用機序である.
インフルエンザウイルスがシアル酸と結合することが報告されてから60年近く,エンドサイトーシスにより宿主細胞に取り込まれることが見い出されてから40年以上が経過した現在においても2,3),インフルエンザウイルスの宿主細胞への侵入の機構の全貌は解明されておらず,とくに,鍵となる受容体タンパク質は同定されていない.筆者らの研究グループは,インフルエンザウイルスは宿主細胞に吸着すると細胞内Ca2+濃度の一過性の上昇をひき起こし,それにともない生じるエンドサイトーシスにより宿主細胞に取り込まれることを報告した4).さらに,Ca2+濃度の一過性の上昇およびインフルエンザウイルスの感染には細胞外から細胞内へのCa2+の流入が重要であることも示唆された.そこで,細胞膜に局在する電位依存性Ca2+チャネルがインフルエンザウイルスの感染による細胞内Ca2+濃度の一過性の上昇に関与するのではないかと考えた.
1.Ca2+チャネル阻害薬はインフルエンザウイルスの侵入および感染を抑制する
Ca2+チャネルがインフルエンザウイルスの感染の過程に関与するかどうかを検討するため,Ca2+チャネル阻害薬の効果について評価した.イヌの腎臓尿細管上皮細胞に由来するMDCK細胞に既知のCa2+チャネル阻害薬であるアムロジピン,ベラパミル,ジルチアゼムを処理したところ,いずれもインフルエンザウイルスの感染を抑制した.また,ほかの細胞株においても同様の感染の抑制が認められた.
この3種類のCa2+チャネル阻害薬のうち,ジルチアゼムの効果がもっとも高かったことから,ジルチアゼムがインフルエンザウイルスの感染に依存的な細胞内Ca2+濃度の一過性の上昇を抑制するかどうか検討した.FRETを利用したCa2+センサーであるCameleon 5) を用いてCos-1細胞において細胞内Ca2+濃度を測定したところ,Ca2+チャネル阻害薬の非存在下においてみられたインフルエンザウイルスの感染に依存した細胞内Ca2+濃度の上昇が,Ca2+チャネル阻害薬の存在下においてほぼ完全に消失した.また,インフルエンザウイルスの宿主細胞への侵入について評価するため,宿主細胞に取り込まれたのち後期エンドソームに存在するインフルエンザウイルスを定量した.インフルエンザウイルスに感染させたCos-1細胞を1時間後に固定し,インフルエンザウイルスおよび後期エンドソームをそれぞれ蛍光免疫染色法により可視化し,後期エンドソームに存在するインフルエンザウイルスを定量したところ,Ca2+チャネル阻害薬の非存在下においては後期エンドソームに存在するインフルエンザウイルスが多く認められたのに対し,Ca2+チャネル阻害薬の存在下においては後期エンドソームに存在するインフルエンザウイルスが約60%減少した.以上の結果から,Ca2+チャネル阻害薬はインフルエンザウイルスの感染に依存的な細胞内Ca2+濃度の上昇,インフルエンザウイルスの侵入および感染を抑制することが示された.
2.電位依存性Ca2+チャネルCav1.2のノックダウンはインフルエンザウイルスの侵入および感染を抑制する
電位依存性Ca2+チャネルにはいくつかのファミリーが存在する.なかでも,L型Ca2+チャネルは呼吸上皮組織を含むヒトの組織において普遍的に発現することが知られている6).いくつかの細胞株においてL型Ca2+チャネルであるCav1.1~Cav1.4をコードするmRNAのコピー数を調べたところ,Cav1.2をコードするmRNAがもっとも多かったことからCav1.2に注目した.siRNA法によりCav1.2をノックダウンしたところ,インフルエンザウイルスの感染に依存した細胞内Ca2+濃度の上昇が抑制された.また,Cav1.2のノックダウンによりインフルエンザウイルスの宿主細胞への侵入および感染が抑制された.以上の結果から,Ca2+チャネル阻害薬によるインフルエンザウイルスの感染の抑制は,Ca2+チャネル以外に対するオフターゲット効果によるものではなく,電位依存性Ca2+チャネル(とくに,Cav1.2)を抑制したためであることが示された.
3.インフルエンザウイルスはシアル酸により修飾されたCav1.2を介して宿主細胞と結合する
インフルエンザウイルスはどのようにしてCav1.2を介して細胞内Ca2+濃度を上昇させるのだろうか? Cos-1細胞において細胞内Ca2+濃度をモニターしつつ蛍光色素により標識したインフルエンザウイルスを感染させたところ,インフルエンザウイルスが吸着した付近でCa2+濃度の小規模な上昇が生じ,それにひきつづいて細胞の全体においてCa2+濃度の上昇が起こることが観察された.このことから,インフルエンザウイルスが宿主細胞のCav1.2と直接的に結合しCa2+の小規模な流入をひき起こしているのではないかと考えた.そこで,メンブレンバインディングアッセイ7) によりインフルエンザウイルスとCav1.2との相互作用について調べた.精製したCa2+チャネルを含む細胞膜の画分をあらかじめCav1.2に対する抗体をコートしたプレートに添加してCav1.2を固定し,そこにインフルエンザウイルスを添加し吸着したインフルエンザウイルスをウェスタンブロット法により検出した.その結果,インフルエンザウイルスの吸着は全長のCav1.2の発現により亢進し,シアル酸を分解する酵素の処理により部分的に減弱した.これらのことから,これまでの報告どおり,インフルエンザウイルスはシアル酸により修飾されたCav1.2を介して宿主細胞と結合すると考えられた.一方,Ca2+キレートの処理によりインフルエンザウイルスの吸着に変化はなかったことから,Ca2+はインフルエンザウイルスと宿主細胞との結合には関与しないことが示された.
4.シアル酸を介したCav1.2とHAタンパク質との結合はインフルエンザウイルスの感染を制御する
さきの結果から,インフルエンザウイルスの表面に存在するシアル酸結合タンパク質であるHAタンパク質と,宿主細胞の細胞膜に存在するCav1.2との相互作用が示唆された.そこで,HAタンパク質とCav1.2との相互作用を免疫沈降法により検証したところ共沈降が確認された.さらに,Cav1.2のC末端側の領域がHAタンパク質と相互作用することが明らかにされた.Cav1.2のC末端側の領域にはシアル酸により修飾される2つのAsnのあることが報告されている8).そこで,このAsnをGlnに置換したシアル酸により修飾されない変異型のCav1.2を作製してHAタンパク質との相互作用について検証したところ,予想どおり,相互作用は野生型のCav1.2と比べ減弱した.さらに,Cav1.2のノックダウンにより抑制された細胞内Ca2+濃度の上昇およびインフルエンザウイルスの感染は,野生型のCav1.2を発現させることにより対照のレベルにまで回復したが,シアル酸により修飾されない変異型のCav1.2の発現では回復は認められなかった.以上の結果から,シアル酸を介したCav1.2とHAタンパク質との相互作用が,インフルエンザウイルスによる細胞内Ca2+濃度の上昇および感染に重要であることが示された.
5.Ca2+チャネル阻害薬はin vivoおよびex vivoにおいてもインフルエンザウイルスの感染を抑制する
生体におけるCa2+チャネル阻害薬によるインフルエンザウイルスの感染の抑制について検証した.まず,インフルエンザウイルスの標的である呼吸上皮組織においてCa2+チャネルが発現しているかどうかを免疫組織染色法により調べたところ,マウスの上気道である鼻腔,気管,気管支の上皮細胞,また,肺においては肺胞上皮細胞および肺胞マクロファージにCa2+チャネルの発現が認められた.さらに,それらの細胞へのインフルエンザウイルスの感染もあわせて確認された.そこで,マウスにおいてCa2+チャネル阻害薬の効果について検証した.インフルエンザウイルスが感染したのちに鼻腔において増殖したインフルエンザウイルスの量を測定したところ,Ca2+チャネル阻害薬の投与により有意に抑制された.Ca2+チャネル阻害薬の投与による効果は,予防的な投与としてインフルエンザウイルスの感染の前の投与,および,治療的な投与としてインフルエンザウイルスの感染の後の投与において,ともに認められた.また,マウスにより高い力価のインフルエンザウイルスを感染させて健康状態をモニターしたところ,Ca2+チャネル阻害薬を投与しない場合には体重がいちじるしく減少し5日目には全例が死亡したのに対し,Ca2+チャネル阻害薬を投与した場合には一過性の体重の減少ののち回復し生存期間が延長した.以上の結果から,Ca2+チャネル阻害薬によるin vivoにおけるインフルエンザウイルスの感染の抑制が認められた.
ヒトの呼吸器系におけるCa2+チャネル阻害薬によるインフルエンザウイルスの感染の抑制について検証するためex vivo実験系を用いた.気道上皮細胞株であるBEAS-2B細胞をマトリゲルを用いて3次元培養すると,条件により肺胞を模倣するスフェロイドや気道上皮組織を模倣する単層構造が形成されることが知られている9).これらの呼吸組織を模倣した3次元培養においても,Ca2+チャネル阻害薬はインフルエンザウイルスの感染を抑制した.以上から,Ca2+チャネル阻害薬は,in vitro,in vivo,ex vivoにおいてインフルエンザウイルスの感染を抑制することが示された.
おわりに
この研究において,電位依存性Ca2+チャネルがインフルエンザウイルスの宿主細胞への侵入において鍵となる受容体タンパク質であることが明らかにされた(図1).そして,Ca2+チャネル阻害薬によりin vivoおよびex vivoにおいてインフルエンザウイルスの感染が抑制された.これらの成果は,ウイルスに対する既存の治療法における耐性株の出現という問題について,新たな対抗手段を提供する可能性がある.すなわち,薬剤耐性の獲得は核におけるウイルスRNAの複製の際に起こることがわかっているが,電位依存性Ca2+チャネルを標的とした治療は薬剤耐性の獲得よりもまえの過程であるウイルスの侵入の過程を抑制することから,薬剤耐性の起こりにくい新しい概念にもとづく治療法の開発につながることが期待される.
しかし,現在,処方されている高血圧治療薬としてのCa2+チャネル阻害薬(カルシウム拮抗薬)をそのままのかたちで抗ウイルス薬として使用することはむずかしい.まず,高血圧治療薬としての本来の作用,すなわち,血圧の低下が副作用として認められるのは必至である.また,経口投与では対象の臓器となる肺や気道に薬剤が分布しないという薬物動態の問題もある.これら問題点は,ドラッグデリバリー系の開発により薬剤を呼吸上皮組織に特異的に到達させることにより解決される可能性がある.一方,電位依存性Ca2+チャネルそれ自体の機能は抑制せずウイルスのHAタンパク質との相互作用のみを阻害する化合物の同定も有用であろう.これらの課題が解決されれば,薬剤耐性が起こりにくく,かつ,副作用も少ない理想的な創薬につながると期待される.
文 献
- Herfst, S., Schrauwen, E., Linster, M. et al.: Airborne transmission of influenza A/H5N1 virus between ferrets. Science, 336, 1534-1541 (2012)[PubMed]
- Walop, J. N., Boschman, T. A. & Jacobs, J.: Affinity of N-acetylneuraminic acid for influenza virus neuraminidase. Biochim. Biophys. Acta, 44, 185-186 (1960)[PubMed]
- Matlin, K. S., Reggio, H., Helenius, A. et al.: Infectious entry pathway of influenza virus in a canine kidney cell line. J. Cell Biol., 91, 601-613 (1981)[PubMed]
- Fujioka, Y., Tsuda, M., Nanbo, A. et al.: A Ca2+-dependent signalling circuit regulates influenza A virus internalization and infection. Nat. Commun., 4, 2763 (2013)[PubMed]
- Nagai, T., Yamada, S., Tominaga, T. et al.: Expanded dynamic range of fluorescent indicators for Ca2+ by circularly permuted yellow fluorescent proteins. Proc. Natl. Acad. Sci. USA, 101, 10554-10559 (2004)[PubMed]
- Brennan, S. C., Finney, B. A., Lazarou, M. et al.: Fetal calcium regulates branching morphogenesis in the developing human and mouse lung: involvement of voltage-gated calcium channels. PLoS One, 8, e80294 (2013)[PubMed]
- Cote, M., Misasi, J., Ren, T. et al.: Small molecule inhibitors reveal Niemann-Pick C1 is essential for Ebola virus infection. Nature, 477, 344-348 (2011)[PubMed]
- Lazniewska, J. & Weiss N.: Glycosylation of voltage-gated calcium channels in health and disease. Biochim. Biophys. Acta, 1859, 662-668 (2017)[PubMed]
- Shen, Y., Hou, Y., Yao, S. et al.: In vitro epithelial organoid generation induced by substrate nanotopography. Sci. Rep., 5, 9293 (2015)[PubMed]
活用したデータベースにかかわるキーワードと統合TVへのリンク
著者プロフィール
略歴:2008年 東京大学大学院総合文化研究科 修了,同年 北海道大学大学院医学研究科 博士研究員,2014年 同 特任助教を経て,2018年より北海道大学大学院医学研究院 講師.
研究テーマ:生細胞イメージング法を用いた細胞内シグナル伝達系の時空間制御の解明.
抱負:自分がおもしろいと思うだけでなく,おもしろいと思ってもらえる研究をしていきたい.
大場 雄介(Yusuke Ohba)
北海道大学大学院医学研究院 教授.
研究室URL:http://cp.med.hokudai.ac.jp
© 2018 藤岡容一朗・大場雄介 Licensed under CC 表示 2.1 日本