転写部位の近傍において2本鎖DNA切断が生じるとENLはATMによりリン酸化されポリコーム抑制複合体1をリクルートすることにより転写を抑制する
宇井 彩子
(東北大学加齢医学研究所 加齢ゲノム制御プロテオーム研究部門)
email:宇井彩子
DOI: 10.7875/first.author.2015.063
Transcriptional elongation factor ENL phosphorylated by ATM recruits Polycomb and switches off transcription for DSB repair.
Ayako Ui, Yuko Nagaura, Akira Yasui
Molecular Cell, 58, 468-482 (2015)
ENLは転写伸長因子複合体の構成タンパク質として転写を促進することが知られている.筆者らは,ENLと相互作用するタンパク質として転写抑制能をもつポリコーム抑制複合体1の構成タンパク質であるBMI1を同定した.転写が活性化されているときにはENLはポリコーム抑制複合体1をリクルートしないが,転写部位の近傍において2本鎖DNA切断が起こるとENLはATMによりリン酸化されることによりBMI1との相互作用が増加し,ポリコーム抑制複合体1を転写部位にリクルートして転写を抑制した.さらに,この転写の抑制は2本鎖DNA切断部位においてDNA修復タンパク質のリクルートを促進したことから,ATMによる転写の抑制は転写より2本鎖DNA切断部位の修復を優先して進めるために必要である可能性が示唆された.
ATMはDNA損傷チェックポイント機構やDNA修復を制御する重要なキナーゼであるが,近年,転写も制御することが示されている1).2010年,転写部位の近傍において2本鎖DNA切断が起こると,ATMによりヒストンH2AのLys119あるいはLys120がユビキチン化され転写が抑制されることが見い出された1).当時,この転写部位に起こるヒストンH2Aのユビキチン化はATMによるヒストンγH2AXの形成に依存してリクルートされるRNF8およびRNF168によるのではないかと推測されたが,のちの研究から,RNF8およびRNF168はヒストンH2AのLys119あるいはLys120をユビキチン化する活性をもたないことが明らかにされ2),ATMがどのようにヒストンH2AのLys119あるいはLys120のユビキチン化を制御して転写を抑制しているのかは不明であった.また,2014年には,SWI/SNF複合体の構成タンパク質であるPBAFがATMによりリン酸化されヒストンH2Aのユビキチン化の促進および2本鎖DNA切断により誘導される転写の抑制に関与すること,また,ヒストンH2Aをユビキチン化する活性をもつポリコーム群タンパク質が2本鎖DNA切断により誘導される転写の抑制に関与することが示された3).しかし,クロマチンリモデリングタンパク質であるPBAFがどうやってヒストンH2Aのユビキチン化をひき起こすのか,ポリコーム群タンパク質がどうやって転写部位にリクルートされて転写の抑制に関与するのか,また,ATMとポリコーム群タンパク質がどのような関係にあるのかも不明で,ATMによる転写部位におけるヒストンH2AのLys119あるいはLys120のユビキチン化および2本鎖DNA切断により誘導される転写の抑制の制御機構については明らかではなかった.
今回,筆者らは,転写部位の近傍において2本鎖DNA切断が起こると,ATMが転写伸長因子複合体の構成タンパク質として転写を促進するENLをリン酸化し,転写抑制能をもつポリコーム抑制複合体1をリクルートしてヒストンH2AのLys119あるいはLys120をユビキチン化することにより転写伸長反応を停止する,という新しい転写抑制機構を明らかにした.また,ATMは2本鎖DNA切断の近傍において転写を抑制することより,DNA修復を転写より優先的に進めゲノムの安定性を維持している可能性のあることを明らかにした.
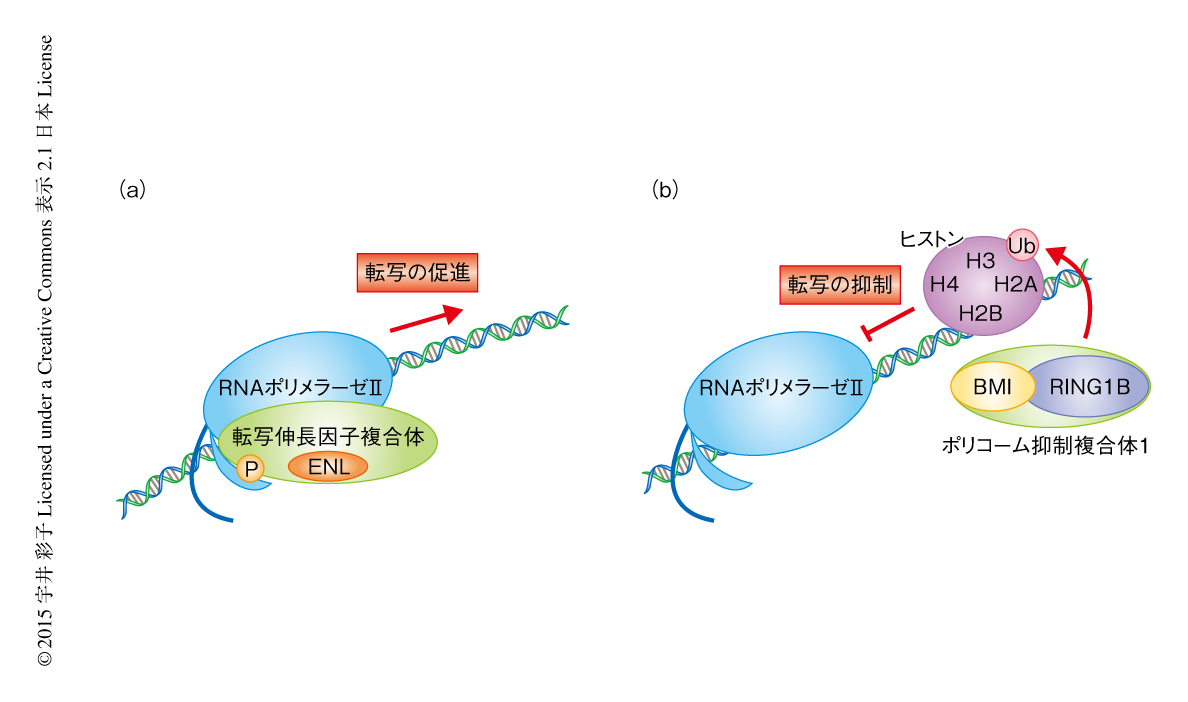
ENLと相互作用するタンパク質を検索したところ,ポリコーム抑制複合体1の構成タンパク質でありユビキチンリガーゼ複合体のサブユニットであるRING1BおよびBMI1が同定された.in vitroにおける解析により,ENLはBMI1と直接的に相互作用することが明らかにされた.ENLはRNAポリメラーゼIIのC末端ドメインのリン酸化を制御する転写伸長因子複合体(super elongation complex:SEC)の構成タンパク質であり,転写を促進することが知られている4-9)(図1a).一方で,ポリコーム抑制複合体1はヒストンH2AのLys119あるいはLys120をユビキチン化することにより転写を抑制することが知られている10)(図1b).このように,反対の機能をもつENLとポリコーム抑制複合体1について,転写の過程における挙動を調べた.その結果,ENLは転写が活性化した際には転写部位に結合し転写活性化に関与していた.一方で,ポリコーム抑制複合体1は転写部位にほとんど結合せず転写活性化には関与していなかった.このことから,ENLとポリコーム抑制複合体1は転写において異なる機能をもつと考えられた.
転写の抑制をひき起こしたときENLおよびポリコーム抑制複合体1の挙動はどう変化するのか検討した.ENLは転写の活性化とともに転写部位に結合し,転写を抑制しても変化なく転写部位に局在しつづけた.一方で,ポリコーム抑制複合体1は転写を活性化した際,また,RNAポリメラーゼIIのリン酸化の抑制により転写を抑制した際には転写部位に結合しなかったが,転写部位の近傍において2本鎖DNA切断を起こすことにより転写を抑制した際には転写部位にリクルートされた.
転写活性化の近傍において2本鎖DNA切断を起こすことにより転写を抑制した際のポリコーム抑制複合体1の転写部位へのリクルートはENLに依存するのか,また,この転写の抑制を制御することが報告されているATMに依存するのか検討した.その結果,ENLをノックダウンした細胞ではポリコーム抑制複合体1の転写部位へのリクルートは減少した.また,ATMの阻害剤を処理することによりポリコーム抑制複合体1の転写部位へのリクルートは減少した.これらの結果から,ポリコーム抑制複合体1は2本鎖DNA切断が生じた際にENLおよびATMに依存して転写部位にリクルートされることが明らかにされた.
2本鎖DNA切断が生じた際の転写部位におけるヒストンH2AのLys119あるいはLys120のユビキチン化および転写の抑制に,ENLあるいはポリコーム抑制複合体1は関与するのか検討した.その結果,ENLをノックダウンした細胞,および,ポリコーム抑制複合体1の構成タンパク質をノックダウンした細胞では,2本鎖DNA切断が生じた際の転写部位におけるヒストンH2Aのユビキチン化が減少し,転写の抑制は起こらないことが明らかにされた.
以上の結果から,ENLとポリコーム抑制複合体1との結合はATMにより制御されており,ENLがポリコーム抑制複合体1を転写部位にリクルートすることにより転写を抑制するのではないかと推測した.そこで,ENLおよびBMI1においてATMによるリン酸化部位を検索したところ,ENLにATMによるリン酸化部位が見い出された.放射線を照射することにより2本鎖DNA切断を起こすとENLはATMによりリン酸化されること,ENLのリン酸化部位に変異を導入するとATMによるリン酸化は起こらなくなること,ENLのリン酸化によりBMI1との相互作用が増加することが明らかにされた.さらに,ENLのリン酸化部位の変異体ではポリコーム抑制複合体1は転写部位にリクルートされず,転写の抑制も起こらなくなった.このことから,2本鎖DNA切断が生じるとENLはATMによりリン酸化され,BMI1との相互作用が増強することによりポリコーム抑制複合体1を転写部位にリクルートし,転写の抑制をひき起こしていると考えられた.
ENLのリン酸化を模倣した変異体は,in vivoにおいてほかの転写伸長因子複合体の構成タンパク質との相互作用は変化しないまま,BMI1との結合が増加した.この結果から,ENLはATMによりリン酸化されると立体構造に変化が起こり,転写伸長因子複合体の構成タンパク質とのとの相互作用は保ちつつポリコーム抑制複合体1と相互作用できるようになると考えられた.
2本鎖DNA切断が生じた際にその近傍において転写が抑制されないと2本鎖DNA切断の修復にどのような影響があるのか検討した.2本鎖DNA切断により誘導される転写の抑制の起こらないENLの変異体では,DNA修復タンパク質であるKU70の2本鎖DNA切断部位へのリクルートが減少し,また,放射線に感受性を示した.このことから,ATMは2本鎖DNA切断が生じた際にその近傍において転写を抑制することにより,転写より2本鎖DNA切断の修復を優先して進め,これがゲノム安定性の維持につながるのではないかと考えられた.
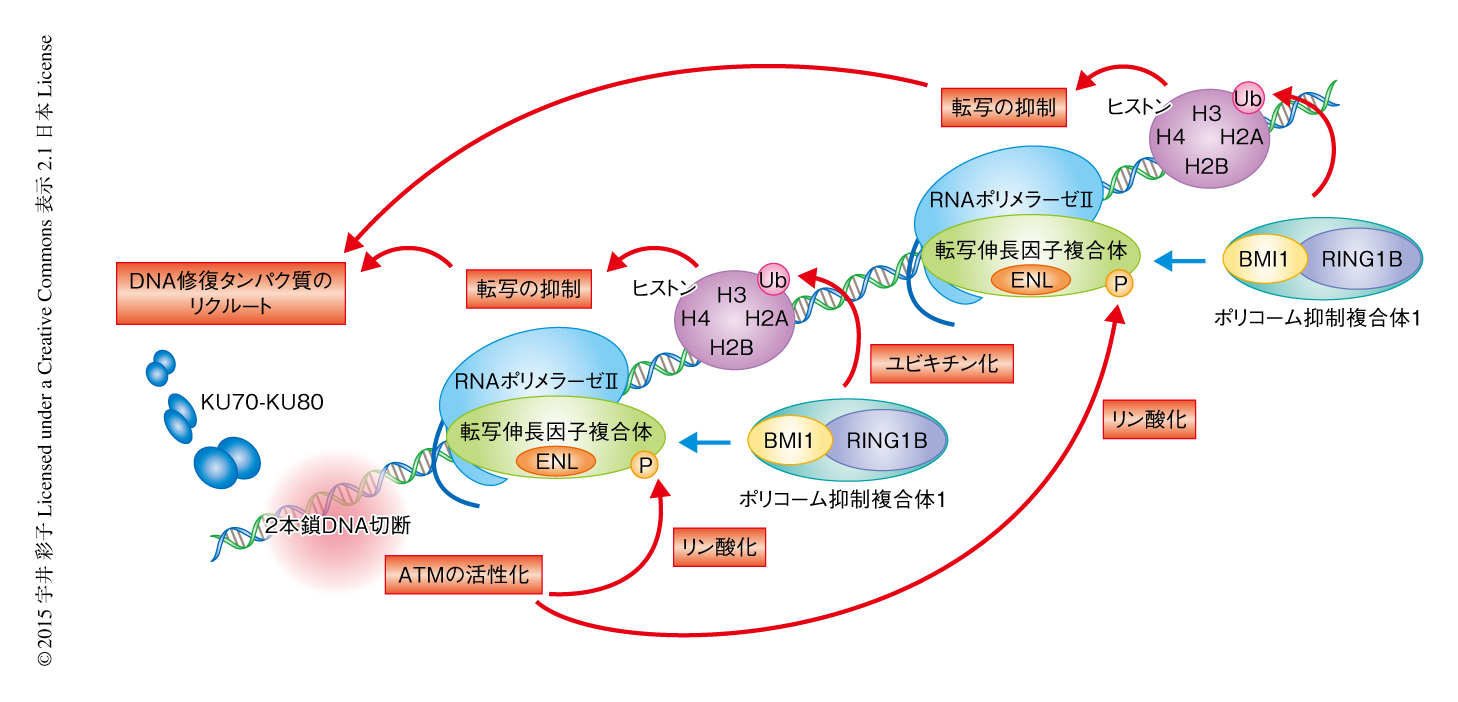
今回の研究により,転写促進能をもつタンパク質と転写抑制能をもつタンパク質とが協調して転写伸長反応をすばやく停止する新しい転写抑制機構が存在すること,ATMは転写伸長因子複合体の構成タンパク質であるENLのリン酸化により転写伸長から転写の抑制へとスイッチを切り換えることによりゲノムの安定性を維持していることが明らかにされた(図2).
ENLを含む転写伸長因子複合体は転写伸長反応を促進すると考えられている9).このため,ATMがこのENLにリン酸化というマークをつけ,このマークによりポリコーム抑制複合体1を転写伸長部位にリクルートしてヒストンH2Aをユビキチン化すれば,すぐに転写伸長反応を停止できるのだろう.2本鎖DNA切断という細胞の緊急時に転写促進能をもつタンパク質と転写抑制能をもつタンパク質とが協調して転写伸長反応を停止する機構はこれまで知られておらず,新しい転写抑制機構だと考えられた.
ATMがDNA損傷チェックポイントタンパク質やDNA修復タンパク質の制御だけではなく,転写伸長因子複合体の構成タンパク質をリン酸化することにより転写を制御することも明らかにされた.ATMによる転写の抑制が起こらないとDNA修復タンパク質であるKU70の2本鎖DNA切断部位へのリクルートが阻害されたことから,このATMによる転写の抑制は転写部位の近傍における2本鎖DNA切断の修復の促進に重要だと考えられた.おそらく,転写が活性化している際には巨大な転写複合体がクロマチンを占拠していること,また,クロマチンが転写の活性化に適した状態に変化していることなど,転写の活性化はDNA修復を阻害する可能性が考えられ,転写と2本鎖DNA切断の修復が近傍において同時に起こるとそれらが衝突する可能性が考えられる.そこで,ATMが転写を一時的に停止し,転写複合体のクロマチンへの結合を抑制し,ヒストンの修飾やクロマチンの構造などを2本鎖DNA切断の修復に適した状態に変化させるとともに,転写と2本鎖DNA切断の修復との衝突をさけ,転写より2本鎖DNA切断の修復を優先的に進めゲノムの安定性を維持しているのではないかと考えられた.
略歴:2003年 東北大学大学院薬学研究科博士後期課程 修了,同年 同 研究員,2006年 国立がんセンター リサーチレジデント,2007年 同 研究員,2010年 東北大学加齢医学研究所 助教を経て,2015年より聖マリアンナ医科大学 講師.
研究テーマ:DNA損傷応答,染色体の不安定性.
抱負:DNA損傷応答および染色体の不安定性の研究をとおして医療の発展に貢献したい.
© 2015 宇井 彩子 Licensed under CC 表示 2.1 日本
(東北大学加齢医学研究所 加齢ゲノム制御プロテオーム研究部門)
email:宇井彩子
DOI: 10.7875/first.author.2015.063
Transcriptional elongation factor ENL phosphorylated by ATM recruits Polycomb and switches off transcription for DSB repair.
Ayako Ui, Yuko Nagaura, Akira Yasui
Molecular Cell, 58, 468-482 (2015)
要 約
ENLは転写伸長因子複合体の構成タンパク質として転写を促進することが知られている.筆者らは,ENLと相互作用するタンパク質として転写抑制能をもつポリコーム抑制複合体1の構成タンパク質であるBMI1を同定した.転写が活性化されているときにはENLはポリコーム抑制複合体1をリクルートしないが,転写部位の近傍において2本鎖DNA切断が起こるとENLはATMによりリン酸化されることによりBMI1との相互作用が増加し,ポリコーム抑制複合体1を転写部位にリクルートして転写を抑制した.さらに,この転写の抑制は2本鎖DNA切断部位においてDNA修復タンパク質のリクルートを促進したことから,ATMによる転写の抑制は転写より2本鎖DNA切断部位の修復を優先して進めるために必要である可能性が示唆された.
はじめに
ATMはDNA損傷チェックポイント機構やDNA修復を制御する重要なキナーゼであるが,近年,転写も制御することが示されている1).2010年,転写部位の近傍において2本鎖DNA切断が起こると,ATMによりヒストンH2AのLys119あるいはLys120がユビキチン化され転写が抑制されることが見い出された1).当時,この転写部位に起こるヒストンH2Aのユビキチン化はATMによるヒストンγH2AXの形成に依存してリクルートされるRNF8およびRNF168によるのではないかと推測されたが,のちの研究から,RNF8およびRNF168はヒストンH2AのLys119あるいはLys120をユビキチン化する活性をもたないことが明らかにされ2),ATMがどのようにヒストンH2AのLys119あるいはLys120のユビキチン化を制御して転写を抑制しているのかは不明であった.また,2014年には,SWI/SNF複合体の構成タンパク質であるPBAFがATMによりリン酸化されヒストンH2Aのユビキチン化の促進および2本鎖DNA切断により誘導される転写の抑制に関与すること,また,ヒストンH2Aをユビキチン化する活性をもつポリコーム群タンパク質が2本鎖DNA切断により誘導される転写の抑制に関与することが示された3).しかし,クロマチンリモデリングタンパク質であるPBAFがどうやってヒストンH2Aのユビキチン化をひき起こすのか,ポリコーム群タンパク質がどうやって転写部位にリクルートされて転写の抑制に関与するのか,また,ATMとポリコーム群タンパク質がどのような関係にあるのかも不明で,ATMによる転写部位におけるヒストンH2AのLys119あるいはLys120のユビキチン化および2本鎖DNA切断により誘導される転写の抑制の制御機構については明らかではなかった.
今回,筆者らは,転写部位の近傍において2本鎖DNA切断が起こると,ATMが転写伸長因子複合体の構成タンパク質として転写を促進するENLをリン酸化し,転写抑制能をもつポリコーム抑制複合体1をリクルートしてヒストンH2AのLys119あるいはLys120をユビキチン化することにより転写伸長反応を停止する,という新しい転写抑制機構を明らかにした.また,ATMは2本鎖DNA切断の近傍において転写を抑制することより,DNA修復を転写より優先的に進めゲノムの安定性を維持している可能性のあることを明らかにした.
1.転写促進能をもつENLと転写抑制能をもつポリコーム抑制複合体1の構成タンパク質であるBMI1は相互作用する
ENLと相互作用するタンパク質を検索したところ,ポリコーム抑制複合体1の構成タンパク質でありユビキチンリガーゼ複合体のサブユニットであるRING1BおよびBMI1が同定された.in vitroにおける解析により,ENLはBMI1と直接的に相互作用することが明らかにされた.ENLはRNAポリメラーゼIIのC末端ドメインのリン酸化を制御する転写伸長因子複合体(super elongation complex:SEC)の構成タンパク質であり,転写を促進することが知られている4-9)(図1a).一方で,ポリコーム抑制複合体1はヒストンH2AのLys119あるいはLys120をユビキチン化することにより転写を抑制することが知られている10)(図1b).このように,反対の機能をもつENLとポリコーム抑制複合体1について,転写の過程における挙動を調べた.その結果,ENLは転写が活性化した際には転写部位に結合し転写活性化に関与していた.一方で,ポリコーム抑制複合体1は転写部位にほとんど結合せず転写活性化には関与していなかった.このことから,ENLとポリコーム抑制複合体1は転写において異なる機能をもつと考えられた.
2.ポリコーム抑制複合体1は転写部位の近傍において2本鎖DNA切断が生じるとそこにリクルートされる
転写の抑制をひき起こしたときENLおよびポリコーム抑制複合体1の挙動はどう変化するのか検討した.ENLは転写の活性化とともに転写部位に結合し,転写を抑制しても変化なく転写部位に局在しつづけた.一方で,ポリコーム抑制複合体1は転写を活性化した際,また,RNAポリメラーゼIIのリン酸化の抑制により転写を抑制した際には転写部位に結合しなかったが,転写部位の近傍において2本鎖DNA切断を起こすことにより転写を抑制した際には転写部位にリクルートされた.
3.2本鎖DNA切断が生じるとポリコーム抑制複合体1はENLおよびATMに依存して転写部位にリクルートされる
転写活性化の近傍において2本鎖DNA切断を起こすことにより転写を抑制した際のポリコーム抑制複合体1の転写部位へのリクルートはENLに依存するのか,また,この転写の抑制を制御することが報告されているATMに依存するのか検討した.その結果,ENLをノックダウンした細胞ではポリコーム抑制複合体1の転写部位へのリクルートは減少した.また,ATMの阻害剤を処理することによりポリコーム抑制複合体1の転写部位へのリクルートは減少した.これらの結果から,ポリコーム抑制複合体1は2本鎖DNA切断が生じた際にENLおよびATMに依存して転写部位にリクルートされることが明らかにされた.
4.2本鎖DNA切断が生じるとENLおよびポリコーム抑制複合体1は転写部位のヒストンH2Aのユビキチン化を促進することにより転写を抑制する
2本鎖DNA切断が生じた際の転写部位におけるヒストンH2AのLys119あるいはLys120のユビキチン化および転写の抑制に,ENLあるいはポリコーム抑制複合体1は関与するのか検討した.その結果,ENLをノックダウンした細胞,および,ポリコーム抑制複合体1の構成タンパク質をノックダウンした細胞では,2本鎖DNA切断が生じた際の転写部位におけるヒストンH2Aのユビキチン化が減少し,転写の抑制は起こらないことが明らかにされた.
5.ENLはATMによりリン酸化されるとBMI1との結合が増加する
以上の結果から,ENLとポリコーム抑制複合体1との結合はATMにより制御されており,ENLがポリコーム抑制複合体1を転写部位にリクルートすることにより転写を抑制するのではないかと推測した.そこで,ENLおよびBMI1においてATMによるリン酸化部位を検索したところ,ENLにATMによるリン酸化部位が見い出された.放射線を照射することにより2本鎖DNA切断を起こすとENLはATMによりリン酸化されること,ENLのリン酸化部位に変異を導入するとATMによるリン酸化は起こらなくなること,ENLのリン酸化によりBMI1との相互作用が増加することが明らかにされた.さらに,ENLのリン酸化部位の変異体ではポリコーム抑制複合体1は転写部位にリクルートされず,転写の抑制も起こらなくなった.このことから,2本鎖DNA切断が生じるとENLはATMによりリン酸化され,BMI1との相互作用が増強することによりポリコーム抑制複合体1を転写部位にリクルートし,転写の抑制をひき起こしていると考えられた.
ENLのリン酸化を模倣した変異体は,in vivoにおいてほかの転写伸長因子複合体の構成タンパク質との相互作用は変化しないまま,BMI1との結合が増加した.この結果から,ENLはATMによりリン酸化されると立体構造に変化が起こり,転写伸長因子複合体の構成タンパク質とのとの相互作用は保ちつつポリコーム抑制複合体1と相互作用できるようになると考えられた.
6.ATMは2本鎖DNA切断が生じた際に転写より2本鎖DNA切断の修復を優先させる
2本鎖DNA切断が生じた際にその近傍において転写が抑制されないと2本鎖DNA切断の修復にどのような影響があるのか検討した.2本鎖DNA切断により誘導される転写の抑制の起こらないENLの変異体では,DNA修復タンパク質であるKU70の2本鎖DNA切断部位へのリクルートが減少し,また,放射線に感受性を示した.このことから,ATMは2本鎖DNA切断が生じた際にその近傍において転写を抑制することにより,転写より2本鎖DNA切断の修復を優先して進め,これがゲノム安定性の維持につながるのではないかと考えられた.
おわりに
今回の研究により,転写促進能をもつタンパク質と転写抑制能をもつタンパク質とが協調して転写伸長反応をすばやく停止する新しい転写抑制機構が存在すること,ATMは転写伸長因子複合体の構成タンパク質であるENLのリン酸化により転写伸長から転写の抑制へとスイッチを切り換えることによりゲノムの安定性を維持していることが明らかにされた(図2).
ENLを含む転写伸長因子複合体は転写伸長反応を促進すると考えられている9).このため,ATMがこのENLにリン酸化というマークをつけ,このマークによりポリコーム抑制複合体1を転写伸長部位にリクルートしてヒストンH2Aをユビキチン化すれば,すぐに転写伸長反応を停止できるのだろう.2本鎖DNA切断という細胞の緊急時に転写促進能をもつタンパク質と転写抑制能をもつタンパク質とが協調して転写伸長反応を停止する機構はこれまで知られておらず,新しい転写抑制機構だと考えられた.
ATMがDNA損傷チェックポイントタンパク質やDNA修復タンパク質の制御だけではなく,転写伸長因子複合体の構成タンパク質をリン酸化することにより転写を制御することも明らかにされた.ATMによる転写の抑制が起こらないとDNA修復タンパク質であるKU70の2本鎖DNA切断部位へのリクルートが阻害されたことから,このATMによる転写の抑制は転写部位の近傍における2本鎖DNA切断の修復の促進に重要だと考えられた.おそらく,転写が活性化している際には巨大な転写複合体がクロマチンを占拠していること,また,クロマチンが転写の活性化に適した状態に変化していることなど,転写の活性化はDNA修復を阻害する可能性が考えられ,転写と2本鎖DNA切断の修復が近傍において同時に起こるとそれらが衝突する可能性が考えられる.そこで,ATMが転写を一時的に停止し,転写複合体のクロマチンへの結合を抑制し,ヒストンの修飾やクロマチンの構造などを2本鎖DNA切断の修復に適した状態に変化させるとともに,転写と2本鎖DNA切断の修復との衝突をさけ,転写より2本鎖DNA切断の修復を優先的に進めゲノムの安定性を維持しているのではないかと考えられた.
文 献
- Shanbhag, N. M., Rafalska-Metcalf, I. U., Balane-Bolivar, C. et al.: ATM-dependent chromatin changes silence transcription in cis to DNA double-strand breaks. Cell, 141, 970-981 (2010)[PubMed]
- Mattiroli, F., Vissers, J. H., van Dijk, W. J. et al.: RNF168 ubiquitinates K13-15 on H2A/H2AX to drive DNA damage signaling. Cell, 150, 1182-1195 (2012)[PubMed]
- Kakarougkas, A., Ismail, A., Chambers, A. L. et al.: Requirement for PBAF in transcriptional repression and repair at DNA breaks in actively transcribed regions of chromatin. Mol. Cell, 55, 723-732 (2014)[PubMed]
- Sobhian, B. Laguette, N., Yatim, A. et al.: HIV-1 Tat assembles a multifunctional transcription elongation complex and stably associates with the 7SK snRNP. Mol. Cell, 38, 439-451 (2010)[PubMed]
- He, N., Chan, C. K., Sobhian, B. et al.: Human Polymerase-Associated Factor complex (PAFc) connects the Super Elongation Complex (SEC) to RNA polymerase II on chromatin. Proc. Natl. Acad. Sci. USA, 108, E636-E645 (2011)[PubMed]
- Lin, C., Garrett, A. S., De Kumar, B. et al.: Dynamic transcriptional events in embryonic stem cells mediated by the super elongation complex (SEC). Genes Dev., 25, 1486-1498 (2011)[PubMed]
- Smith, E., Lin, C. Q. & Shilatifard, A.: The super elongation complex (SEC) and MLL in development and disease. Genes Dev., 25, 661-672 (2011)[PubMed]
- Luo, Z. J., Lin, C. Q. & Shilatifard, A.: The super elongation complex (SEC) family in transcriptional control. Nat. Rev. Mol. Cell Biol., 13, 543-547 (2012)[PubMed]
- Zhou, Q., Li, T. D. & Price, D. H.: RNA polymerase II elongation control. Annu. Rev. Biochem., 81, 119-143 (2012)[PubMed]
- Schwartz, Y. B. & Pirrotta, V.: Polycomb silencing mechanisms and the management of genomic programmes. Nat. Rev. Genet., 8, 9-22 (2007)[PubMed]
著者プロフィール
略歴:2003年 東北大学大学院薬学研究科博士後期課程 修了,同年 同 研究員,2006年 国立がんセンター リサーチレジデント,2007年 同 研究員,2010年 東北大学加齢医学研究所 助教を経て,2015年より聖マリアンナ医科大学 講師.
研究テーマ:DNA損傷応答,染色体の不安定性.
抱負:DNA損傷応答および染色体の不安定性の研究をとおして医療の発展に貢献したい.
© 2015 宇井 彩子 Licensed under CC 表示 2.1 日本