歯周病の原因細菌であるPorphyromonas gingivalisは補体とToll様受容体とのクロストークを利用した免疫系からのユニークな回避機構をもつ
前川 知樹
(米国Pennsylvania大学School of Dental Medicine,Department of Microbiology)
email:前川知樹
DOI: 10.7875/first.author.2014.088
Porphyromonas gingivalis manipulates complement and TLR signaling to uncouple bacterial clearance from inflammation and promote dysbiosis.
Tomoki Maekawa, Jennifer L. Krauss, Toshiharu Abe, Ravi Jotwani, Martha Triantafilou, Kathy Triantafilou, Ahmed Hashim, Shifra Hoch, Michael A. Curtis, Gabriel Nussbaum, John D. Lambris, George Hajishengallis
Cell Host & Microbe, 15, 768-778 (2014)
グラム陰性桿菌であるPorphyromonas gingivalisは歯周病の代表的な原因細菌として知られている.P. gingivalisは,歯周炎の組織における絶対量は少ないものの,口腔のフローラを質的に変化させることにより炎症などの免疫の破綻をひき起こすことが示唆されている.今回,筆者らは,歯周病の発症に重要な役割をもつ好中球に焦点をあて,P. gingivalisのもつ免疫系からのユニークな回避機構について明らかにした.P. gingivalisはジンジパインというタンパク分解酵素をもち,炎症による局所の微小な出血からヘム鉄を得ると同時に,補体の成分であるC5からC5aを切り出している.切り出されたC5aはP. gingivalisのもつToll様受容体への抗原性とともに,好中球におけるクロストークを活性化させ,抗菌作用を担うアダプタータンパク質MyD88のユビキチン化による分解,および,Malを介したPI3キナーゼの活性化による好中球の食作用の抑制により,免疫系から回避していることが示唆された.P. gingivalisは歯周病をひき起こすkeystone細菌として重要な役割をはたしているため,C5aのアンタゴニストは歯周病の新しい治療法につながる可能性がある.
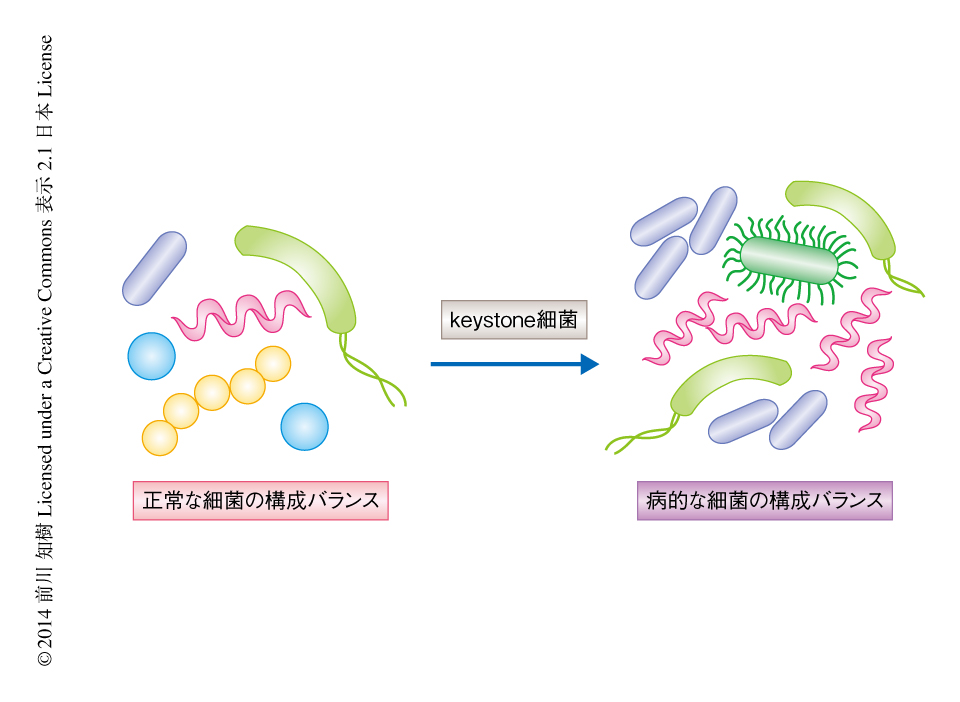
歯周病は慢性炎症をともなう歯周結合組織や周囲骨組織の破壊を特徴とする疾患で,国民の約80%が罹患している生活習慣病である.代表的な原因細菌としてグラム陰性桿菌であるPorphyromonas gingivalisが同定されているが,P. gingivalisは単独で感染させても歯槽骨の吸収をひき起こさないことが示されている.ところが,マウスの口腔フローラに少量のP. gingivalisを感染させると歯槽骨の吸収をひき起こし,さらには,口腔の全体における総細菌数が増加し細菌構成のバランスの異常をひき起こす.このように,量は少ないものの中心的な役割をはたす細菌はkeystone細菌と名づけられている1-3)(図1).P. gingivalisは免疫細胞による殺菌作用や貪食作用を抑制するが,軽微な炎症をひき起こすことによりその生存に必須なヘム鉄や分解されたペプチドを得ている.しかし,P. gingivalisのもつ免疫系のユニークな回避機構の詳細についてはいまだ明らかになっていない.好中球はヒトの歯周炎の組織において歯周病の発症および進行に大きくかかわっていることから4),この研究においては,P. gingivalisと好中球との関連をin vivoおよびin vitroにて検討した.
補体のひとつC5a受容体,あるいは,Toll様受容体(Toll-like receptor:TLR)のひとつTLR2を介したP. gingivalisのもつ免疫系の回避機構の解明のため,C5a受容体ノックアウトマウスおよびTLR2ノックアウトマウスを用いたチャンバーモデル5)(背中にチタンコイルを留置する方法),および,特異的な阻害剤を用い検討した.チャンバーにP. gingivalisを投与し2時間後に回収すると,予想されたとおり,C5a受容体のアンタゴニストを同時に投与した場合にはP. gingivalisのもつ免疫系の回避機構は抑制され好中球による殺菌が認められた.ジンジパイン欠損株であるKDP128株を使用した際にはC5aが産生されないため6),免疫系の回避機構は機能しなかったが,好中球による殺菌は認められた.また,抗TLR2抗体を投与した場合,あるいは,C5a受容体ノックアウトマウスまたはTLR2ノックアウトマウスにおいては,P. gingivalisのもつ免疫系の回避機構は抑制された.つまり,C5a受容体からのシグナルおよびTLR2からのシグナルはP. gingivalisの生存に必須であることが示唆された.興味深いことに,C5a受容体あるいはTLR2の欠損により,炎症性サイトカインの発現は完全には抑制されなかった.
MyD88は免疫シグナル伝達系におけるアダプタータンパク質であり殺菌において重要な役割を担っている5).ヒトの好中球において,P. gingivalisの刺激によりmRNAレベルでのMyD88の発現は変化しなかったものの,タンパク質レベルでは発現が減少した.TLR2のアゴニストである合成ペプチドPam3CSK4による刺激のみではMyD88の分解はひき起こされなかったが,同時にC5aをくわえるとMyD88は分解された.つまり,好中球におけるMyD88の分解は,C5a受容体とTLR2とのクロストークによりひき起こされることが明らかになった.さらに,蛍光共鳴エネルギー移動(fluorescence resonance energy transfer:FRET)解析および共焦点顕微鏡による解析により,C5a受容体とTLR2は非常に近い位置で作用していることが確認された.また,プロテアソーム阻害剤であるEpoxomycinによりMyD88の分解が抑制されたことから,MyD88の分解はユビキチン化を介することが示唆された.実際に,HL-60細胞の好中球においてユビキチンリガーゼのひとつであるSmurf1をノックダウンすると,P. gingivalisによるMyD88の分解は抑制された.P. gingivalisによるMyD88のユビキチン化はチャンバーモデルを用いてin vivoにおいても確認された.
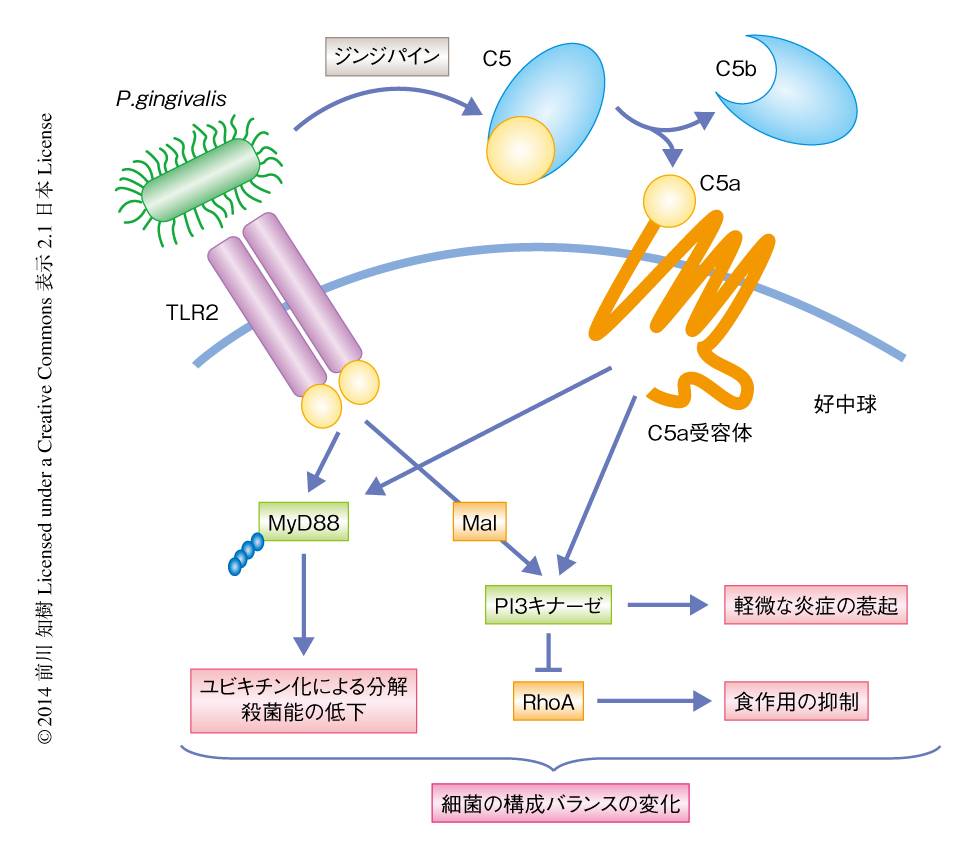
MyD88ノックアウトマウスにC5a受容体あるいは抗TLR2抗体をくわえたときと,C5a受容体ノックアウトマウスあるいはTLR2ノックアウトマウスとで,好中球によるP. gingivalisの殺菌能は同じ程度であったことから,P. gingivalisにはMyD88とは独立した免疫系の回避機構の存在することが考えられた.そこで,マウスにP. gingivalisを投与すると同時にPI3キナーゼの阻害剤であるLY294002をくわえたところ,P. gingivalisは好中球により殺菌された.食作用の程度を調べると,PI3キナーゼ阻害剤をくわえたときにはくわえていないときと比べ有意にP. gingivalisの食作用が生じていた.P. gingivalisによる好中球の食作用の抑制は,TLR2とC5a受容体とのクロストークがPI3キナーゼを活性化することにより,食作用において重要な役割をはたすRhoファミリーGタンパク質のひとつであるRhoA 7) が抑制されることによりひき起こされたものと考えられた.また興味深いことに,PI3キナーゼ阻害剤の投与により炎症性サイトカインの発現は抑制された.つまり,P. gingivalisはMyD88とは独立にPI3キナーゼを活性化することにより好中球の食作用を抑制し,また,P. gingivalisそれ自体の栄養素の取得のため炎症反応を制御し軽微な炎症をひき起こしていることが明らかになった(図2).
MalはTLR2シグナル伝達経路においてMyD88とTLR2とを橋渡しするアダプタータンパク質である8,9).また同時に,MalはPI3キナーゼとTLR2とのシグナル伝達にも重要な役割を担っている.Mal,TLR2,PI3キナーゼの共免疫沈降により,P. gingivalisの刺激に対しMalが重要な橋渡し役をはたしている可能性が示唆された.しかし,MalはMyD88のように宿主の防御に作用するのか,あるいは,C5a受容体-TLR2-PI3キナーゼ経路の活性化をひき起こすのかは明らかになっていなかった.このMalの好中球における役割を解明するため,P. gingivalisの殺菌に対するMalノックダウンの影響について検討した.Malをノックダウンすると,C5a受容体,抗TLR2抗体,あるいは,PI3キナーゼの阻害剤であるLY294002を用いた場合と同様に,好中球によるP. gingivalisの殺菌作用が認められた.さらに,好中球によるP. gingivalisの食作用も認められた.つまり,MalはPI3キナーゼの上流に位置することがと予測された.Malノックアウトマウスにおいても同様な結果が確認された.P. gingivalisはMyD88とは独立に,Malを介したTLR2とPI3キナーゼとのシグナル伝達を活性化することにより,好中球によるP. gingivalisの食作用を抑制し軽微な炎症反応をひき起こしていることが示唆された.
これまでの結果から,好中球においてP. gingivalisはTLR2とC5a受容体とのクロストークをひき起こすことによりMyD88のユビキチン化を介した分解をひき起こし,宿主に防御的な抗菌反応を抑制することが示唆された.また,C5a受容体とTLR2とのクロストークはMalを介してPI3キナーゼを活性化することにより好中球の食作用を抑制し,炎症反応を制御し生存に必要な軽微な炎症反応をひき起こしていた.
keystone細菌という量は少ないが重要な役割をはたす細菌は,メタゲノミクスの概念がでてきてからまもないとはいえ,いまだ報告は少ない.サルモネラ菌などの消化管への感染による食中毒の事例では,腸内フローラのほとんどを病原細菌が独占し炎症をひき起こす.したがって,この研究におけるP. gingivalisの感染においては,一般的な感染モデルとはまったく異なる病態発症の機構が存在すると考えられた.歯周病においても,1990年代からこれまで,P. gingivalisのもつ病原性のみが強調されており,いまだ,P. gingivalisが細菌の構成バランスの異常をひき起こすという報告はない.このP. gingivalisの免疫系のユニークな回避機構は,今後,P. gingivalisの特性を逆手にとった治療法に応用できることが予想される.事実,筆者らはすでに,サルにおける実験的な歯周炎に補体治療薬を応用し報告している.今後は,keystone細菌の候補となる細菌をメタゲノム解析により網羅的に同定することにより,細菌感染症に対しより選択的かつ効率的な治療法の開発が可能になるかもしれない.
略歴:2011年 新潟大学大学院医歯学総合研究科 修了,2012年より米国Pennsylvania大学School of Dental Medicine博士研究員.
研究テーマ:keystone細菌の同定による細菌感染症に対する新規の治療法の開発.
抱負:メタゲノミクスを駆使し,世界中の細菌感染症を対象として,ユニークな機能をもつkeystone細菌を同定する.細菌感染症に対し選択的かつ効果的な次世代プロバイオティクスを用いた治療法を見い出す.
© 2014 前川 知樹 Licensed under CC 表示 2.1 日本
(米国Pennsylvania大学School of Dental Medicine,Department of Microbiology)
email:前川知樹
DOI: 10.7875/first.author.2014.088
Porphyromonas gingivalis manipulates complement and TLR signaling to uncouple bacterial clearance from inflammation and promote dysbiosis.
Tomoki Maekawa, Jennifer L. Krauss, Toshiharu Abe, Ravi Jotwani, Martha Triantafilou, Kathy Triantafilou, Ahmed Hashim, Shifra Hoch, Michael A. Curtis, Gabriel Nussbaum, John D. Lambris, George Hajishengallis
Cell Host & Microbe, 15, 768-778 (2014)
この論文に出現する遺伝子・タンパク質のUniprot ID
補体, Toll様受容体, TLR, ジンジパイン(Q51817), C5(P06684), C5a(P06684), MyD88(P22366), Mal(Q99JY1), PI3キナーゼ, C5a受容体(P30993), Toll-like receptor, TLR2(Q9QUN7), 炎症性サイトカイン, ユビキチンリガーゼ, Smurf1(Q9HCE7), RhoファミリーGタンパク質, RhoA(Q9QUI0)
要 約
グラム陰性桿菌であるPorphyromonas gingivalisは歯周病の代表的な原因細菌として知られている.P. gingivalisは,歯周炎の組織における絶対量は少ないものの,口腔のフローラを質的に変化させることにより炎症などの免疫の破綻をひき起こすことが示唆されている.今回,筆者らは,歯周病の発症に重要な役割をもつ好中球に焦点をあて,P. gingivalisのもつ免疫系からのユニークな回避機構について明らかにした.P. gingivalisはジンジパインというタンパク分解酵素をもち,炎症による局所の微小な出血からヘム鉄を得ると同時に,補体の成分であるC5からC5aを切り出している.切り出されたC5aはP. gingivalisのもつToll様受容体への抗原性とともに,好中球におけるクロストークを活性化させ,抗菌作用を担うアダプタータンパク質MyD88のユビキチン化による分解,および,Malを介したPI3キナーゼの活性化による好中球の食作用の抑制により,免疫系から回避していることが示唆された.P. gingivalisは歯周病をひき起こすkeystone細菌として重要な役割をはたしているため,C5aのアンタゴニストは歯周病の新しい治療法につながる可能性がある.
はじめに
歯周病は慢性炎症をともなう歯周結合組織や周囲骨組織の破壊を特徴とする疾患で,国民の約80%が罹患している生活習慣病である.代表的な原因細菌としてグラム陰性桿菌であるPorphyromonas gingivalisが同定されているが,P. gingivalisは単独で感染させても歯槽骨の吸収をひき起こさないことが示されている.ところが,マウスの口腔フローラに少量のP. gingivalisを感染させると歯槽骨の吸収をひき起こし,さらには,口腔の全体における総細菌数が増加し細菌構成のバランスの異常をひき起こす.このように,量は少ないものの中心的な役割をはたす細菌はkeystone細菌と名づけられている1-3)(図1).P. gingivalisは免疫細胞による殺菌作用や貪食作用を抑制するが,軽微な炎症をひき起こすことによりその生存に必須なヘム鉄や分解されたペプチドを得ている.しかし,P. gingivalisのもつ免疫系のユニークな回避機構の詳細についてはいまだ明らかになっていない.好中球はヒトの歯周炎の組織において歯周病の発症および進行に大きくかかわっていることから4),この研究においては,P. gingivalisと好中球との関連をin vivoおよびin vitroにて検討した.
1.P. gingivalisは好中球による殺菌作用を抑制するが炎症を完全には抑制しない
補体のひとつC5a受容体,あるいは,Toll様受容体(Toll-like receptor:TLR)のひとつTLR2を介したP. gingivalisのもつ免疫系の回避機構の解明のため,C5a受容体ノックアウトマウスおよびTLR2ノックアウトマウスを用いたチャンバーモデル5)(背中にチタンコイルを留置する方法),および,特異的な阻害剤を用い検討した.チャンバーにP. gingivalisを投与し2時間後に回収すると,予想されたとおり,C5a受容体のアンタゴニストを同時に投与した場合にはP. gingivalisのもつ免疫系の回避機構は抑制され好中球による殺菌が認められた.ジンジパイン欠損株であるKDP128株を使用した際にはC5aが産生されないため6),免疫系の回避機構は機能しなかったが,好中球による殺菌は認められた.また,抗TLR2抗体を投与した場合,あるいは,C5a受容体ノックアウトマウスまたはTLR2ノックアウトマウスにおいては,P. gingivalisのもつ免疫系の回避機構は抑制された.つまり,C5a受容体からのシグナルおよびTLR2からのシグナルはP. gingivalisの生存に必須であることが示唆された.興味深いことに,C5a受容体あるいはTLR2の欠損により,炎症性サイトカインの発現は完全には抑制されなかった.
2.C5a受容体とTLR2のクロストークはMyD88の分解を誘導する
MyD88は免疫シグナル伝達系におけるアダプタータンパク質であり殺菌において重要な役割を担っている5).ヒトの好中球において,P. gingivalisの刺激によりmRNAレベルでのMyD88の発現は変化しなかったものの,タンパク質レベルでは発現が減少した.TLR2のアゴニストである合成ペプチドPam3CSK4による刺激のみではMyD88の分解はひき起こされなかったが,同時にC5aをくわえるとMyD88は分解された.つまり,好中球におけるMyD88の分解は,C5a受容体とTLR2とのクロストークによりひき起こされることが明らかになった.さらに,蛍光共鳴エネルギー移動(fluorescence resonance energy transfer:FRET)解析および共焦点顕微鏡による解析により,C5a受容体とTLR2は非常に近い位置で作用していることが確認された.また,プロテアソーム阻害剤であるEpoxomycinによりMyD88の分解が抑制されたことから,MyD88の分解はユビキチン化を介することが示唆された.実際に,HL-60細胞の好中球においてユビキチンリガーゼのひとつであるSmurf1をノックダウンすると,P. gingivalisによるMyD88の分解は抑制された.P. gingivalisによるMyD88のユビキチン化はチャンバーモデルを用いてin vivoにおいても確認された.
3.PI3キナーゼの活性化による食作用の抑制と炎症の誘導
MyD88ノックアウトマウスにC5a受容体あるいは抗TLR2抗体をくわえたときと,C5a受容体ノックアウトマウスあるいはTLR2ノックアウトマウスとで,好中球によるP. gingivalisの殺菌能は同じ程度であったことから,P. gingivalisにはMyD88とは独立した免疫系の回避機構の存在することが考えられた.そこで,マウスにP. gingivalisを投与すると同時にPI3キナーゼの阻害剤であるLY294002をくわえたところ,P. gingivalisは好中球により殺菌された.食作用の程度を調べると,PI3キナーゼ阻害剤をくわえたときにはくわえていないときと比べ有意にP. gingivalisの食作用が生じていた.P. gingivalisによる好中球の食作用の抑制は,TLR2とC5a受容体とのクロストークがPI3キナーゼを活性化することにより,食作用において重要な役割をはたすRhoファミリーGタンパク質のひとつであるRhoA 7) が抑制されることによりひき起こされたものと考えられた.また興味深いことに,PI3キナーゼ阻害剤の投与により炎症性サイトカインの発現は抑制された.つまり,P. gingivalisはMyD88とは独立にPI3キナーゼを活性化することにより好中球の食作用を抑制し,また,P. gingivalisそれ自体の栄養素の取得のため炎症反応を制御し軽微な炎症をひき起こしていることが明らかになった(図2).
4.MalはC5a受容体とTLR2とのクロストークによるPI3キナーゼの活性化に重要である
MalはTLR2シグナル伝達経路においてMyD88とTLR2とを橋渡しするアダプタータンパク質である8,9).また同時に,MalはPI3キナーゼとTLR2とのシグナル伝達にも重要な役割を担っている.Mal,TLR2,PI3キナーゼの共免疫沈降により,P. gingivalisの刺激に対しMalが重要な橋渡し役をはたしている可能性が示唆された.しかし,MalはMyD88のように宿主の防御に作用するのか,あるいは,C5a受容体-TLR2-PI3キナーゼ経路の活性化をひき起こすのかは明らかになっていなかった.このMalの好中球における役割を解明するため,P. gingivalisの殺菌に対するMalノックダウンの影響について検討した.Malをノックダウンすると,C5a受容体,抗TLR2抗体,あるいは,PI3キナーゼの阻害剤であるLY294002を用いた場合と同様に,好中球によるP. gingivalisの殺菌作用が認められた.さらに,好中球によるP. gingivalisの食作用も認められた.つまり,MalはPI3キナーゼの上流に位置することがと予測された.Malノックアウトマウスにおいても同様な結果が確認された.P. gingivalisはMyD88とは独立に,Malを介したTLR2とPI3キナーゼとのシグナル伝達を活性化することにより,好中球によるP. gingivalisの食作用を抑制し軽微な炎症反応をひき起こしていることが示唆された.
これまでの結果から,好中球においてP. gingivalisはTLR2とC5a受容体とのクロストークをひき起こすことによりMyD88のユビキチン化を介した分解をひき起こし,宿主に防御的な抗菌反応を抑制することが示唆された.また,C5a受容体とTLR2とのクロストークはMalを介してPI3キナーゼを活性化することにより好中球の食作用を抑制し,炎症反応を制御し生存に必要な軽微な炎症反応をひき起こしていた.
おわりに
keystone細菌という量は少ないが重要な役割をはたす細菌は,メタゲノミクスの概念がでてきてからまもないとはいえ,いまだ報告は少ない.サルモネラ菌などの消化管への感染による食中毒の事例では,腸内フローラのほとんどを病原細菌が独占し炎症をひき起こす.したがって,この研究におけるP. gingivalisの感染においては,一般的な感染モデルとはまったく異なる病態発症の機構が存在すると考えられた.歯周病においても,1990年代からこれまで,P. gingivalisのもつ病原性のみが強調されており,いまだ,P. gingivalisが細菌の構成バランスの異常をひき起こすという報告はない.このP. gingivalisの免疫系のユニークな回避機構は,今後,P. gingivalisの特性を逆手にとった治療法に応用できることが予想される.事実,筆者らはすでに,サルにおける実験的な歯周炎に補体治療薬を応用し報告している.今後は,keystone細菌の候補となる細菌をメタゲノム解析により網羅的に同定することにより,細菌感染症に対しより選択的かつ効率的な治療法の開発が可能になるかもしれない.
文 献
- Hajishengallis, G., Liang, S., Payne, M. A. et al.: Low-abundance biofilm species orchestrates inflammatory periodontal disease through the commensal microbiota and complement. Cell Host Microbe, 10, 497-506 (2011)[PubMed]
- Hajishengallis, G.: Immunomicrobial pathogenesis of periodontitis: keystones, pathobionts, and host response. Trends Immunol., 35, 3-11 (2014)[PubMed]
- Hajishengallis, G., Darveau, R. P. & Curtis, M. A.: The keystone-pathogenhypothesis. Nat. Rev. Microbiol., 10, 717-725 (2012)[PubMed]
- Nussbaum, G. & Shapira, L.: How has neutrophil research improved our understanding of periodontal pathogenesis? J. Clin. Periodontol., 38 (Suppl. 11), 49-59 (2011)[PubMed]
- Burns, E., Eliyahu, T., Uematsu, S. et al.: TLR2-dependent inflammatory response to Porphyromonas gingivalis is MyD88 independent, whereas MyD88 is required to clear infection. J. Immunol., 184, 1455-1462 (2010)[PubMed]
- Liang, S., Krauss, J. L., Domon, H. et al.: The C5a receptor impairs IL-12-dependent clearance of Porphyromonas gingivalis and is required for induction of periodontal bone loss. J. Immunol., 186, 869-877 (2011)[PubMed]
- Wiedemann, A., Patel, J. C., Lim, J. et al.: Two distinct cytoplasmic regions of the β2 integrin chain regulate RhoA function during phagocytosis. J. Cell Biol., 172, 1069-1079 (2006)[PubMed]
- Honda, F., Kano, H., Kanegane, H. et al.: The kinase Btk negatively regulates the production of reactive oxygen species and stimulation-induced apoptosis in human neutrophils. Nat. Immunol., 13, 369-378 (2012)[PubMed] [新着論文レビュー]
- Kagan, J. C. & Medzhitov, R.: Phosphoinositide-mediated adaptor recruitment controls Toll-like receptor signaling. Cell, 125, 943-955 (2006)[PubMed]
著者プロフィール
略歴:2011年 新潟大学大学院医歯学総合研究科 修了,2012年より米国Pennsylvania大学School of Dental Medicine博士研究員.
研究テーマ:keystone細菌の同定による細菌感染症に対する新規の治療法の開発.
抱負:メタゲノミクスを駆使し,世界中の細菌感染症を対象として,ユニークな機能をもつkeystone細菌を同定する.細菌感染症に対し選択的かつ効果的な次世代プロバイオティクスを用いた治療法を見い出す.
© 2014 前川 知樹 Licensed under CC 表示 2.1 日本