高糖質食の摂取による糖代謝の異常が腫瘍の悪性化に及ぼす影響
平林 享・Ross L. Cagan
(米国Icahn School of Medicine at Mount Sinai,Department of Developmental and Regenerative Biology)
email:平林 享
DOI: 10.7875/first.author.2013.108
Transformed Drosophila cells evade diet-mediated insulin resistance through Wingless signaling.
Susumu Hirabayashi, Thomas J. Baranski, Ross L. Cagan
Cell, 154, 664-675 (2013)
2型糖尿病はさまざまながんの発症率を上昇させることが知られているが,その分子機構は明らかになっていない.ショウジョウバエに高糖質食をあたえると,高血糖,高インスリン血症,インスリン抵抗性など,2型糖尿病に認められる糖代謝の異常がひき起こされる.今回,筆者らは,Ras/Srcの活性化したショウジョウバエに高糖質食をあたえると,腫瘍の増殖および転移能が亢進し悪性化することを見い出した.高糖質食をあたえたショウジョウバエの野生型の組織はインスリン抵抗性を示したのに対し,Ras/Srcの活性化した組織では逆にインスリン感受性が亢進しグルコースの取り込みが促進された.この現象は高糖質食とRas/Srcの活性化によるWingless/Wntシグナル伝達経路を介したインスリン受容体の発現の上昇によるものであることがわかった.したがって,高糖質食によりインスリン感受性の亢進したRas/Srcの活性化した組織では,インスリンおよびグルコースを効率的に利用することにより腫瘍の悪性化が促進されると考えられた.また,これらの経路を標的とした治療薬を組み合わせることにより,高糖質食による腫瘍の悪性化は抑制された.
近年,2型糖尿病や肥満などの生活習慣病は増加の一途をたどっている.2型糖尿病は心疾患をはじめとしたさまざまな合併症を併発する.最近,2型糖尿病は肝がん,膵臓がん,大腸がんを促進する危険因子であることが報告され,糖尿病の合併症にがんも追加されるべきであるとの見解が示されている1).しかし,2型糖尿病ががんの発生や進行にどのようにかかわっているのかはよくわかっていない.
インスリンは血中のグルコースの組織への取り込みを促進し血糖を低下させるホルモンであるが,2型糖尿病の患者ではさまざまな組織においてインスリン感受性が低下しグルコースの取り込みが減少する(インスリン抵抗性).この結果,血中のグルコース濃度が高まる(高血糖)とともに,インスリン抵抗性を補償するため血中のインスリンが増加する(高インスリン血症).したがって,高インスリン血症および高血糖はがんを促進する危険因子である可能性が指摘されているが,その因果関係には不明な点が多い.とくに,インスリン抵抗性をひき起こした組織に発生したがん細胞はどのようにインスリンやグルコースを利用するのか,その作用機序はまったく不明である.
筆者らは,ショウジョウバエに高糖質食をあたえると,高血糖,高インスリン血症,インスリン抵抗性などの糖代謝の異常や,心機能の低下など,2型糖尿病に認められる症状のひき起こされることを報告している2,3).今回,筆者らは,Ras/Srcの活性化したモデルショウジョウバエを用いて,高糖質食による腫瘍の悪性化の分子機構について解析するとともに,その分子機構にもとづき予測された治療薬の組合せについて検討した.
ショウジョウバエの複眼原基の上皮組織にがん遺伝子であるRas遺伝子の活性型変異体を導入するとともに,がん遺伝子産物であるSrcの抑制タンパク質をコードするCsk遺伝子の機能喪失変異体を導入することにより,RasとSrcを同時に活性化した細胞のクローンを誘導した.この変異ショウジョウバエに普通食をあたえると,Ras/Srcの活性化した細胞は組織に散在した小さなクローンを形成した.一方,この変異ショウジョウバエに高糖質食をあたえ糖代謝の異常を誘導して糖尿病様とすると,Ras/Srcの活性化した細胞は過増殖し腫瘍を形成した.このとき,腫瘍の形成にともないRas/Srcの活性化した細胞は複眼原基の上皮組織から浸潤して転移し,ショウジョウバエの気管である管状上皮にまきつくように2次腫瘍を形成した.高糖質食と同じカロリーの高脂肪食もしくは高タンパク質食をあたえたショウジョウバエは糖代謝の異常をひき起こさず2),Ras/Srcを活性化した細胞の過増殖も認められなかった.以上の結果から,高糖質食により糖尿病様の症状を呈したショウジョウバエでは,Ras/Srcの活性化した腫瘍は悪性化することがわかった.そこで,このモデルショウジョウバエを用いて,高糖質食が腫瘍の悪性化を促進する分子機構について解析することにした.
Ras/Srcの活性化した腫瘍の高糖質食による悪性化におけるインスリンシグナル伝達経路の役割について解析した.Ras/Srcの活性化とAkt遺伝子の機能低下変異体を組み合わせると,高糖質食による腫瘍の悪性化は抑制された.一方,Ras/Srcの活性化した細胞に活性型のインスリン受容体を過剰に発現させると,普通食をあたえた場合においても腫瘍の形成が認められた.以上の結果は,高糖質食によるRas/Srcの活性化した細胞の過増殖にはインスリンシグナル伝達経路の活性化が重要であることを示した.
野生型の組織およびRas/Srcの活性化した組織におけるインスリン感受性について解析した.野生型の複眼原基の上皮組織は高糖質食により顕著なインスリン抵抗性を示し,インスリン感受性およびグルコースの取り込みが低下した.一方,Ras/Srcの活性化した組織ではインスリン感受性が亢進し,グルコースの取り込みは促進された.以上の結果から,Ras/Srcの活性化した組織は高糖質食によるインスリン抵抗性を回避し,組織の外部のインスリンおよび血糖を効率的に利用できるものと考えられた.
Ras/Srcの活性化した組織が高糖質食によるインスリン抵抗性を回避する分子機構について解析した.高糖質食により悪性化したRas/Srcの活性化した腫瘍ではWingless/Wntの発現が上昇することを見い出した.また,遺伝学的な解析から,高糖質食によるRas/Srcの活性化した腫瘍の悪性化において,転写因子Tcfを介した古典的Wingless/Wntシグナル伝達経路が必要であることが明らかになった.Ras/Srcの活性化した細胞に活性型のインスリン受容体を過剰に発現させた変異体では普通食をあたえた場合においても腫瘍が形成されるが,このとき,Wingless/Wntの発現の上昇が認められた.このことは,Ras/Srcの活性化とインスリンシグナル伝達経路の活性化は協調してWingless/Wntの発現を誘導することを示した.
Wingless/Wntの活性化した組織におけるインスリン感受性について検討した.Wingless/Wntを過剰に発現させた複眼原基の上皮組織は高糖質食によるインスリン抵抗性を回避し,逆に,インスリン感受性が亢進した.したがって,Wingless/Wntの発現の上昇はインスリン抵抗性の回避に十分であることが明らかになった.
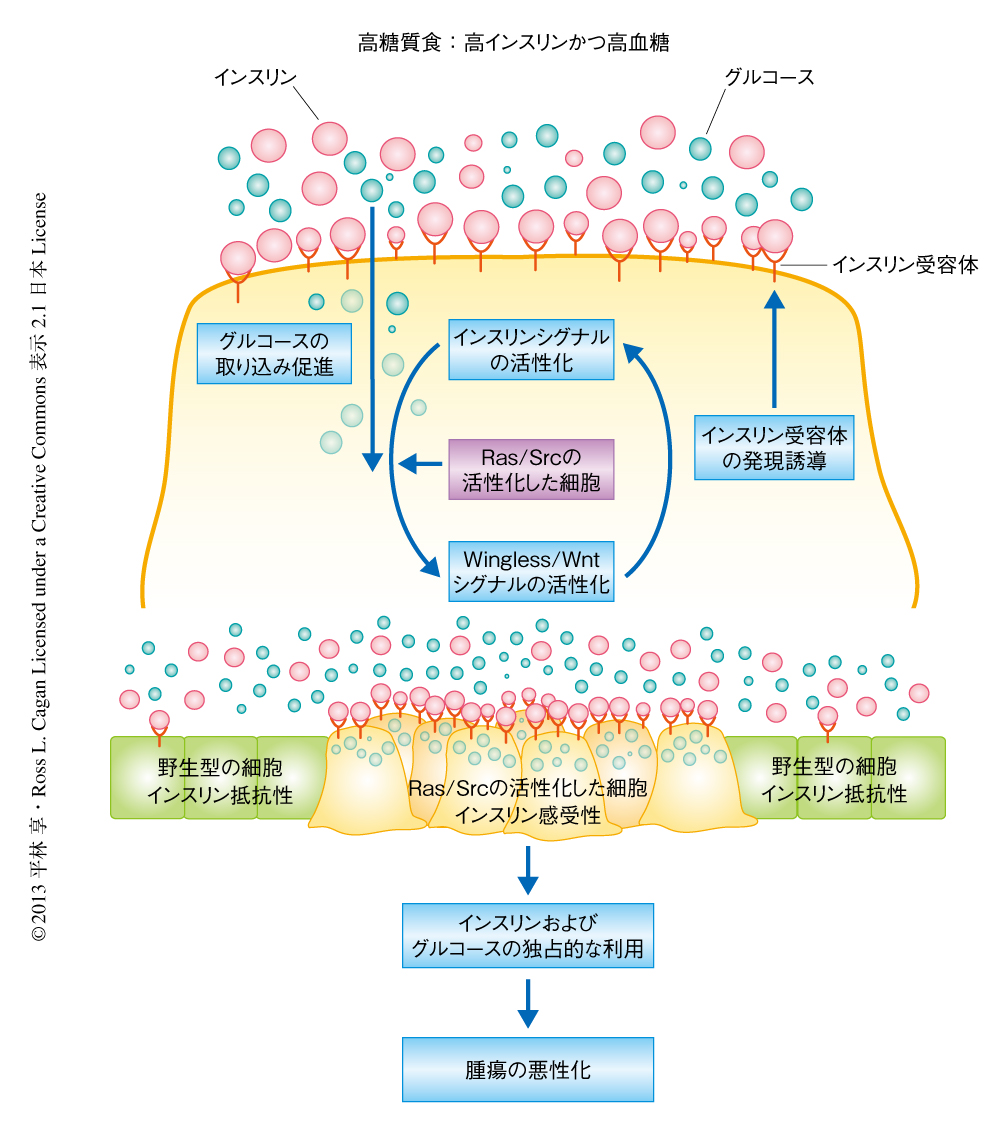
高糖質食をあたえたRas/Srcの活性化した組織では,野生型の組織に比べインスリン受容体の遺伝子の発現が有意に上昇していることがわかった.また,このインスリン受容体の発現は転写因子Tcfを介した古典的Wingless/Wntシグナル伝達経路によるものであることが明らかになった.以上の結果から,Ras/Srcの活性化した細胞は高インスリン状態と協調してWingless/Wntの発現を誘導し,活性化された古典的Wingless/Wntシグナル伝達経路は転写因子Tcfを介してインスリン受容体の発現を誘導しインスリンシグナル伝達経路を活性化するという,シグナル増幅回路を形成することが示された(図1).
ショウジョウバエのヒト疾患モデルを用いた治療薬の候補となる物質の探索は,個体の全体に対する化合物の影響が判定できるため,薬理と毒性との総合評価による治療効果の判定が可能である.筆者らの研究室では,さまざまなショウジョウバエがんモデルを使ってがん治療薬の探索を行っており,多発性内分泌腫瘍症2型のモデルショウジョウバエを用いた,のちに米国Food and Drug Administration(FDA)により転移性内分泌腫瘍症の治療薬として認可されたVandetanibの同定や,化学遺伝学的な手法を用いて創薬された新規のマルチキナーゼ阻害剤について報告している4,5).
この研究において明らかにされたRas/Srcの活性化した腫瘍の高糖質食による悪性化の分子機構から,いくつかの治療の標的が予測された.アカルボースはαグルコシダーゼ阻害剤で2型糖尿病の経口血糖降下薬である.パモ酸ピルビニウムは,最近,Wingless/Wntシグナル伝達経路を阻害することが示された化合物である6).AD81は,最近,筆者らの研究室において創薬化学と遺伝学を駆使して合成された新規の化合物であり,Ras,Src,および,インスリンシグナル伝達経路の下流のタンパク質S6Kを阻害するマルチキナーゼ阻害剤である5).高糖質食により腫瘍の悪性化したショウジョウバエの多くは3齢幼虫期で死亡し約30%しか蛹にならない.そこで,腫瘍の大きさ(薬剤の効果)と蛹化率(薬剤の全身性の毒性)を指標として薬剤の効果を検討した.それぞれの薬剤を単独で投与した場合,蛹化率は上昇した.2つの薬剤を組み合わせた場合は蛹化率がさらに上昇し,3つの薬剤を組み合わせた場合は90%以上の個体が蛹になるとともに腫瘍の形成が劇的に抑制された.以上の結果から,高糖質食により悪性化したがんの治療には,複数のシグナル伝達経路を標的とすることが効果的であることが示唆された.
疫学的な研究により糖尿病とがんへの罹患との強い相関が示されているが,その因果関係および分子機構は依然として不明である.この研究では,ショウジョウバエを用いた解析により,高糖質食による糖代謝の異常が腫瘍の悪性化を促進する分子機構の一端を明らかにした.すなわち,高糖質食をあたえたショウジョウバエではRas/Srcの活性化した細胞は古典的Wingless/Wntシグナル伝達経路を介してインスリン受容体の発現を誘導することにより,インスリン抵抗性を回避し高インスリン血症による豊富なインスリンを独占的に利用することが可能となる.インスリンシグナル伝達経路が活性化すると,高血糖による豊富なグルコースが利用できるとともに,Ras/Srcと協調してさらにWingless/Wntシグナルが活性化する.その結果,シグナル増幅回路が形成され腫瘍の悪性化が進行すると考えられる.
今後は,ヒトにおいても同様な分子機構がはたらくかどうかを解析する必要があるが,最近,ヒトの線維芽細胞を用いた解析により,Wntシグナルが転写因子Tcfを介してインスリン受容体の発現を亢進することが報告され,古典的Wntシグナル伝達経路とインスリンシグナル伝達経路とのクロストークはヒトにおいても保存されていることが示された7).Wntシグナルは肝がん,膵臓がん,大腸がんなど糖尿病との相関の強く認められるがんにおいて上昇することが知られている8-10).したがって,Wntシグナルの活性化したがんはインスリン受容体の発現の誘導を介してインスリン抵抗性を回避することにより,糖尿病の患者において悪性化する可能性が考えられる.実際に,糖尿病により悪性化したがんにおいてWntシグナルの活性化が認められるかどうかは,今後の研究課題である.
略歴:2004年 東京医科歯科大学大学院医歯学総合研究科博士課程 修了,同年 同 助手を経て,2007年より米国Icahn School of Medicine at Mount Sinai博士研究員.
研究テーマ:がんと代謝.
抱負:Medicine from Drosophila.
Ross L. Cagan
米国Icahn School of Medicine at Mount SinaiにてProfessor.
研究室URL:http://drb.mssm.edu/labs/cagan.html
© 2013 平林 享・Ross L. Cagan Licensed under CC 表示 2.1 日本
(米国Icahn School of Medicine at Mount Sinai,Department of Developmental and Regenerative Biology)
email:平林 享
DOI: 10.7875/first.author.2013.108
Transformed Drosophila cells evade diet-mediated insulin resistance through Wingless signaling.
Susumu Hirabayashi, Thomas J. Baranski, Ross L. Cagan
Cell, 154, 664-675 (2013)
要 約
2型糖尿病はさまざまながんの発症率を上昇させることが知られているが,その分子機構は明らかになっていない.ショウジョウバエに高糖質食をあたえると,高血糖,高インスリン血症,インスリン抵抗性など,2型糖尿病に認められる糖代謝の異常がひき起こされる.今回,筆者らは,Ras/Srcの活性化したショウジョウバエに高糖質食をあたえると,腫瘍の増殖および転移能が亢進し悪性化することを見い出した.高糖質食をあたえたショウジョウバエの野生型の組織はインスリン抵抗性を示したのに対し,Ras/Srcの活性化した組織では逆にインスリン感受性が亢進しグルコースの取り込みが促進された.この現象は高糖質食とRas/Srcの活性化によるWingless/Wntシグナル伝達経路を介したインスリン受容体の発現の上昇によるものであることがわかった.したがって,高糖質食によりインスリン感受性の亢進したRas/Srcの活性化した組織では,インスリンおよびグルコースを効率的に利用することにより腫瘍の悪性化が促進されると考えられた.また,これらの経路を標的とした治療薬を組み合わせることにより,高糖質食による腫瘍の悪性化は抑制された.
はじめに
近年,2型糖尿病や肥満などの生活習慣病は増加の一途をたどっている.2型糖尿病は心疾患をはじめとしたさまざまな合併症を併発する.最近,2型糖尿病は肝がん,膵臓がん,大腸がんを促進する危険因子であることが報告され,糖尿病の合併症にがんも追加されるべきであるとの見解が示されている1).しかし,2型糖尿病ががんの発生や進行にどのようにかかわっているのかはよくわかっていない.
インスリンは血中のグルコースの組織への取り込みを促進し血糖を低下させるホルモンであるが,2型糖尿病の患者ではさまざまな組織においてインスリン感受性が低下しグルコースの取り込みが減少する(インスリン抵抗性).この結果,血中のグルコース濃度が高まる(高血糖)とともに,インスリン抵抗性を補償するため血中のインスリンが増加する(高インスリン血症).したがって,高インスリン血症および高血糖はがんを促進する危険因子である可能性が指摘されているが,その因果関係には不明な点が多い.とくに,インスリン抵抗性をひき起こした組織に発生したがん細胞はどのようにインスリンやグルコースを利用するのか,その作用機序はまったく不明である.
筆者らは,ショウジョウバエに高糖質食をあたえると,高血糖,高インスリン血症,インスリン抵抗性などの糖代謝の異常や,心機能の低下など,2型糖尿病に認められる症状のひき起こされることを報告している2,3).今回,筆者らは,Ras/Srcの活性化したモデルショウジョウバエを用いて,高糖質食による腫瘍の悪性化の分子機構について解析するとともに,その分子機構にもとづき予測された治療薬の組合せについて検討した.
1.高糖質食をあたえたショウジョウバエでは腫瘍の形成および転移能が促進される
ショウジョウバエの複眼原基の上皮組織にがん遺伝子であるRas遺伝子の活性型変異体を導入するとともに,がん遺伝子産物であるSrcの抑制タンパク質をコードするCsk遺伝子の機能喪失変異体を導入することにより,RasとSrcを同時に活性化した細胞のクローンを誘導した.この変異ショウジョウバエに普通食をあたえると,Ras/Srcの活性化した細胞は組織に散在した小さなクローンを形成した.一方,この変異ショウジョウバエに高糖質食をあたえ糖代謝の異常を誘導して糖尿病様とすると,Ras/Srcの活性化した細胞は過増殖し腫瘍を形成した.このとき,腫瘍の形成にともないRas/Srcの活性化した細胞は複眼原基の上皮組織から浸潤して転移し,ショウジョウバエの気管である管状上皮にまきつくように2次腫瘍を形成した.高糖質食と同じカロリーの高脂肪食もしくは高タンパク質食をあたえたショウジョウバエは糖代謝の異常をひき起こさず2),Ras/Srcを活性化した細胞の過増殖も認められなかった.以上の結果から,高糖質食により糖尿病様の症状を呈したショウジョウバエでは,Ras/Srcの活性化した腫瘍は悪性化することがわかった.そこで,このモデルショウジョウバエを用いて,高糖質食が腫瘍の悪性化を促進する分子機構について解析することにした.
2.Ras/Srcの活性化した細胞はインスリン抵抗性を回避する
Ras/Srcの活性化した腫瘍の高糖質食による悪性化におけるインスリンシグナル伝達経路の役割について解析した.Ras/Srcの活性化とAkt遺伝子の機能低下変異体を組み合わせると,高糖質食による腫瘍の悪性化は抑制された.一方,Ras/Srcの活性化した細胞に活性型のインスリン受容体を過剰に発現させると,普通食をあたえた場合においても腫瘍の形成が認められた.以上の結果は,高糖質食によるRas/Srcの活性化した細胞の過増殖にはインスリンシグナル伝達経路の活性化が重要であることを示した.
野生型の組織およびRas/Srcの活性化した組織におけるインスリン感受性について解析した.野生型の複眼原基の上皮組織は高糖質食により顕著なインスリン抵抗性を示し,インスリン感受性およびグルコースの取り込みが低下した.一方,Ras/Srcの活性化した組織ではインスリン感受性が亢進し,グルコースの取り込みは促進された.以上の結果から,Ras/Srcの活性化した組織は高糖質食によるインスリン抵抗性を回避し,組織の外部のインスリンおよび血糖を効率的に利用できるものと考えられた.
3.Ras/Srcの活性化した細胞はWingless/Wntシグナルを介しインスリン受容体の発現を誘導する
Ras/Srcの活性化した組織が高糖質食によるインスリン抵抗性を回避する分子機構について解析した.高糖質食により悪性化したRas/Srcの活性化した腫瘍ではWingless/Wntの発現が上昇することを見い出した.また,遺伝学的な解析から,高糖質食によるRas/Srcの活性化した腫瘍の悪性化において,転写因子Tcfを介した古典的Wingless/Wntシグナル伝達経路が必要であることが明らかになった.Ras/Srcの活性化した細胞に活性型のインスリン受容体を過剰に発現させた変異体では普通食をあたえた場合においても腫瘍が形成されるが,このとき,Wingless/Wntの発現の上昇が認められた.このことは,Ras/Srcの活性化とインスリンシグナル伝達経路の活性化は協調してWingless/Wntの発現を誘導することを示した.
Wingless/Wntの活性化した組織におけるインスリン感受性について検討した.Wingless/Wntを過剰に発現させた複眼原基の上皮組織は高糖質食によるインスリン抵抗性を回避し,逆に,インスリン感受性が亢進した.したがって,Wingless/Wntの発現の上昇はインスリン抵抗性の回避に十分であることが明らかになった.
高糖質食をあたえたRas/Srcの活性化した組織では,野生型の組織に比べインスリン受容体の遺伝子の発現が有意に上昇していることがわかった.また,このインスリン受容体の発現は転写因子Tcfを介した古典的Wingless/Wntシグナル伝達経路によるものであることが明らかになった.以上の結果から,Ras/Srcの活性化した細胞は高インスリン状態と協調してWingless/Wntの発現を誘導し,活性化された古典的Wingless/Wntシグナル伝達経路は転写因子Tcfを介してインスリン受容体の発現を誘導しインスリンシグナル伝達経路を活性化するという,シグナル増幅回路を形成することが示された(図1).
4.高糖質食により悪性化したがんの治療薬の候補となる物質の探索
ショウジョウバエのヒト疾患モデルを用いた治療薬の候補となる物質の探索は,個体の全体に対する化合物の影響が判定できるため,薬理と毒性との総合評価による治療効果の判定が可能である.筆者らの研究室では,さまざまなショウジョウバエがんモデルを使ってがん治療薬の探索を行っており,多発性内分泌腫瘍症2型のモデルショウジョウバエを用いた,のちに米国Food and Drug Administration(FDA)により転移性内分泌腫瘍症の治療薬として認可されたVandetanibの同定や,化学遺伝学的な手法を用いて創薬された新規のマルチキナーゼ阻害剤について報告している4,5).
この研究において明らかにされたRas/Srcの活性化した腫瘍の高糖質食による悪性化の分子機構から,いくつかの治療の標的が予測された.アカルボースはαグルコシダーゼ阻害剤で2型糖尿病の経口血糖降下薬である.パモ酸ピルビニウムは,最近,Wingless/Wntシグナル伝達経路を阻害することが示された化合物である6).AD81は,最近,筆者らの研究室において創薬化学と遺伝学を駆使して合成された新規の化合物であり,Ras,Src,および,インスリンシグナル伝達経路の下流のタンパク質S6Kを阻害するマルチキナーゼ阻害剤である5).高糖質食により腫瘍の悪性化したショウジョウバエの多くは3齢幼虫期で死亡し約30%しか蛹にならない.そこで,腫瘍の大きさ(薬剤の効果)と蛹化率(薬剤の全身性の毒性)を指標として薬剤の効果を検討した.それぞれの薬剤を単独で投与した場合,蛹化率は上昇した.2つの薬剤を組み合わせた場合は蛹化率がさらに上昇し,3つの薬剤を組み合わせた場合は90%以上の個体が蛹になるとともに腫瘍の形成が劇的に抑制された.以上の結果から,高糖質食により悪性化したがんの治療には,複数のシグナル伝達経路を標的とすることが効果的であることが示唆された.
おわりに
疫学的な研究により糖尿病とがんへの罹患との強い相関が示されているが,その因果関係および分子機構は依然として不明である.この研究では,ショウジョウバエを用いた解析により,高糖質食による糖代謝の異常が腫瘍の悪性化を促進する分子機構の一端を明らかにした.すなわち,高糖質食をあたえたショウジョウバエではRas/Srcの活性化した細胞は古典的Wingless/Wntシグナル伝達経路を介してインスリン受容体の発現を誘導することにより,インスリン抵抗性を回避し高インスリン血症による豊富なインスリンを独占的に利用することが可能となる.インスリンシグナル伝達経路が活性化すると,高血糖による豊富なグルコースが利用できるとともに,Ras/Srcと協調してさらにWingless/Wntシグナルが活性化する.その結果,シグナル増幅回路が形成され腫瘍の悪性化が進行すると考えられる.
今後は,ヒトにおいても同様な分子機構がはたらくかどうかを解析する必要があるが,最近,ヒトの線維芽細胞を用いた解析により,Wntシグナルが転写因子Tcfを介してインスリン受容体の発現を亢進することが報告され,古典的Wntシグナル伝達経路とインスリンシグナル伝達経路とのクロストークはヒトにおいても保存されていることが示された7).Wntシグナルは肝がん,膵臓がん,大腸がんなど糖尿病との相関の強く認められるがんにおいて上昇することが知られている8-10).したがって,Wntシグナルの活性化したがんはインスリン受容体の発現の誘導を介してインスリン抵抗性を回避することにより,糖尿病の患者において悪性化する可能性が考えられる.実際に,糖尿病により悪性化したがんにおいてWntシグナルの活性化が認められるかどうかは,今後の研究課題である.
文 献
- Giovannucci, E., Harlan, D. M., Archer, M. C. et al.: Diabetes and cancer: a consensus report. CA Cancer J. Clin., 60, 207-221 (2010)[PubMed]
- Musselman, L. P., Fink, J. L., Narzinski, K. et al.: A high-sugar diet produces obesity and insulin resistance in wild-type Drosophila. Dis. Model Mech., 4, 842-849 (2011)[PubMed]
- Na, J., Musselman, L. P., Pendse, J. et al.: A Drosophila model of high sugar diet-induced cardiomyopathy. PLoS Genet., 9, e1003175 (2013)[PubMed]
- Vidal, M., Wells, S., Ryan, A. et al.: ZD6474 suppresses oncogenic RET isoforms in a Drosophila model for type 2 multiple endocrine neoplasia syndromes and papillary thyroid carcinoma. Cancer Res., 65, 3538-3541 (2005)[PubMed]
- Dar, A. C., Das, T. K., Shokat, K. M. et al.: Chemical genetic discovery of targets and anti-targets for cancer polypharmacology. Nature, 486, 80-84 (2012)[PubMed]
- Thorne, C. A., Hanson, A. J., Schneider, J. et al.: Small-molecule inhibition of Wnt signaling through activation of casein kinase 1α. Nat. Chem. Biol., 6, 829-836 (2010)[PubMed]
- Singh, R., De Aguiar, R. B., Naik, S. et al.: LRP6 enhances glucose metabolism by promoting TCF7L2-dependent insulin receptor expression and IGF receptor stabilization in humans. Cell Metab., 17, 197-209 (2013)[PubMed]
- Fodde, R., Smits, R. & Clevers, H.: APC, signal transduction and genetic instability in colorectal cancer. Nat. Rev. Cancer, 1, 55-67 (2001)[PubMed]
- Laurent-Puig, P. & Zucman-Rossi, J.: Genetics of hepatocellular tumors. Oncogene, 25, 3778-3786 (2006)[PubMed]
- Pasca di Magliano, M., Biankin, A. V., Heiser, P. W. et al.: Common activation of canonical Wnt signaling in pancreatic adenocarcinoma. PLoS One, 2, e1155 (2007)[PubMed]
著者プロフィール
略歴:2004年 東京医科歯科大学大学院医歯学総合研究科博士課程 修了,同年 同 助手を経て,2007年より米国Icahn School of Medicine at Mount Sinai博士研究員.
研究テーマ:がんと代謝.
抱負:Medicine from Drosophila.
Ross L. Cagan
米国Icahn School of Medicine at Mount SinaiにてProfessor.
研究室URL:http://drb.mssm.edu/labs/cagan.html
© 2013 平林 享・Ross L. Cagan Licensed under CC 表示 2.1 日本