淡明細胞型腎細胞がんにおける統合的な分子解析
佐藤悠佑1・本間之夫2・小川誠司1
(1東京大学医学部附属病院 がんゲノミクスプロジェクト,2東京大学大学院医学系研究科 泌尿器外科学)
email:佐藤悠佑,小川誠司
DOI: 10.7875/first.author.2013.092
Integrated molecular analysis of clear-cell renal cell carcinoma.
Yusuke Sato, Tetsuichi Yoshizato, Yuichi Shiraishi, Shigekatsu Maekawa, Yusuke Okuno, Takumi Kamura, Teppei Shimamura, Aiko Sato-Otsubo, Genta Nagae, Hiromichi Suzuki, Yasunobu Nagata, Kenichi Yoshida, Ayana Kon, Yutaka Suzuki, Kenichi Chiba, Hiroko Tanaka, Atsushi Niida, Akihiro Fujimoto, Tatsuhiko Tsunoda, Teppei Morikawa, Daichi Maeda, Haruki Kume, Sumio Sugano, Masashi Fukayama, Hiroyuki Aburatani, Masashi Sanada, Satoru Miyano, Yukio Homma, Seishi Ogawa
Nature Genetics, 45, 860-867 (2013)
淡明細胞型腎細胞がんは腎がんのおよそ80%をしめる.きわめて高頻度にVHL遺伝子が不活性化していることにくわえ,PBRM1遺伝子,BAP1遺伝子,SETD2遺伝子,KDM5C遺伝子など,クロマチンの制御に関与する遺伝子に変異の生じていることが知られているが,分子病態の全体像はいまだ不明である.今回,筆者らは,遺伝子の変異にくわえ,ゲノムコピー数の異常,遺伝子発現の異常,DNAメチル化の異常を網羅的に検出し,これらを統合的に解析することにより淡明細胞型腎細胞がんの分子病態の全容の解明を試みた.ユビキチンリガーゼ複合体であるVHL複合体の機能喪失は淡明細胞型腎細胞がんの95%以上においてみられたが,これは,VHL遺伝子の変異やその遺伝子プロモーターのDNAメチル化だけでなく,VHL複合体の構成タンパク質のひとつであるElongin CをコードするTCEB1遺伝子の変異でも生じることが明らかになった.また,治療の標的となりうる新規の遺伝子異常を同定した.さらに,ゲノム異常にもとづいた分類を行い,これは予後の予測や治療方針の検討に有用となりうることが示唆された.
腎がんは,わが国では年間に約18,000人が発症し約7000人が死亡する悪性腫瘍であり,そのうちおよそ80%を淡明細胞型腎細胞がん(clear cell renal cell carcinoma)がしめる.現在のところ,手術による切除のほかに根治の期待できる治療法はなく,進行例にはインターフェロンによる免疫療法やVEGFあるいはmTORを標的とした分子標的薬が用いられている1).しかし,その効果は限定的なものであり,治療成績の改善のためには分子病態の詳細な理解が必要と考えられる.淡明細胞型腎細胞がんでは,VHL遺伝子の変異やその遺伝子プロモーターのDNAメチル化による不活性化が非常に高頻度に生じており2),これにより低酸素の環境において誘導される転写因子HIFが分解されず蓄積することが知られている.また,近年のゲノム解析により,PBRM1遺伝子,BAP1遺伝子,SETD2遺伝子,KDM5C遺伝子など,クロマチンの制御に関与する遺伝子の変異が明らかにされたが3-5),分子病態の全体像には不明な点が多い.今回,筆者らは,100例以上の淡明細胞型腎細胞がんに対し,全ゲノム塩基配列解析(14例)あるいは全エキソン塩基配列解析(106例)にくわえ,RNA塩基配列解析(100例),ゲノムコピー数の解析(240例),遺伝子発現の解析(101例),DNAメチル化解析(106例)を網羅的に行い,これらを統合的に解析することにより淡明細胞型腎細胞がんの分子病態の全容の解明を試みた.
淡明細胞型腎細胞がん14例に対して全ゲノム塩基配列解析を行った結果,1例あたり平均5100個の変異を検出した.これは造血器腫瘍よりも多いが,ほかの固形腫瘍よりも少ない変異数であった.多くの悪性腫瘍ではC > T/G > Aの塩基置換の割合が高いのに対し6),淡明細胞型腎細胞がんではT > C/A > Gがもっとも多く,C > T/G > A,C > A/G > Tとつづいていた.この塩基置換のパターンは肝細胞がんと類似していた7).また,1例あたり平均12個のゲノム構造異常(染色体転座や逆位)を認めたが,複数の症例に共通する異常はみられなかった.106例の全エキソン塩基配列解析では1例あたり平均48.8個の遺伝子変異を検出した.777の遺伝子が複数の症例において変異しており,このうち28の遺伝子が淡明細胞型腎細胞がんにおいて有意に変異を生じていると考えられた.
有意に変異していた遺伝子のうち,とくに高い頻度で変異のみられた4つの遺伝子,VHL遺伝子,PBRM1遺伝子,BAP1遺伝子,SETD2遺伝子について,さらに134例,合計で240例について遺伝子変異の解析を行った.VHL遺伝子は82%の症例で変異が,10%の症例で遺伝子プロモーターのDNAメチル化が生じていた.また,PBRM1遺伝子,BAP1遺伝子,SETD2遺伝子はそれぞれ41%,10%,11%の症例において変異をきたしていた.これら4つの遺伝子はいずれも第3染色体短腕に位置しており,これらの変異のほとんどは第3染色体短腕におけるヘテロ接合性の消失(loss of heterozygosity:LOH)をともなっていた.また,ナンセンス変異やフレームシフト変異が多くみられ,これらの遺伝子はがん抑制遺伝子として作用しているものと考えられた.
BAP1遺伝子およびSETD2遺伝子の変異アリルの頻度は,VHL遺伝子の変異アリルの頻度より有意に低かった.また,PBRM1遺伝子の変異は予後に影響を及ぼさないのに対し,BAP1遺伝子の変異例では全生存率が有意に低く,SETD2遺伝子の変異例では高頻度に遠隔転移をきたしていた.これらのことから,VHL遺伝子やPBRM1遺伝子の変異は淡明細胞型腎細胞がんの発生初期に生じているのに対し,BAP1遺伝子およびSETD2遺伝子の変異はそれらにひきつづいて生じ,淡明細胞型腎細胞がんの進展にかかわっていることが示唆された.
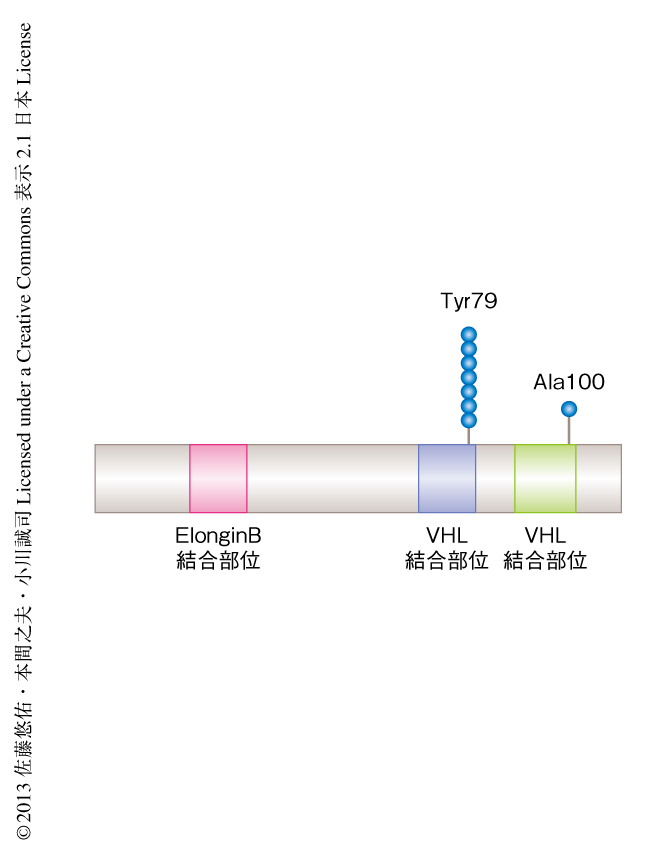
淡明細胞型腎細胞がんにおいてVHL遺伝子に異常のない症例の分子病態はこれまで不明であったが,そのような症例の一部にElongin CをコードするTCEB1遺伝子の変異を新規に検出した.VHLはElongin B,Elongin C,CUL3とユビキチンリガーゼ複合体を形成し,HIFをユビキチン化することによりその分解を促している.VHLの不活性化によりHIFが分解されず蓄積することが,淡明細胞型腎細胞がんの発生につながると考えられている.3.3%(240例中8例)の症例にTCEB1遺伝子の変異を認めたが,これらはいずれもVHL遺伝子に異常のみられない症例であった.また,TCEB1遺伝子の変異例ではTCEB1遺伝子の位置する第8染色体長腕の欠失をともなっており,VHLと同様に,Elongin Cはその機能を喪失することにより淡明細胞型腎細胞がんの発生に関与すると考えられた.興味深いことに,Elongin Cの変異は特定の2か所のアミノ酸残基,Tyr79およびAla100にのみ生じており,これらのアミノ酸残基はVHLとの結合において重要な役割を担っていると考えられた(図1).293T細胞に野生型および変異型のElongion Cを発現させ免疫沈降実験を行ったところ,野生型のElongin CはVHLとの結合が保たれていたが,変異型のElongin CではVHLとの結合はみられなかった.また,HeLa細胞においてウェスタンブロット法によりHIFタンパク質の発現を確認したところ,変異型のElongin Cを発現させただけではHIFの蓄積はみられなかったが,内在性のElongin Cをノックダウンしたうえで変異型のElongin Cを発現させたところHIFの蓄積が観察された.臨床検体において免疫染色を行ったところ,VHL遺伝子の変異例と同様に,TCEB1遺伝子の変異例においても腫瘍細胞の核にHIFの蓄積が確認された.
全エキソン塩基配列解析およびゲノムコピー数の解析により,TET2遺伝子の異常を16.0%(変異5.6%,欠失10.4%)の症例に認めた.TET2遺伝子はDNA脱メチル化にかかわっていると考えられており,造血器腫瘍において高頻度に異常のみられることが知られているが8),固形腫瘍においては大腸がん以外ではじめてその異常が見い出された.また,肺がん9) や乳頭状腎細胞がん10) において,酸化ストレス応答にかかわるKEAP1遺伝子,NRF2遺伝子,CUL3遺伝子に変異の生じることが知られているが,淡明細胞型腎細胞がんにおいて6.6%の症例にこのいずれかの遺伝子の変異を,また,10.4%の症例にCUL3遺伝子の欠失を認めた.MTOR遺伝子の変異を5.6%の症例に認めたが,PIK3CA遺伝子,PTEN遺伝子,TSC1/2遺伝子などとあわせ,26%の症例にmTORシグナル伝達系に関連する遺伝子の変異を認めた.淡明細胞型腎細胞がんではすでに進行例の治療にmTOR阻害薬が使用されているが,mTORシグナル伝達系に関連する遺伝子の変異の状態と治療の効果との関連については,今後の研究において十分に評価する必要があると考えられた.
淡明細胞型腎細胞がんは遺伝子の発現パターンによりccAおよびccBの2つのサブグループにクラスタリングされることが知られているが11),今回の解析でも,それが再現された.ccAサブグループでは血管新生に関与する遺伝子の発現が亢進しており,一方,ccBサブグループでは細胞周期の進行に関与する遺伝子の発現が亢進していた.
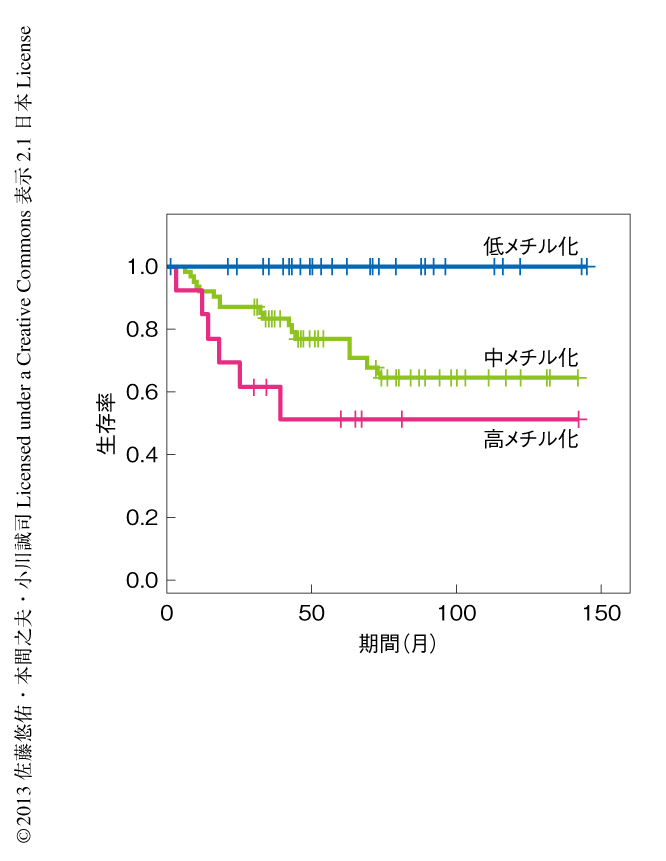
淡明細胞型腎細胞がんをDNAメチル化の状態にもとづいてクラスタリングしたところ,3つのサブグループに分類された.この3つのサブグループのあいだで全体のDNAメチル化の程度に有意な差のみられたことから,それぞれを高メチル化サブグループ,中メチル化サブグループ,低メチル化サブグループとよぶことにした.DNAメチル化のパターンによる分類とほかのゲノム異常とを比較したところ,高メチル化サブグループでは遺伝子変異の総数が有意に多く,染色体の多倍体化,第9染色体短腕におけるヘテロ接合性の消失,第14染色体長腕におけるヘテロ接合性の消失などゲノムコピー数の異常や,BAP1遺伝子の変異頻度,ccBサブグループの頻度が有意に高かった.また,GSEA(gene set enrichment analysis)法による解析を行ったところ,高メチル化サブグループにおいて有意にDNAメチル化されていた1228の遺伝子には,PRC2(Polycomb repressive complex 2,Polycomb抑制複合体2)の標的となる遺伝子が濃縮されていた.PRC2の重要な構成タンパク質をコードするEZH2遺伝子の発現が高メチル化サブグループにおいて有意に高かったこととあわせ,このサブグループではPRC2の機能が亢進していると考えられた.高メチル化サブグループは予後が非常に悪く(図2),PRC2による遺伝子サイレンシングの制御の破綻が悪性度の高いがんの発生に関与していることが示唆された.
この研究では,100例以上の淡明細胞型腎細胞がんを対象に,遺伝子変異の同定をはじめとする多彩なアプローチから淡明細胞型腎細胞がんにおいて生じているゲノム異常のプロファイルを詳細に明らかにした.近年の遺伝子解析技術の進歩にともない大規模な遺伝子解析研究が欧米を中心に行われつつあるが,統合的な解析は非常にかぎられており,この研究の成果がわが国から発信されることは非常に意義深いものと考えられる.今後の研究により,淡明細胞型腎細胞がんの新たな分類法や治療法の開発はもちろん,ゲノム異常にもとづいた治療法や薬剤の選択,すなわち,オーダーメイド医療の実現がより進むことが期待される.
なお,近年,全エキソン塩基配列解析を中心とする網羅的なゲノム解析が世界中でさかんに行われており,淡明細胞型腎細胞がんについても例外ではないが,ほかの論文ではVHL遺伝子の変異頻度が40~60%にとどまっているものが多い.これは,全エキソン塩基配列解析ではGCリッチな領域の正確な塩基配列決定がむずかしいという問題があり,その影響からVHL遺伝子のエキソン1における変異の検出感度が著しく悪いためと考えられる.この研究においても,全エキソン塩基配列解析により検出されたVHL遺伝子の変異頻度は約40%であったのだが,Sanger法やディープシークエンシング法などほかの手法を併用して徹底的に調べた結果,82%という変異頻度を得ることができた.プロモーター遺伝子のDNAメチル化やTCEB1遺伝子の変異をあわせると95%以上の症例においてVHL複合体の構成タンパク質をコードする遺伝子に異常が認められており,将来的には,腎細胞がんの分類(淡明細胞型腎細胞がんの定義)もゲノム異常にもとづくものになっていくのではないかと想像している.
また,この論文に1日先行して,米国の大規模なプロジェクトであるThe Cancer Genome Atlasから同様の研究デザインによる論文が出版された12).およそ400例の検体を解析した非常に規模の大きい研究であり,この論文とあわせ,今後の淡明細胞型腎細胞がんの研究の進展に大きく寄与することが期待される.
略歴:東京大学大学院医学系研究科博士課程 在学中.
研究テーマ:泌尿器腫瘍におけるゲノム解析.
抱負:ゲノム解析に関しては泌尿器科の領域にはまだまだ未開の地が多いので,今後も,どんどん切りこんでいきたい.
本間 之夫(Yukio Homma)
東京大学大学院医学系研究科 教授.
小川 誠司(Seishi Ogawa)
京都大学大学院医学研究科 教授.
(1東京大学医学部附属病院 がんゲノミクスプロジェクト,2東京大学大学院医学系研究科 泌尿器外科学)
email:佐藤悠佑,小川誠司
DOI: 10.7875/first.author.2013.092
Integrated molecular analysis of clear-cell renal cell carcinoma.
Yusuke Sato, Tetsuichi Yoshizato, Yuichi Shiraishi, Shigekatsu Maekawa, Yusuke Okuno, Takumi Kamura, Teppei Shimamura, Aiko Sato-Otsubo, Genta Nagae, Hiromichi Suzuki, Yasunobu Nagata, Kenichi Yoshida, Ayana Kon, Yutaka Suzuki, Kenichi Chiba, Hiroko Tanaka, Atsushi Niida, Akihiro Fujimoto, Tatsuhiko Tsunoda, Teppei Morikawa, Daichi Maeda, Haruki Kume, Sumio Sugano, Masashi Fukayama, Hiroyuki Aburatani, Masashi Sanada, Satoru Miyano, Yukio Homma, Seishi Ogawa
Nature Genetics, 45, 860-867 (2013)
この論文に出現する遺伝子・タンパク質のUniprot ID
VHL(P40337), PBRM1(Q86U86), BAP1(Q92560), SETD2(Q9BYW2), KDM5C(P41229), ユビキチンリガーゼ複合体, Elongin C(Q15369), TCEB1(Q15369), インターフェロン, VEGF, mTOR(P42345), HIF, Elongin B(P62869), CUL3(Q9JLV5), TET2(Q6N021), KEAP1(Q14145), NRF2(Q16236), MTOR(P42345), PIK3CA(P42336), PTEN(P60484), TSC1(Q92574), /2(P49815), PRC2, Polycomb repressive complex 2, Polycomb抑制複合体2, EZH2(Q15910)
要 約
淡明細胞型腎細胞がんは腎がんのおよそ80%をしめる.きわめて高頻度にVHL遺伝子が不活性化していることにくわえ,PBRM1遺伝子,BAP1遺伝子,SETD2遺伝子,KDM5C遺伝子など,クロマチンの制御に関与する遺伝子に変異の生じていることが知られているが,分子病態の全体像はいまだ不明である.今回,筆者らは,遺伝子の変異にくわえ,ゲノムコピー数の異常,遺伝子発現の異常,DNAメチル化の異常を網羅的に検出し,これらを統合的に解析することにより淡明細胞型腎細胞がんの分子病態の全容の解明を試みた.ユビキチンリガーゼ複合体であるVHL複合体の機能喪失は淡明細胞型腎細胞がんの95%以上においてみられたが,これは,VHL遺伝子の変異やその遺伝子プロモーターのDNAメチル化だけでなく,VHL複合体の構成タンパク質のひとつであるElongin CをコードするTCEB1遺伝子の変異でも生じることが明らかになった.また,治療の標的となりうる新規の遺伝子異常を同定した.さらに,ゲノム異常にもとづいた分類を行い,これは予後の予測や治療方針の検討に有用となりうることが示唆された.
はじめに
腎がんは,わが国では年間に約18,000人が発症し約7000人が死亡する悪性腫瘍であり,そのうちおよそ80%を淡明細胞型腎細胞がん(clear cell renal cell carcinoma)がしめる.現在のところ,手術による切除のほかに根治の期待できる治療法はなく,進行例にはインターフェロンによる免疫療法やVEGFあるいはmTORを標的とした分子標的薬が用いられている1).しかし,その効果は限定的なものであり,治療成績の改善のためには分子病態の詳細な理解が必要と考えられる.淡明細胞型腎細胞がんでは,VHL遺伝子の変異やその遺伝子プロモーターのDNAメチル化による不活性化が非常に高頻度に生じており2),これにより低酸素の環境において誘導される転写因子HIFが分解されず蓄積することが知られている.また,近年のゲノム解析により,PBRM1遺伝子,BAP1遺伝子,SETD2遺伝子,KDM5C遺伝子など,クロマチンの制御に関与する遺伝子の変異が明らかにされたが3-5),分子病態の全体像には不明な点が多い.今回,筆者らは,100例以上の淡明細胞型腎細胞がんに対し,全ゲノム塩基配列解析(14例)あるいは全エキソン塩基配列解析(106例)にくわえ,RNA塩基配列解析(100例),ゲノムコピー数の解析(240例),遺伝子発現の解析(101例),DNAメチル化解析(106例)を網羅的に行い,これらを統合的に解析することにより淡明細胞型腎細胞がんの分子病態の全容の解明を試みた.
1.淡明細胞型腎細胞がんにおける遺伝子変異の概要
淡明細胞型腎細胞がん14例に対して全ゲノム塩基配列解析を行った結果,1例あたり平均5100個の変異を検出した.これは造血器腫瘍よりも多いが,ほかの固形腫瘍よりも少ない変異数であった.多くの悪性腫瘍ではC > T/G > Aの塩基置換の割合が高いのに対し6),淡明細胞型腎細胞がんではT > C/A > Gがもっとも多く,C > T/G > A,C > A/G > Tとつづいていた.この塩基置換のパターンは肝細胞がんと類似していた7).また,1例あたり平均12個のゲノム構造異常(染色体転座や逆位)を認めたが,複数の症例に共通する異常はみられなかった.106例の全エキソン塩基配列解析では1例あたり平均48.8個の遺伝子変異を検出した.777の遺伝子が複数の症例において変異しており,このうち28の遺伝子が淡明細胞型腎細胞がんにおいて有意に変異を生じていると考えられた.
2.第3染色体短腕に存在するがん抑制遺伝子
有意に変異していた遺伝子のうち,とくに高い頻度で変異のみられた4つの遺伝子,VHL遺伝子,PBRM1遺伝子,BAP1遺伝子,SETD2遺伝子について,さらに134例,合計で240例について遺伝子変異の解析を行った.VHL遺伝子は82%の症例で変異が,10%の症例で遺伝子プロモーターのDNAメチル化が生じていた.また,PBRM1遺伝子,BAP1遺伝子,SETD2遺伝子はそれぞれ41%,10%,11%の症例において変異をきたしていた.これら4つの遺伝子はいずれも第3染色体短腕に位置しており,これらの変異のほとんどは第3染色体短腕におけるヘテロ接合性の消失(loss of heterozygosity:LOH)をともなっていた.また,ナンセンス変異やフレームシフト変異が多くみられ,これらの遺伝子はがん抑制遺伝子として作用しているものと考えられた.
BAP1遺伝子およびSETD2遺伝子の変異アリルの頻度は,VHL遺伝子の変異アリルの頻度より有意に低かった.また,PBRM1遺伝子の変異は予後に影響を及ぼさないのに対し,BAP1遺伝子の変異例では全生存率が有意に低く,SETD2遺伝子の変異例では高頻度に遠隔転移をきたしていた.これらのことから,VHL遺伝子やPBRM1遺伝子の変異は淡明細胞型腎細胞がんの発生初期に生じているのに対し,BAP1遺伝子およびSETD2遺伝子の変異はそれらにひきつづいて生じ,淡明細胞型腎細胞がんの進展にかかわっていることが示唆された.
3.TCEB1遺伝子の変異
淡明細胞型腎細胞がんにおいてVHL遺伝子に異常のない症例の分子病態はこれまで不明であったが,そのような症例の一部にElongin CをコードするTCEB1遺伝子の変異を新規に検出した.VHLはElongin B,Elongin C,CUL3とユビキチンリガーゼ複合体を形成し,HIFをユビキチン化することによりその分解を促している.VHLの不活性化によりHIFが分解されず蓄積することが,淡明細胞型腎細胞がんの発生につながると考えられている.3.3%(240例中8例)の症例にTCEB1遺伝子の変異を認めたが,これらはいずれもVHL遺伝子に異常のみられない症例であった.また,TCEB1遺伝子の変異例ではTCEB1遺伝子の位置する第8染色体長腕の欠失をともなっており,VHLと同様に,Elongin Cはその機能を喪失することにより淡明細胞型腎細胞がんの発生に関与すると考えられた.興味深いことに,Elongin Cの変異は特定の2か所のアミノ酸残基,Tyr79およびAla100にのみ生じており,これらのアミノ酸残基はVHLとの結合において重要な役割を担っていると考えられた(図1).293T細胞に野生型および変異型のElongion Cを発現させ免疫沈降実験を行ったところ,野生型のElongin CはVHLとの結合が保たれていたが,変異型のElongin CではVHLとの結合はみられなかった.また,HeLa細胞においてウェスタンブロット法によりHIFタンパク質の発現を確認したところ,変異型のElongin Cを発現させただけではHIFの蓄積はみられなかったが,内在性のElongin Cをノックダウンしたうえで変異型のElongin Cを発現させたところHIFの蓄積が観察された.臨床検体において免疫染色を行ったところ,VHL遺伝子の変異例と同様に,TCEB1遺伝子の変異例においても腫瘍細胞の核にHIFの蓄積が確認された.
4.そのほかの遺伝子異常
全エキソン塩基配列解析およびゲノムコピー数の解析により,TET2遺伝子の異常を16.0%(変異5.6%,欠失10.4%)の症例に認めた.TET2遺伝子はDNA脱メチル化にかかわっていると考えられており,造血器腫瘍において高頻度に異常のみられることが知られているが8),固形腫瘍においては大腸がん以外ではじめてその異常が見い出された.また,肺がん9) や乳頭状腎細胞がん10) において,酸化ストレス応答にかかわるKEAP1遺伝子,NRF2遺伝子,CUL3遺伝子に変異の生じることが知られているが,淡明細胞型腎細胞がんにおいて6.6%の症例にこのいずれかの遺伝子の変異を,また,10.4%の症例にCUL3遺伝子の欠失を認めた.MTOR遺伝子の変異を5.6%の症例に認めたが,PIK3CA遺伝子,PTEN遺伝子,TSC1/2遺伝子などとあわせ,26%の症例にmTORシグナル伝達系に関連する遺伝子の変異を認めた.淡明細胞型腎細胞がんではすでに進行例の治療にmTOR阻害薬が使用されているが,mTORシグナル伝達系に関連する遺伝子の変異の状態と治療の効果との関連については,今後の研究において十分に評価する必要があると考えられた.
5.淡明細胞型腎細胞がんのゲノム異常にもとづく分類
淡明細胞型腎細胞がんは遺伝子の発現パターンによりccAおよびccBの2つのサブグループにクラスタリングされることが知られているが11),今回の解析でも,それが再現された.ccAサブグループでは血管新生に関与する遺伝子の発現が亢進しており,一方,ccBサブグループでは細胞周期の進行に関与する遺伝子の発現が亢進していた.
淡明細胞型腎細胞がんをDNAメチル化の状態にもとづいてクラスタリングしたところ,3つのサブグループに分類された.この3つのサブグループのあいだで全体のDNAメチル化の程度に有意な差のみられたことから,それぞれを高メチル化サブグループ,中メチル化サブグループ,低メチル化サブグループとよぶことにした.DNAメチル化のパターンによる分類とほかのゲノム異常とを比較したところ,高メチル化サブグループでは遺伝子変異の総数が有意に多く,染色体の多倍体化,第9染色体短腕におけるヘテロ接合性の消失,第14染色体長腕におけるヘテロ接合性の消失などゲノムコピー数の異常や,BAP1遺伝子の変異頻度,ccBサブグループの頻度が有意に高かった.また,GSEA(gene set enrichment analysis)法による解析を行ったところ,高メチル化サブグループにおいて有意にDNAメチル化されていた1228の遺伝子には,PRC2(Polycomb repressive complex 2,Polycomb抑制複合体2)の標的となる遺伝子が濃縮されていた.PRC2の重要な構成タンパク質をコードするEZH2遺伝子の発現が高メチル化サブグループにおいて有意に高かったこととあわせ,このサブグループではPRC2の機能が亢進していると考えられた.高メチル化サブグループは予後が非常に悪く(図2),PRC2による遺伝子サイレンシングの制御の破綻が悪性度の高いがんの発生に関与していることが示唆された.
おわりに
この研究では,100例以上の淡明細胞型腎細胞がんを対象に,遺伝子変異の同定をはじめとする多彩なアプローチから淡明細胞型腎細胞がんにおいて生じているゲノム異常のプロファイルを詳細に明らかにした.近年の遺伝子解析技術の進歩にともない大規模な遺伝子解析研究が欧米を中心に行われつつあるが,統合的な解析は非常にかぎられており,この研究の成果がわが国から発信されることは非常に意義深いものと考えられる.今後の研究により,淡明細胞型腎細胞がんの新たな分類法や治療法の開発はもちろん,ゲノム異常にもとづいた治療法や薬剤の選択,すなわち,オーダーメイド医療の実現がより進むことが期待される.
なお,近年,全エキソン塩基配列解析を中心とする網羅的なゲノム解析が世界中でさかんに行われており,淡明細胞型腎細胞がんについても例外ではないが,ほかの論文ではVHL遺伝子の変異頻度が40~60%にとどまっているものが多い.これは,全エキソン塩基配列解析ではGCリッチな領域の正確な塩基配列決定がむずかしいという問題があり,その影響からVHL遺伝子のエキソン1における変異の検出感度が著しく悪いためと考えられる.この研究においても,全エキソン塩基配列解析により検出されたVHL遺伝子の変異頻度は約40%であったのだが,Sanger法やディープシークエンシング法などほかの手法を併用して徹底的に調べた結果,82%という変異頻度を得ることができた.プロモーター遺伝子のDNAメチル化やTCEB1遺伝子の変異をあわせると95%以上の症例においてVHL複合体の構成タンパク質をコードする遺伝子に異常が認められており,将来的には,腎細胞がんの分類(淡明細胞型腎細胞がんの定義)もゲノム異常にもとづくものになっていくのではないかと想像している.
また,この論文に1日先行して,米国の大規模なプロジェクトであるThe Cancer Genome Atlasから同様の研究デザインによる論文が出版された12).およそ400例の検体を解析した非常に規模の大きい研究であり,この論文とあわせ,今後の淡明細胞型腎細胞がんの研究の進展に大きく寄与することが期待される.
文 献
- Ljungberg, B., Cowan, N. C., Hanbury, D. C. et al.: EAU guidelines on renal cell carcinoma: the 2010 update. Eur. Urol., 58, 398-406 (2010)[PubMed]
- Gnarra, J. R., Tory, K., Weng, Y. et al.: Mutations of the VHL tumour suppressor gene in renal carcinoma. Nat. Genet., 7, 85-90 (1994)[PubMed]
- Varela, I., Tarpey, P., Raine, K. et al.: Exome sequencing identifies frequent mutation of the SWI/SNF complex gene PBRM1 in renal carcinoma. Nature, 469, 539-542 (2011)[PubMed]
- Pena-Llopis, S., Vega-Rubin-de-Celis, S., Liao, A. et al.: BAP1 loss defines a new class of renal cell carcinoma. Nat. Genet., 44, 751-759 (2012)[PubMed]
- Dalgliesh, G. L., Furge, K., Greenman, C. et al.: Systematic sequencing of renal carcinoma reveals inactivation of histone modifying genes. Nature, 463, 360-363 (2010)[PubMed]
- Greenman, C., Stephens, P., Smith, R. et al.: Patterns of somatic mutation in human cancer genomes. Nature, 446, 153-158 (2007)[PubMed]
- Fujimoto, A. Totoki, Y. Abe, T. et al.: Whole-genome sequencing of liver cancers identifies etiological influences on mutation patterns and recurrent mutations in chromatin regulators. Nat. Genet., 44, 760-764 (2012)[PubMed]
- Delhommeau, F., Dupont, S., Della Valle, V. et al.: Mutation in TET2 in myeloid cancers. N. Engl. J. Med., 360, 2289-2301 (2009)[PubMed]
- Shibata, T., Ohta, T., Tong, K. I. et al.: Cancer related mutations in NRF2 impair its recognition by Keap1-Cul3 E3 ligase and promote malignancy. Proc. Natl. Acad. Sci. USA, 105, 13568-13573 (2008)[PubMed]
- Ooi, A., Dykema, K., Ansari, A. et al.: CUL3 and NRF2 mutations confer an NRF2 activation phenotype in a sporadic form of papillary renal cell carcinoma. Cancer Res., 73, 2044-2051 (2013)[PubMed]
- Brannon, A. R., Reddy, A., Seiler, M. et al.: Molecular stratification of clear cell renal cell carcinoma by consensus clustering reveals distinct subtypes and survival patterns. Genes Cancer, 1, 152-163 (2010)[PubMed]
- Cancer Genome Atlas Research Network: Comprehensive molecular characterization of clear cell renal cell carcinoma. Nature, 499, 43-49 (2013)[PubMed]
著者プロフィール
略歴:東京大学大学院医学系研究科博士課程 在学中.
研究テーマ:泌尿器腫瘍におけるゲノム解析.
抱負:ゲノム解析に関しては泌尿器科の領域にはまだまだ未開の地が多いので,今後も,どんどん切りこんでいきたい.
本間 之夫(Yukio Homma)
東京大学大学院医学系研究科 教授.
小川 誠司(Seishi Ogawa)
京都大学大学院医学研究科 教授.
© 2013 佐藤悠佑・本間之夫・小川誠司 Licensed under CC 表示 2.1 日本