メチル化シトシンヒドロキシラーゼTet1はES細胞自己複製を制御する
伊藤伸介・Yi Zhang
(米国North Carolina大学Chapel Hill校Lineberger Comprehensive Cancer Center,Department of Biochemistry and Biophysics)
email:伊藤伸介
DOI: 10.7875/first.author.2010.007
Role of Tet proteins in 5mC to 5hmC conversion, ES-cell self-renewal and inner cell mass specification.
Shinsuke Ito, Ana C. D’Alessio, Olena V. Taranova, Kwonho Hong, Lawrence C. Sowers, Yi Zhang
Nature, 466, 1129-1133 (2010)
エピジェネティック修飾のひとつであるDNAメチル化は,遺伝子発現の抑制やゲノム安定性の維持に必須である.これまでDNAメチル化の解析は詳細に行われていたが,DNAのメチル基を消去するDNA脱メチル化酵素,および,その分子基盤は不明であった.筆者らは,DNA脱メチル化酵素として機能する可能性をもつTetタンパク質ファミリーに着目し,そのメチル化シトシンヒドロキシラーゼ活性に依存して生成される5-ヒドロキメチルシトシンを検出した.siRNAを用いたノックダウン実験により,マウスES細胞ではTet1が自己複製の維持に重要であることが明らかになった.その分子機構の解明にあたり,筆者らは,Tet1の標的遺伝子のひとつとして自己複製マーカーであるNanog遺伝子を同定した.Tet1ノックダウン細胞ではNanog遺伝子のプロモーターはDNAメチル化をうけており発現が抑制されていた.また,Tet1は胚盤胞期における内部細胞塊への分化にも寄与していることが明らかになった.以上の結果は,Tet1がDNAメチル化の状態を調節することにより,ES細胞の維持に重要なはたらきをしていることを示唆した.
DNAメチル化はもっともよく解析されているエピジェネティック修飾のひとつであり,多種類の生物において遺伝子発現の抑制やゲノム安定性の維持のうえで必要不可欠である.これまでにDNAメチル化を確立する酵素であるDNAメチルトランスフェラーゼの解析は詳細に行われているにもかかわらず,DNAのメチル基を消去するDNA脱メチル化酵素,および,その分子基盤はあまり理解されておらず,長年にわたって議論の的となっていた.筆者らは,最近になり同定された,DNA脱メチル化酵素として機能する可能性をもつTetタンパク質ファミリーに着目し,マウスES細胞(embryonic stem cells,胚性幹細胞)および発生初期胚における機能を解析した.
ゲノムの塩基配列に規定されない,いわゆるエピジェネティックな修飾は,個体の発生や分化の過程において時間的・空間的に厳格な遺伝子発現の制御を行ううえで重要な役割をはたしている.このエピジェネティックな修飾には,DNAメチル化やヒストンの多彩な化学修飾(リン酸化,アセチル化,ユビキチン化,メチル化など)があり,いずれも可逆的な修飾である.DNAメチル化は,DNAメチルトランスフェラーゼ(DNA methyltransferase;DNMT)がCpGジヌクレオチドのシトシン5位の炭素にメチル基を付加して5-メチルシトシン(5mC)とすることによって起こり,その機構はこれまで詳細に解析されている(図1a).一方で,DNA脱メチル化に関しては,さまざまな機構が提唱されているものの結論にはいたっていない1).DNA脱メチル化には受動的な機構と能動的な機構とが存在する.受動的な脱メチル化とは,DNAが複製されるとき親鎖側のメチル基を娘鎖側にコピーする“維持メチル化”が起こらないことにより娘鎖DNAにシトシンが取り込まれ5-メチルシトシンが減少するものである.他方,能動的な脱メチル化はDNA複製には依存しない機構であり,受精直後の精子ゲノム,始原生殖細胞のゲノムや細胞分化後の一部の遺伝子プロモーターでこのようなDNA脱メチル化が観察されている.現象としてはとらえられているが,実際に生体内でどのような反応によりDNA脱メチル化が起こっているのかは明らかになっておらず,DNA脱メチル化酵素の存在も含めて,その実体は不明である.これまでに,植物では5-メチルシトシンを切除することのできるDNAグリコシラーゼについて複数の報告があるが,哺乳動物ではそれらのホモログは確認されていない1).哺乳動物の能動的な脱メチル化は,1)加水分解によりメチル基を直接に除去する機構,2)AID/APOBECファミリータンパク質に依存的に5-メチルシトシンの脱アミノ化によって形成されるT/Gミスマッチが塩基除去修復によりシトシンに置換される機構,3)メチル基を連続的な酸化反応により脱離する機構,などによって行われるものと推測されている.
本稿では,最近になり同定された,メチル基を酸化(ヒドロキシル化)するTetファミリータンパク質に焦点をあて,そのマウスES細胞あるいは発生初期胚における機能を概説する.
チミン-7-ヒドロキシラーゼは,O2,Fe2+,および,α-ケトグルタル酸を補因子とし,チミンの5位のメチル基を連続して酸化することによってイソオロチン酸を産生する(図1b).イソオロチン酸は,イソオロチン酸デカルボキシラーゼによってCO2を放出しウラシルに変換される2).チミン-7-ヒドロキシラーゼとイソオロチン酸デカルボキシラーゼは真菌において単離されているが,哺乳動物では同定されていない.しかし,このチミジンサルベージ経路におけるチミンからウラシルへの変換反応は,チミンと5-メチルシトシンの構造上の類似性から,DNA脱メチル化反応のモデルのひとつとして提起されていた3).他方,寄生性原虫であるトリパノソーマには,チミン-7-ヒドロキシラーゼと類似した酸化活性をもつα-ケトグルタル酸依存型ジオキシゲナーゼ,JBPタンパク質が存在する4).2009年,Raoらのグループは,5-メチルシトシンのメチル基を酸化する酵素を同定すべく,JBPタンパク質の酸化反応にヒントを得てα-ケトグルタル酸依存型ジオキシゲナーゼドメインに相同性をもつ哺乳動物ホモログをデータベース検索し,Tetファミリータンパク質Tet1,Tet2,Tet3を同定した5).Tet1は,O2,Fe2+,および,α-ケトグルタル酸に依存的に5-メチルシトシンのメチル基をヒドロキシル化し,5-ヒドロキシメチルシトシン(5hmC)を合成する活性をもつことが明らかとなった(図1c).この5-ヒドロキシメチルシトシンが哺乳動物のゲノムDNAに存在することは1972年に報告されていたが,最近まで,注目されることはなかった6).また,5-ヒドロキシメチルシトシンはプルキンエ細胞,顆粒細胞などの神経細胞やES細胞などに限定的に存在した5,7).
筆者らは,3つのTetファミリータンパク質が同様な活性をもつかどうか検証することから研究をはじめた.ヒト骨肉腫細胞U2OSにマウスTetファミリータンパク質を一過性に発現させ,抗5-メチルシトシン抗体あるいは抗5-ヒドロキシメチルシトシン抗体を用いて細胞染色を行った結果,Tetファミリータンパク質を発現する細胞は5-メチルシトシン染色の強度が減少し,5-ヒドロキシメチルシトシン染色陽性になった.一方で,Fe2+結合ドメインに変異を導入したTetファミリータンパク質を発現させた細胞では,5-メチルシトシン染色の強度に変化は観察されなかった.くわえて,バキュロウイルス発現系により精製したTetファミリータンパク質と5-メチルシトシンを単一に含む二本鎖DNAとを用いたin vitroアッセイによって,Tetファミリータンパク質はO2,Fe2+,および,α-ケトグルタル酸に依存的に5-メチルシトシンを5-ヒドロキシメチルシトシンに変換する活性をもつことが示された.これらの結果から,いずれのTetファミリータンパク質も5-ヒドロキシメチルシトシン合成活性をもつことが示された.
Tetファミリータンパク質の生物学的な機能を理解するため,マウスにおいてさまざまな組織間あるいは細胞間におけるTetファミリーmRNAの発現比較を行った.Tet1はES細胞に特異的に発現しているのに対し,Tet2は幅広い組織で発現していることが明らかとなった.Tet3は,ES細胞では発現せず,肺,膵臓,脾臓などで強い発現がみられた.
Raoらの報告により,ES細胞で5-ヒドロキシメチルシトシンが観察されたことから,どのTetファミリータンパク質がES細胞において機能的に重要かどうかを知るため,RNAi法によってTetファミリータンパク質を発現抑制してその表現型を解析した.siRNAを発現するレンチウイルスをマウスES細胞に感染させ,薬剤で選択したのちTetファミリーmRNAの発現抑制を定量的PCR法により確認した.また,ES細胞の未分化状態を判別する目的でアルカリホスファターゼ染色すると,Tet1ノックダウン細胞は染色が弱く,かつ,細胞形態の変化が観察された.しかしながら,Tet2ノックダウン細胞およびTet3ノックダウン細胞は対照細胞と同様にES細胞に典型的なコロニーを形成した.これらの結果は,Tet1がES細胞を維持するうえで重要な役割をはたしていることを示唆した.事実,Tet1ノックダウンES細胞は細胞増殖能,コロニー形成能が顕著に低下しており,自己複製能に異常のあることが確認された.さらに,Tet1ノックダウンES細胞は対照細胞と比較して栄養外胚葉に特異的なマーカー(Cdx2,Hand1)と原始内胚葉に特異的なマーカー(Gata6,Gata4)とを強く発現しており,分化をしていることが示唆された.しかしながら,Tet1ノックダウンES細胞の多くの集団がES細胞のマーカーであるSSEA-1を発現していることから,Tet1ノックダウンES細胞は自己複製能に欠損のあるものの,ある程度の未分化な状態は維持していることが示唆された.
Tet1がどのようにしてES細胞の自己複製の維持に寄与しているのか,その分子機構を理解するため,Tet1ノックダウンES細胞におけるOct4,Nanog,Sox2など自己複製マーカーの発現レベルをmRNAの定量的PCR法およびウェスタンブロットにより解析した.その結果,対照細胞と比較してTet1ノックダウンES細胞においてOct4,Sox2の発現に変化がない一方で,Nanogの発現レベルに低下が認められた.つぎに,Nanog遺伝子がTet1の標的遺伝子である可能性を考え,クロマチン免疫沈降法を用いてこれを検討した結果,Tet1はNanog遺伝子のコアプロモーターに結合していることが判明した.さらに,Tet1ノックダウンES細胞において,Nanog遺伝子コアプロモーターのDNAメチル化レベルが上昇していた.Nanog遺伝子プロモーターはES細胞では低メチル化状態にあり,分化した細胞ではDNAメチル化をうけて発現抑制されることが報告されていた8).よって,Tet1非存在下ではNanog遺伝子プロモーターはDNAメチル化をうけて発現抑制されていることが示唆された.また,Tet1のノックダウンによるNanogの発現抑制がNanog遺伝子プロモーターのメチル化に依存的な現象であるかどうかを検証するため,3つのDNAメチルトランスフェラーゼ,DNMT1,DNMT3a,DNMT3bをノックアウトしたES細胞においてTet1をノックダウンし,Nanogの発現レベルを解析した.その結果,DNAにメチル基を新規に付与することができないこのノックアウトES細胞では,Tet1の存在の有無にかかわらずNanogを発現することが判明した.
以上の結果より,Tet1はNanog遺伝子コアプロモーターに結合し,そのDNA低メチル化状態を維持して安定な発現を行い,ES細胞を維持していることが明らかになった(図2).また,Tet1ノックダウンES細胞において,Nanogを強制発現させることでTet1ノックダウンES細胞の大部分の欠損表現型を相補できたことから,幹細胞を維持するうえでNanog遺伝子がTet1の主要な標的遺伝子であることがわかった.
一方,マウス初期胚発生に目をむけると,受精卵は卵割を開始して32細胞期になると栄養外胚葉と内部細胞塊の2種類の細胞系列から構成される胚盤胞になる.これらの過程をとおしてゲノム全体のDNAメチル化レベルは大幅に低下すること9),および,内部細胞塊から樹立されるES細胞の維持にTet1が必要であることを考慮し,受精後の最初の細胞系列の決定にTet1が重要な役割をはたすのではないかとの仮説をたてた.まず,免疫染色により,Tet1は着床前初期胚において核に局在し,胚盤胞期にはおもに内部細胞塊に発現することが確認された.つぎに,2細胞期の1つの細胞にTet1 siRNAとRFP-ヒストンH2B mRNAとをインジェクションし,Tet1をノックダウンした細胞が胚盤胞期において,栄養外胚葉と内部細胞塊のいずれの細胞に寄与するかRFPの蛍光をもとに追跡した.その結果,Tet1をノックダウンした細胞は栄養外胚葉に寄与する割合が高いことが判明し,ES細胞を用いたノックダウン実験と同様の現象が観察された.
以上の結果により,Tet1はES細胞の維持,および,胚盤胞期における内部細胞塊への分化に重要であることが明らかになった.
筆者らは,RaoらのグループのTet1発見を発展させ,Tetファミリータンパク質が5-メチルシトシンを5-ヒドロキシメチルシトシンに変換する活性をもつこと,マウスのTet1がES細胞の自己複製の維持に必要であることを明らかにした.しかしながら,自己複製の維持にTet1のヒドロキシラーゼ活性が直接的に関与しているのかどうか,また,5-ヒドロキシメチルシトシンの存在意義,つまり,5-ヒドロキシメチルシトシンがDNA脱メチル化プロセスの中間産物なのか,あるいは,5-ヒドロキシメチルシトシンが最終産物なのかに対し,明白な答えはでていないのが現状である.これまでの報告により,5-ヒドロキシメチルシトシンの特性として,1)メチル化CpG結合タンパク質MeCP2は5-ヒドロキシメチルシトシンを含む二本鎖DNAに対して結合活性が低いこと10),2)DNMT1はDNA複製と共役して親鎖側のメチル基を娘鎖側にコピーするのに対し,親鎖側に5-ヒドロキシメチルシトシンが存在する場合にはメチル基を娘鎖側にコピーすることができないこと11),3)仔ウシ胸腺抽出液中に5-ヒドロキシメチルシトシン特異的なDNAグリコシラーゼ活性が検出されること12),などがある.1)に関しては,5-メチルシトシンを認識して結合する転写リプレッサー複合体は5-ヒドロキシメチルシトシンには結合できず,別の複合体がこれに結合する可能性が示唆される.2)に関しては,5-ヒドロキシメチルシトシンが維持メチル化機構に対して抑制的に作用する結果,受動的な脱メチル化にいたることが考えられる.3)に関しては,5-ヒドロキシメチルシトシングリコシラーゼが5-ヒドロキシメチルシトシンを切除し,塩基除去修復によってDNA脱メチル化の起こることが示唆される.いずれの場合においても,5-ヒドロキシメチルシトシンは新たなエピジェネティック修飾のひとつとして,5-メチルシトシンとは異なったアウトプットを提示することが予想される.今後のさらなる解析によって,生体内における5-ヒドロキシメチルシトシンの存在意義の明らかになることが期待される.
略歴:2007年 大阪大学大学院生命機能研究科 修了,同 特任研究員,大阪大学大学院基礎工学研究科 研究員(倉岡 功准教授)を経て,2008年より米国North Carolina大学Chapel Hill校 研究員(Yi Zhang教授).
研究テーマ:哺乳動物におけるDNA脱メチル化機構の解析.
抱負:in vitroでDNA脱メチル化活性を検出したい.
Yi Zhang
米国North Carolina大学Chapel Hill校 教授
研究室URL:http://www.med.unc.edu/~zhangyi/lab.htm
(米国North Carolina大学Chapel Hill校Lineberger Comprehensive Cancer Center,Department of Biochemistry and Biophysics)
email:伊藤伸介
DOI: 10.7875/first.author.2010.007
Role of Tet proteins in 5mC to 5hmC conversion, ES-cell self-renewal and inner cell mass specification.
Shinsuke Ito, Ana C. D’Alessio, Olena V. Taranova, Kwonho Hong, Lawrence C. Sowers, Yi Zhang
Nature, 466, 1129-1133 (2010)
この論文に出現する遺伝子・タンパク質のUniprot ID
メチル化シトシンヒドロキシラーゼTet1(Q3URK3), DNA脱メチル化酵素, Tetタンパク質ファミリー, メチル化シトシンヒドロキシラーゼ(Q3URK3), Tet1(Q3URK3), Nanog(Q80Z64), DNAメチルトランスフェラーゼ, DNA methyltransferase, DNMT, DNAグリコシラーゼ, AID/APOBEC, Tetファミリー, チミン-7-ヒドロキシラーゼ(Q66Q78), イソオロチン酸デカルボキシラーゼ, α-ケトグルタル酸依存型ジオキシゲナーゼ, JBPタンパク質, Tet2(Q4JK59), Tet3(Q8BG87), Cdx2(P43241), Hand1(Q64279), Gata6(Q61169), Gata4(Q08369), SSEA-1, Oct4(P20263), Sox2(P48432), DNMT1(P13864), DNMT3a(O88508), DNMT3b(O88509), ヒストンH2B, メチル化CpG結合タンパク質MeCP2(Q9Z2E1), THase(Q66Q78), IDCase
要 約
エピジェネティック修飾のひとつであるDNAメチル化は,遺伝子発現の抑制やゲノム安定性の維持に必須である.これまでDNAメチル化の解析は詳細に行われていたが,DNAのメチル基を消去するDNA脱メチル化酵素,および,その分子基盤は不明であった.筆者らは,DNA脱メチル化酵素として機能する可能性をもつTetタンパク質ファミリーに着目し,そのメチル化シトシンヒドロキシラーゼ活性に依存して生成される5-ヒドロキメチルシトシンを検出した.siRNAを用いたノックダウン実験により,マウスES細胞ではTet1が自己複製の維持に重要であることが明らかになった.その分子機構の解明にあたり,筆者らは,Tet1の標的遺伝子のひとつとして自己複製マーカーであるNanog遺伝子を同定した.Tet1ノックダウン細胞ではNanog遺伝子のプロモーターはDNAメチル化をうけており発現が抑制されていた.また,Tet1は胚盤胞期における内部細胞塊への分化にも寄与していることが明らかになった.以上の結果は,Tet1がDNAメチル化の状態を調節することにより,ES細胞の維持に重要なはたらきをしていることを示唆した.
はじめに
DNAメチル化はもっともよく解析されているエピジェネティック修飾のひとつであり,多種類の生物において遺伝子発現の抑制やゲノム安定性の維持のうえで必要不可欠である.これまでにDNAメチル化を確立する酵素であるDNAメチルトランスフェラーゼの解析は詳細に行われているにもかかわらず,DNAのメチル基を消去するDNA脱メチル化酵素,および,その分子基盤はあまり理解されておらず,長年にわたって議論の的となっていた.筆者らは,最近になり同定された,DNA脱メチル化酵素として機能する可能性をもつTetタンパク質ファミリーに着目し,マウスES細胞(embryonic stem cells,胚性幹細胞)および発生初期胚における機能を解析した.
1.DNA脱メチル化機構
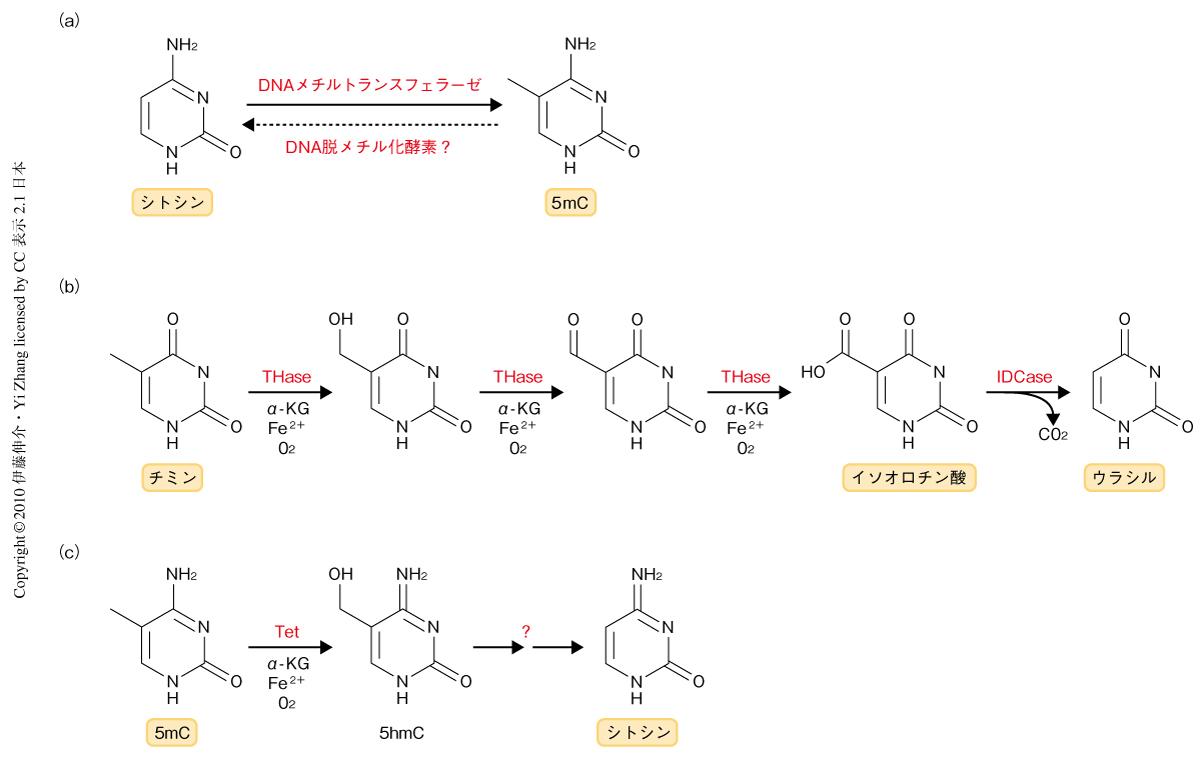
ゲノムの塩基配列に規定されない,いわゆるエピジェネティックな修飾は,個体の発生や分化の過程において時間的・空間的に厳格な遺伝子発現の制御を行ううえで重要な役割をはたしている.このエピジェネティックな修飾には,DNAメチル化やヒストンの多彩な化学修飾(リン酸化,アセチル化,ユビキチン化,メチル化など)があり,いずれも可逆的な修飾である.DNAメチル化は,DNAメチルトランスフェラーゼ(DNA methyltransferase;DNMT)がCpGジヌクレオチドのシトシン5位の炭素にメチル基を付加して5-メチルシトシン(5mC)とすることによって起こり,その機構はこれまで詳細に解析されている(図1a).一方で,DNA脱メチル化に関しては,さまざまな機構が提唱されているものの結論にはいたっていない1).DNA脱メチル化には受動的な機構と能動的な機構とが存在する.受動的な脱メチル化とは,DNAが複製されるとき親鎖側のメチル基を娘鎖側にコピーする“維持メチル化”が起こらないことにより娘鎖DNAにシトシンが取り込まれ5-メチルシトシンが減少するものである.他方,能動的な脱メチル化はDNA複製には依存しない機構であり,受精直後の精子ゲノム,始原生殖細胞のゲノムや細胞分化後の一部の遺伝子プロモーターでこのようなDNA脱メチル化が観察されている.現象としてはとらえられているが,実際に生体内でどのような反応によりDNA脱メチル化が起こっているのかは明らかになっておらず,DNA脱メチル化酵素の存在も含めて,その実体は不明である.これまでに,植物では5-メチルシトシンを切除することのできるDNAグリコシラーゼについて複数の報告があるが,哺乳動物ではそれらのホモログは確認されていない1).哺乳動物の能動的な脱メチル化は,1)加水分解によりメチル基を直接に除去する機構,2)AID/APOBECファミリータンパク質に依存的に5-メチルシトシンの脱アミノ化によって形成されるT/Gミスマッチが塩基除去修復によりシトシンに置換される機構,3)メチル基を連続的な酸化反応により脱離する機構,などによって行われるものと推測されている.
本稿では,最近になり同定された,メチル基を酸化(ヒドロキシル化)するTetファミリータンパク質に焦点をあて,そのマウスES細胞あるいは発生初期胚における機能を概説する.
2.Tetファミリータンパク質に依存的なメチル基のヒドロキシル化反応
チミン-7-ヒドロキシラーゼは,O2,Fe2+,および,α-ケトグルタル酸を補因子とし,チミンの5位のメチル基を連続して酸化することによってイソオロチン酸を産生する(図1b).イソオロチン酸は,イソオロチン酸デカルボキシラーゼによってCO2を放出しウラシルに変換される2).チミン-7-ヒドロキシラーゼとイソオロチン酸デカルボキシラーゼは真菌において単離されているが,哺乳動物では同定されていない.しかし,このチミジンサルベージ経路におけるチミンからウラシルへの変換反応は,チミンと5-メチルシトシンの構造上の類似性から,DNA脱メチル化反応のモデルのひとつとして提起されていた3).他方,寄生性原虫であるトリパノソーマには,チミン-7-ヒドロキシラーゼと類似した酸化活性をもつα-ケトグルタル酸依存型ジオキシゲナーゼ,JBPタンパク質が存在する4).2009年,Raoらのグループは,5-メチルシトシンのメチル基を酸化する酵素を同定すべく,JBPタンパク質の酸化反応にヒントを得てα-ケトグルタル酸依存型ジオキシゲナーゼドメインに相同性をもつ哺乳動物ホモログをデータベース検索し,Tetファミリータンパク質Tet1,Tet2,Tet3を同定した5).Tet1は,O2,Fe2+,および,α-ケトグルタル酸に依存的に5-メチルシトシンのメチル基をヒドロキシル化し,5-ヒドロキシメチルシトシン(5hmC)を合成する活性をもつことが明らかとなった(図1c).この5-ヒドロキシメチルシトシンが哺乳動物のゲノムDNAに存在することは1972年に報告されていたが,最近まで,注目されることはなかった6).また,5-ヒドロキシメチルシトシンはプルキンエ細胞,顆粒細胞などの神経細胞やES細胞などに限定的に存在した5,7).
筆者らは,3つのTetファミリータンパク質が同様な活性をもつかどうか検証することから研究をはじめた.ヒト骨肉腫細胞U2OSにマウスTetファミリータンパク質を一過性に発現させ,抗5-メチルシトシン抗体あるいは抗5-ヒドロキシメチルシトシン抗体を用いて細胞染色を行った結果,Tetファミリータンパク質を発現する細胞は5-メチルシトシン染色の強度が減少し,5-ヒドロキシメチルシトシン染色陽性になった.一方で,Fe2+結合ドメインに変異を導入したTetファミリータンパク質を発現させた細胞では,5-メチルシトシン染色の強度に変化は観察されなかった.くわえて,バキュロウイルス発現系により精製したTetファミリータンパク質と5-メチルシトシンを単一に含む二本鎖DNAとを用いたin vitroアッセイによって,Tetファミリータンパク質はO2,Fe2+,および,α-ケトグルタル酸に依存的に5-メチルシトシンを5-ヒドロキシメチルシトシンに変換する活性をもつことが示された.これらの結果から,いずれのTetファミリータンパク質も5-ヒドロキシメチルシトシン合成活性をもつことが示された.
3.Tet1はマウスES細胞の自己複製に必要である
Tetファミリータンパク質の生物学的な機能を理解するため,マウスにおいてさまざまな組織間あるいは細胞間におけるTetファミリーmRNAの発現比較を行った.Tet1はES細胞に特異的に発現しているのに対し,Tet2は幅広い組織で発現していることが明らかとなった.Tet3は,ES細胞では発現せず,肺,膵臓,脾臓などで強い発現がみられた.
Raoらの報告により,ES細胞で5-ヒドロキシメチルシトシンが観察されたことから,どのTetファミリータンパク質がES細胞において機能的に重要かどうかを知るため,RNAi法によってTetファミリータンパク質を発現抑制してその表現型を解析した.siRNAを発現するレンチウイルスをマウスES細胞に感染させ,薬剤で選択したのちTetファミリーmRNAの発現抑制を定量的PCR法により確認した.また,ES細胞の未分化状態を判別する目的でアルカリホスファターゼ染色すると,Tet1ノックダウン細胞は染色が弱く,かつ,細胞形態の変化が観察された.しかしながら,Tet2ノックダウン細胞およびTet3ノックダウン細胞は対照細胞と同様にES細胞に典型的なコロニーを形成した.これらの結果は,Tet1がES細胞を維持するうえで重要な役割をはたしていることを示唆した.事実,Tet1ノックダウンES細胞は細胞増殖能,コロニー形成能が顕著に低下しており,自己複製能に異常のあることが確認された.さらに,Tet1ノックダウンES細胞は対照細胞と比較して栄養外胚葉に特異的なマーカー(Cdx2,Hand1)と原始内胚葉に特異的なマーカー(Gata6,Gata4)とを強く発現しており,分化をしていることが示唆された.しかしながら,Tet1ノックダウンES細胞の多くの集団がES細胞のマーカーであるSSEA-1を発現していることから,Tet1ノックダウンES細胞は自己複製能に欠損のあるものの,ある程度の未分化な状態は維持していることが示唆された.
4.Tet1はNanogの発現を制御する
Tet1がどのようにしてES細胞の自己複製の維持に寄与しているのか,その分子機構を理解するため,Tet1ノックダウンES細胞におけるOct4,Nanog,Sox2など自己複製マーカーの発現レベルをmRNAの定量的PCR法およびウェスタンブロットにより解析した.その結果,対照細胞と比較してTet1ノックダウンES細胞においてOct4,Sox2の発現に変化がない一方で,Nanogの発現レベルに低下が認められた.つぎに,Nanog遺伝子がTet1の標的遺伝子である可能性を考え,クロマチン免疫沈降法を用いてこれを検討した結果,Tet1はNanog遺伝子のコアプロモーターに結合していることが判明した.さらに,Tet1ノックダウンES細胞において,Nanog遺伝子コアプロモーターのDNAメチル化レベルが上昇していた.Nanog遺伝子プロモーターはES細胞では低メチル化状態にあり,分化した細胞ではDNAメチル化をうけて発現抑制されることが報告されていた8).よって,Tet1非存在下ではNanog遺伝子プロモーターはDNAメチル化をうけて発現抑制されていることが示唆された.また,Tet1のノックダウンによるNanogの発現抑制がNanog遺伝子プロモーターのメチル化に依存的な現象であるかどうかを検証するため,3つのDNAメチルトランスフェラーゼ,DNMT1,DNMT3a,DNMT3bをノックアウトしたES細胞においてTet1をノックダウンし,Nanogの発現レベルを解析した.その結果,DNAにメチル基を新規に付与することができないこのノックアウトES細胞では,Tet1の存在の有無にかかわらずNanogを発現することが判明した.
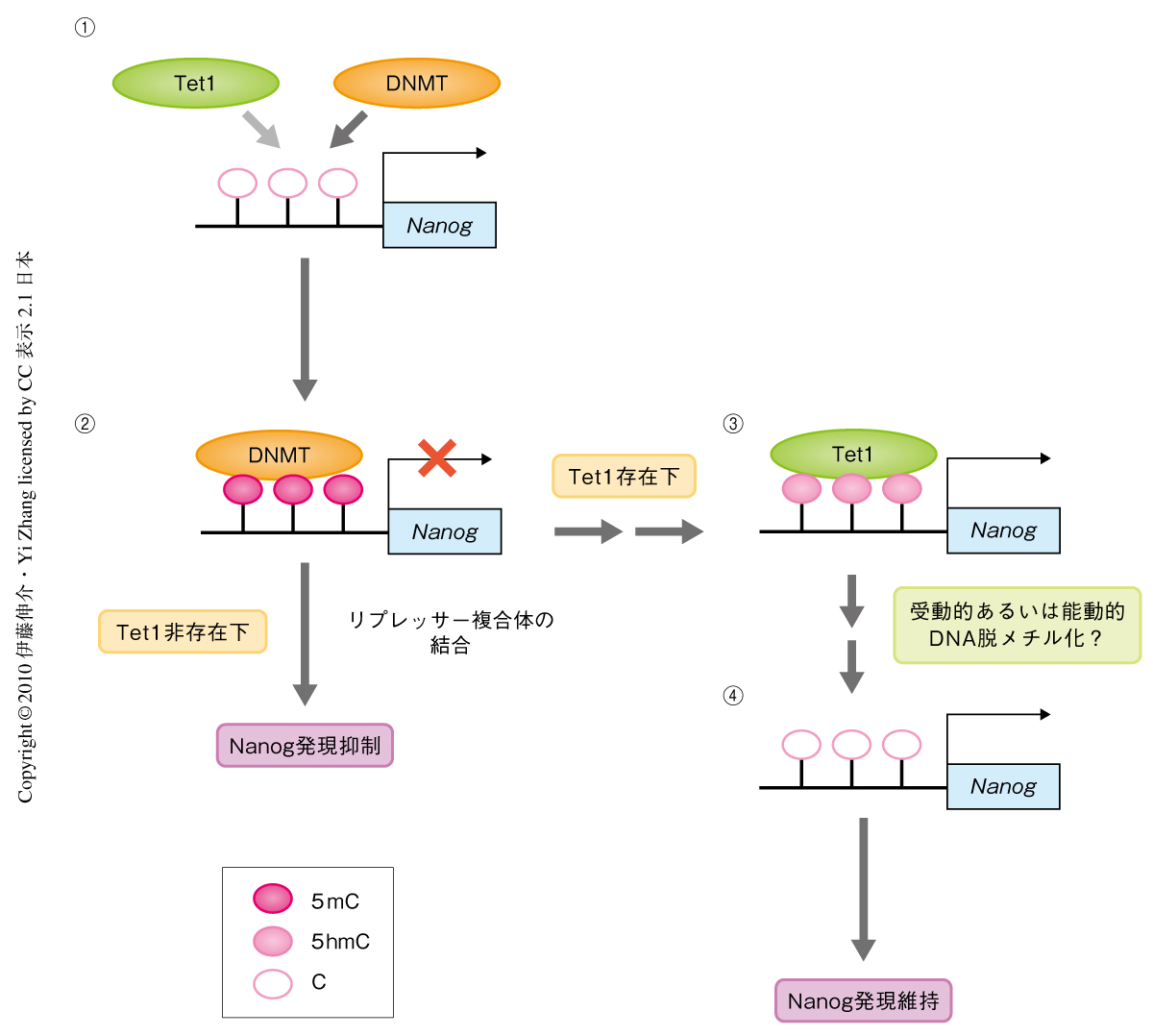
以上の結果より,Tet1はNanog遺伝子コアプロモーターに結合し,そのDNA低メチル化状態を維持して安定な発現を行い,ES細胞を維持していることが明らかになった(図2).また,Tet1ノックダウンES細胞において,Nanogを強制発現させることでTet1ノックダウンES細胞の大部分の欠損表現型を相補できたことから,幹細胞を維持するうえでNanog遺伝子がTet1の主要な標的遺伝子であることがわかった.
5.マウス初期胚におけるTet1
一方,マウス初期胚発生に目をむけると,受精卵は卵割を開始して32細胞期になると栄養外胚葉と内部細胞塊の2種類の細胞系列から構成される胚盤胞になる.これらの過程をとおしてゲノム全体のDNAメチル化レベルは大幅に低下すること9),および,内部細胞塊から樹立されるES細胞の維持にTet1が必要であることを考慮し,受精後の最初の細胞系列の決定にTet1が重要な役割をはたすのではないかとの仮説をたてた.まず,免疫染色により,Tet1は着床前初期胚において核に局在し,胚盤胞期にはおもに内部細胞塊に発現することが確認された.つぎに,2細胞期の1つの細胞にTet1 siRNAとRFP-ヒストンH2B mRNAとをインジェクションし,Tet1をノックダウンした細胞が胚盤胞期において,栄養外胚葉と内部細胞塊のいずれの細胞に寄与するかRFPの蛍光をもとに追跡した.その結果,Tet1をノックダウンした細胞は栄養外胚葉に寄与する割合が高いことが判明し,ES細胞を用いたノックダウン実験と同様の現象が観察された.
以上の結果により,Tet1はES細胞の維持,および,胚盤胞期における内部細胞塊への分化に重要であることが明らかになった.
おわりに
筆者らは,RaoらのグループのTet1発見を発展させ,Tetファミリータンパク質が5-メチルシトシンを5-ヒドロキシメチルシトシンに変換する活性をもつこと,マウスのTet1がES細胞の自己複製の維持に必要であることを明らかにした.しかしながら,自己複製の維持にTet1のヒドロキシラーゼ活性が直接的に関与しているのかどうか,また,5-ヒドロキシメチルシトシンの存在意義,つまり,5-ヒドロキシメチルシトシンがDNA脱メチル化プロセスの中間産物なのか,あるいは,5-ヒドロキシメチルシトシンが最終産物なのかに対し,明白な答えはでていないのが現状である.これまでの報告により,5-ヒドロキシメチルシトシンの特性として,1)メチル化CpG結合タンパク質MeCP2は5-ヒドロキシメチルシトシンを含む二本鎖DNAに対して結合活性が低いこと10),2)DNMT1はDNA複製と共役して親鎖側のメチル基を娘鎖側にコピーするのに対し,親鎖側に5-ヒドロキシメチルシトシンが存在する場合にはメチル基を娘鎖側にコピーすることができないこと11),3)仔ウシ胸腺抽出液中に5-ヒドロキシメチルシトシン特異的なDNAグリコシラーゼ活性が検出されること12),などがある.1)に関しては,5-メチルシトシンを認識して結合する転写リプレッサー複合体は5-ヒドロキシメチルシトシンには結合できず,別の複合体がこれに結合する可能性が示唆される.2)に関しては,5-ヒドロキシメチルシトシンが維持メチル化機構に対して抑制的に作用する結果,受動的な脱メチル化にいたることが考えられる.3)に関しては,5-ヒドロキシメチルシトシングリコシラーゼが5-ヒドロキシメチルシトシンを切除し,塩基除去修復によってDNA脱メチル化の起こることが示唆される.いずれの場合においても,5-ヒドロキシメチルシトシンは新たなエピジェネティック修飾のひとつとして,5-メチルシトシンとは異なったアウトプットを提示することが予想される.今後のさらなる解析によって,生体内における5-ヒドロキシメチルシトシンの存在意義の明らかになることが期待される.
文 献
- Ooi, S. K. & Bestor, T. H.: The colorful history of active DNA demethylation. Cell, 133, 1145-1148 (2008)[PubMed]
- Warn-Cramer, B. J., Macrander, L. A. & Abbott, M. T.: Markedly different ascorbate dependencies of the sequential alpha-ketoglutarate dioxygenase reactions catalyzed by an essentially homogeneous thymine 7-hydroxylase from Rhodotorula glutinis. J. Biol. Chem., 258, 10551-10557 (1983)[PubMed]
- Wu, S. C. & Zhang, Y.: Active DNA demethylation: many roads lead to Rome. Nat. Rev. Mol. Cell Biol., 11, 607-620 (2010)[PubMed]
- Yu, Z. et al.: The protein that binds to DNA base J in trypanosomatids has features of a thymidine hydroxylase. Nucleic Acids Res., 35, 2107-2115 (2007)[PubMed]
- Tahiliani, M. et al.: Conversion of 5-methylcytosine to 5-hydroxymethylcytosine in mammalian DNA by MLL partner TET1. Science, 324, 930-935 (2009)[PubMed]
- Penn, N. W. et al.: The presence of 5-hydroxymethylcytosine in animal deoxyribonucleic acid. Biochem. J., 126, 781-790 (1972)[PubMed]
- Kriaucionis, S. & Heintz, N.: The nuclear DNA base 5-hydroxymethylcytosine is present in Purkinje neurons and the brain. Science, 324, 929-930 (2009)[PubMed]
- Hattori, N. et al.: Epigenetic regulation of Nanog gene in embryonic stem and trophoblast stem cells. Genes Cells, 12, 387-396 (2007)[PubMed]
- Reik, W., Dean, W. & Walter, J.: Epigenetic reprogramming in mammalian development. Science, 293, 1089-1093 (2001)[PubMed]
- Valinluck, V. et al.: Oxidative damage to methyl-CpG sequences inhibits the binding of the methyl-CpG binding domain (MBD) of methyl-CpG binding protein 2 (MeCP2). Nucleic Acids Res., 32, 4100-4108 (2004)[PubMed]
- Valinluck, V. & Sowers, L. C.: Endogenous cytosine damage products alter the site selectivity of human DNA maintenance methyltransferase DNMT1. Cancer Res., 67, 946-950 (2007)[PubMed]
- Cannon, S. V., Cummings, A. & Teebor, G. W.: 5-Hydroxymethylcytosine DNA glycosylase activity in mammalian tissue. Biochem. Biophys. Res. Commun., 151, 1173-1179 (1988)[PubMed]
著者プロフィール
略歴:2007年 大阪大学大学院生命機能研究科 修了,同 特任研究員,大阪大学大学院基礎工学研究科 研究員(倉岡 功准教授)を経て,2008年より米国North Carolina大学Chapel Hill校 研究員(Yi Zhang教授).
研究テーマ:哺乳動物におけるDNA脱メチル化機構の解析.
抱負:in vitroでDNA脱メチル化活性を検出したい.
Yi Zhang
米国North Carolina大学Chapel Hill校 教授
研究室URL:http://www.med.unc.edu/~zhangyi/lab.htm
© 2010 伊藤伸介・Yi Zhang Licensed under CC 表示 2.1 日本