光駆動性の陽イオンチャネルであるチャネルロドプシンの結晶構造からその陽イオンの輸送経路と分子機構の一端を解明
加藤英明・石谷隆一郎・濡木 理
(東京大学大学院理学系研究科 生物化学専攻)
email:加藤英明,石谷隆一郎,濡木 理
DOI: 10.7875/first.author.2012.019
Crystal structure of the channelrhodopsin light-gated cation channel.
Hideaki E. Kato, Feng Zhang, Ofer Yizhar, Charu Ramakrishnan, Tomohiro Nishizawa, Kunio Hirata, Jumpei Ito, Yusuke Aita, Tomoya Tsukazaki, Shigehiko Hayashi, Peter Hegemann, Andrés D. Maturana, Ryuichiro Ishitani, Karl Deisseroth, Osamu Nureki
Nature, 482, 369-374 (2012)
緑藻類から単離された光駆動性の陽イオンチャネルであるチャネルロドプシンは,青色光を吸収すると陽イオン,とくにNa+を取り込むという性質をもつ.そのため,このタンパク質をニューロンに発現させ青色光を照射するとおもにNa+が細胞内に流入する結果,脱分極が生じニューロンは興奮する.この性質に着目することで,チャネルロドプシンは自由行動を行っている生物においてニューロンの集団を非常に高い時間分解能および空間分解能で興奮させることのできる有用なツールとして,2005年以降,利用されつづけてきた.しかし,その有用性の認知と応用例の増加とは裏腹に,チャネルロドプシンの分子機構については現在まで驚くほどその知見が不足していた.今回,筆者らは,チャネルロドプシンの結晶構造を2.3Åという高分解能で決定した.さらに,この結晶構造と電気生理学的な解析の結果,発色団であるレチナールの結合部位の詳細な構造や長らく論争となってきたチャネルロドプシンのイオン輸送経路を解明し,同時に,チャネルロドプシンの初期反応を明らかにすることに成功した.今回の結果は,光エネルギーを陽イオンの輸送に変換する分子機構の一端を明らかにしたというだけでなく,神経生物学のツールとしてより有用な変異型チャネルロドプシンをデザインするため必要な構造情報を提供したという点にも大きな意義がある.
ヒトから微生物まであらゆる生物は光を受容し,その光情報に応じた行動をとる.多くの場合,この光情報の受容は発色団としてレチナールとよばれる低分子化合物を結合したロドプシンファミリータンパク質により担われている.たとえば,ヒトの眼のなかにある動物型ロドプシン(ロドプシン)は光を吸収するとセカンドメッセンジャーである三量体Gタンパク質を活性化することでヒトの視覚の形成に重要な役割をはたす.また,一部の微生物がもつ微生物型ロドプシン(バクテリオロドプシンなど)は光を吸収すると細胞外へプロトンを汲み出しプロトン濃度勾配を形成することで,とくに嫌気性条件でのエネルギーの獲得に重要なはたらきを示す.このように,ひとくちにロドプシンファミリータンパク質といってもその機能は多岐にわたることが知られていたが,イオンチャネル,とくに,陽イオンチャネルとしてはたらくロドプシンファミリータンパク質は発見されておらず,また,すでに構造が明らかになっていたロドプシンファミリータンパク質からの演繹から,陽イオンチャネルとしてはたらくロドプシンファミリータンパク質というのは原理的にむずかしいのではないかと考える研究者も少なからず存在していた.しかし,1995年,ドイツの研究グループが緑藻類の走光性にかかわる新規の微生物型ロドプシンを発見し,2002年に,電気生理学的な解析によりこのタンパク質が陽イオンチャネルとしてはたらくことを示したことにより,陽イオンチャネル型ロドプシンファミリータンパク質が実際に存在することが明らかになった1).これがチャネルロドプシンである.
青色光を照射すると細胞内に陽イオンを取り込むという性質から,チャネルロドプシンはロドプシン研究者からのみならず神経科学者からの注目も集めることになる.2005年から2006年にかけて,3つの研究グループが,チャネルロドプシンを発現させたニューロンに青色光を照射してこれを興奮させることに成功した.2007年には,生きたマウスのニューロンにチャネルロドプシンを発現させ,光ファイバーを脳内に挿入することでこれを興奮させてマウスの行動を制御することに成功した2).これ以降,チャネルロドプシンを用いた神経科学分野における光遺伝学(optogenetics,オプトジェネティクス)の研究例は現在まで飛躍的に増加しつづけてきた.しかし,こうした研究例の増加とは裏腹に,チャネルロドプシンの分子機構,すなわち,このタンパク質がどうして光を吸収すると陽イオンを透過させるようになるのか,また,そもそも陽イオンはこのタンパク質のどこを透過するのかといった問題には不明な点が多く,ほとんど知見は得られていなかった.また,チャネルロドプシンが神経科学における有用なツールとして認識されはじめて以降,チャネルロドプシンの性質を改善しより使いやすい変異型チャネルロドプシンを創出しようという研究の流れが生まれたが3),構造が既知である微生物型ロドプシンから得られる情報だけでは変異体のデザインには限界があり,チャネルロドプシンそのものの構造情報が待ち望まれていた.
膜タンパク質,とくに真核生物に由来する膜タンパク質は,一般に高品質のタンパク質を大量に調製することが困難である.緑藻類から単離された野生型のチャネルロドプシンは発現量が低くその性質も良好ではなかったため,筆者らは,既知の4種のチャネルロドプシンに関して多数のキメラ体を作製し,その発現量と性質をC末端側に融合させた蛍光タンパク質EGFPの蛍光により評価した(FSEC法4)).発現量および性質においてもっとも良好であったキメラ体に関して,三次元的に連続した脂質膜のなかに膜タンパク質を再構成してから結晶化する脂質キュービック法を適用して結晶化を行ったところ,X線結晶構造解析に適した良質な結晶を得ることに成功した.そののち,水銀化合物との共結晶に関し多波長異常分散法を用いて位相決定を行い,最終的には2.3Åという高分解能で結晶構造を決定することに成功した(PDB ID:3UG9).
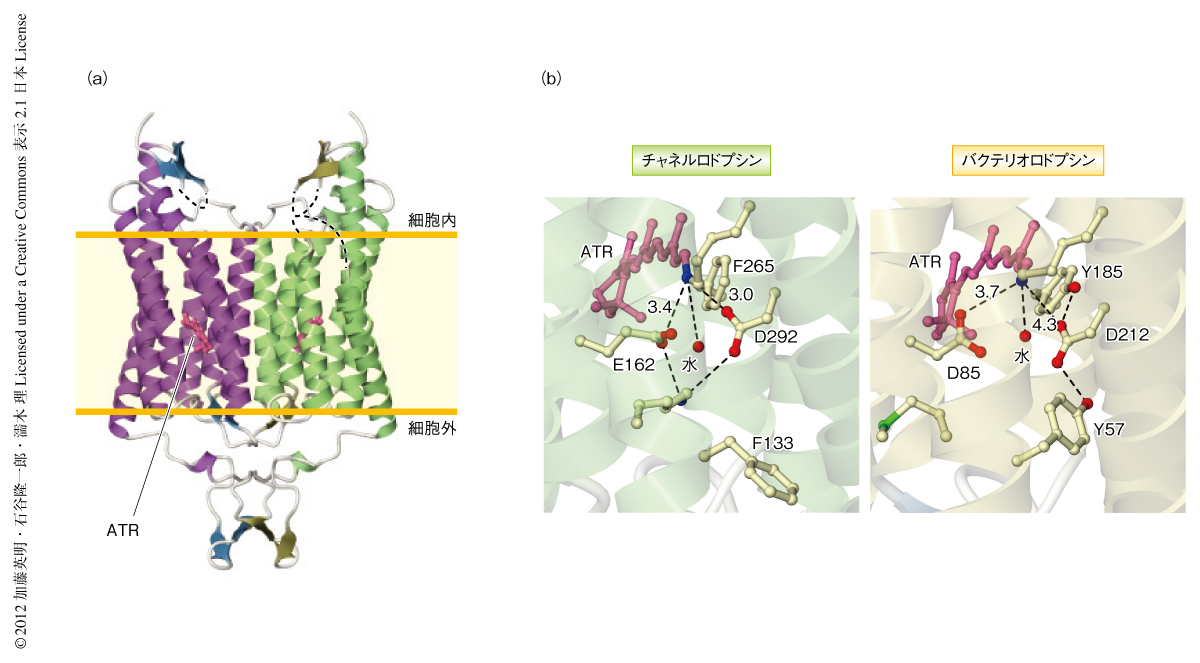
チャネルロドプシンはN末端側の細胞外ドメイン(Nドメイン),7回膜貫通領域,C末端側の細胞内ドメイン(Cドメイン)により構成されており,ほかの微生物型ロドプシンが三量体構造や四量体構造を形成しているのと対照的に,二量体構造を形成していた(図1a).また,二量体のあいだには3箇所のジスルフィド結合が形成されていたため,この二量体構造は結晶化によるアーティファクトではないと考えられた.また,このチャネルロドプシンの構造をこれまでもっともよく研究されている微生物型ロドプシンであるバクテリオロドプシンと比較したところ,両者の構造はレチナールの位置を含め非常によく一致していることがわかった.しかし,チャネルロドプシンにはバクテリオロドプシンに存在しない細胞外ドメインおよび細胞内ドメインが存在していた点,2本のαヘリックスがバクテリオロドプシンと比較して外側に大きく傾いていた点などが異なっていた.
あらゆる微生物型ロドプシンにおいて,発色団である全trans型レチナールはタンパク質部分のもつ特定のLys残基とシッフ塩基結合を形成しており,暗状態ではこのシッフ塩基の窒素原子がプロトン化されていることが知られている.青色光が全trans型レチナールに照射されると全trans型レチナールは13-cis-型レチナールに異性化され,シッフ塩基のプロトンはプロトン受容基としてはたらく酸性アミノ酸残基へと移動する.これがチャネルロドプシンをはじめ多くの微生物型ロドプシンで起こる光サイクルの初期反応である.バクテリオロドプシンの場合,シッフ塩基の近傍にはAsp85とAsp212の2つの酸性アミノ酸残基が存在しているが,主たるプロトン受容基としてはたらくのはAsp85であることが知られている5).この理由には,Asp85がAsp212よりシッフ塩基に近い点,Asp212が2つのTyr残基(Tyr57,Tyr185)により位置を固定されているため光サイクルにおいてpKaを変化させてプロトンを受け取ったり離したりすることができない点,などがあげられる.しかし,チャネルロドプシンではAsp85に対応するGlu162よりもAsp212に対応するAsp292のほうがわずかにシッフ塩基との距離が近く,また,2つのTyr残基はPhe残基(Phe133,Phe265)に置換されていた(図1b).そのため,Asp292は光サイクルにおいて比較的自由にその位置を変え,pKaを変化させることでシッフ塩基のプロトン受容基としてはたらいている可能性が考えられた.Glu162およびAsp292をそれぞれAla残基に置換した変異体を作製しその性質を調べたところ,Asp292をAla残基に置換した変異体ではイオン電流が著しく低下し光照射からチャネル孔が開くまでの時間も長くなることがわかった.これらの実験結果は,バクテリオロドプシンにおいてプロトン受容基としてはたらくAsp85に対応するGlu162ではなく,Asp212に対応するAsp292こそがチャネルロドプシンのプロトン受容基だろう,という筆者らの仮説を強く支持するものであった.
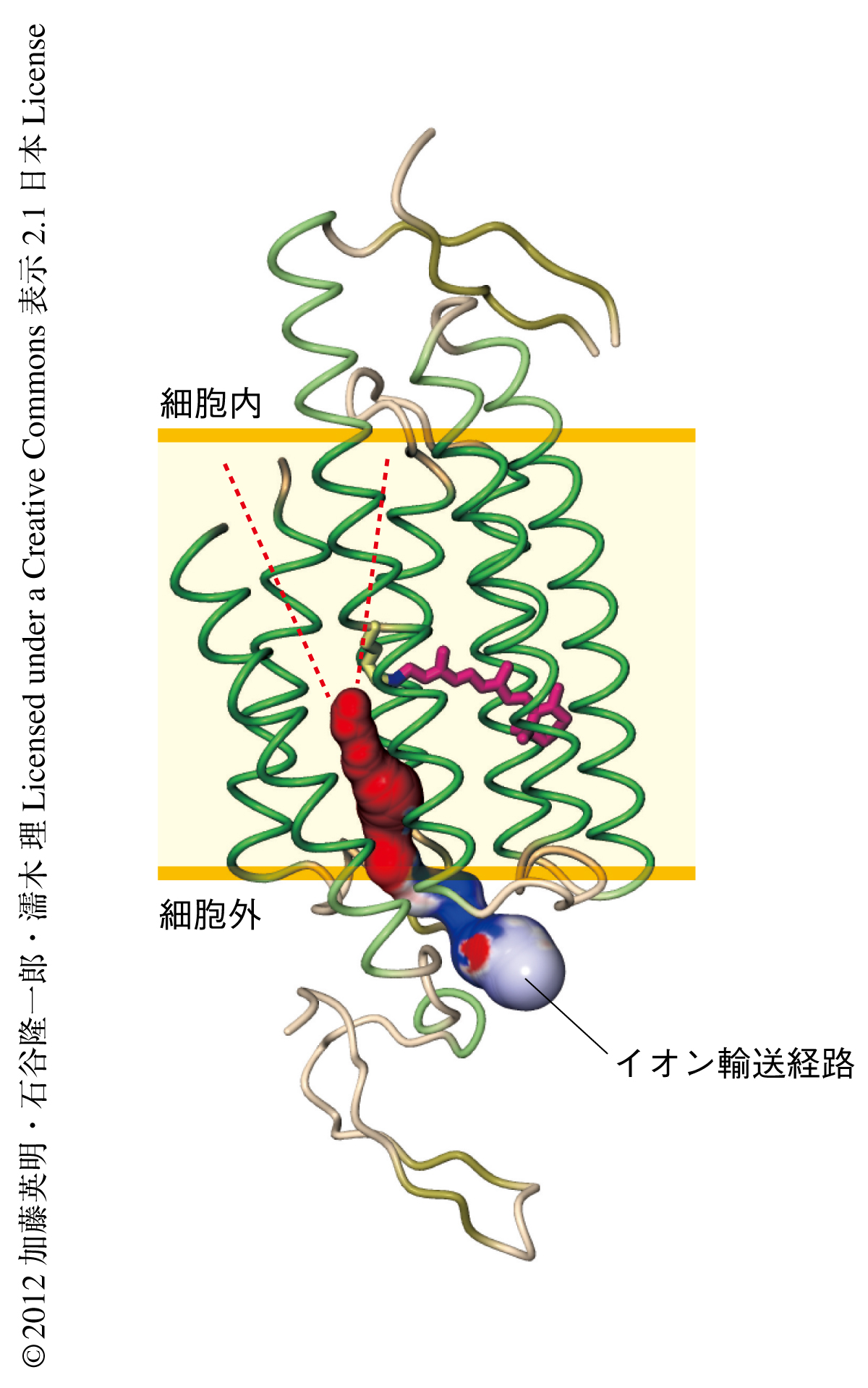
チャネルロドプシンの分子機構を理解するためには,実際にイオンがどこを透過するのか,その輸送経路を解明することが必要不可欠である.先行研究ではチャネルロドプシンのイオン輸送経路は二量体の境界面にあるという説と単量体のなかに存在しているという説が入り乱れていたが,どちらの説が正しいのか決定的なデータは得られていなかった6).得られた結晶構造をもとにチャネルロドプシンの分子表面を描いたところ,二量体の境界面にはイオンの透過できそうな空間は存在せず,また,その境界面に並んでいる残基はどれも疎水性の残基であった一方で,単量体の内部の4つのαヘリックスにより囲まれた領域には強い負電荷を帯びた空間が存在していることがわかった(図2).この空間はバクテリオロドプシンと比較して外側に傾いている2本のαヘリックスにより形成されていたため,この空間はチャネルロドプシンに特有のものであり,イオンの透過に重要である可能性が高いものと考えられた.実際,この経路に存在する4つのアミノ酸残基をAla残基に置換した変異体を作製しそのNa+電流を測定したところ,酸性アミノ酸残基をAla残基に置換した3つの変異体ではどれもNa+電流が低下した.また,4つの残基のうち3つの残基についてはAla残基に置換したことによりイオンの選択性が大きく変化した.これらの結果から,チャネルロドプシンのイオン輸送経路はこの4本のαヘリックスにより囲まれた領域,つまり,二量体の境界面ではなく単量体の内部に存在している可能性が強く示唆された.
今回の研究で明らかにされたのはチャネルロドプシンの暗状態,つまり,閉状態の構造であった.そのため,チャネルロドプシンのイオン輸送経路は細胞の外側には開いていたが,細胞の内側では2つの狭窄部位により閉じていた.ひとつ目の狭窄部位は輸送経路の中央付近に存在しており,保存されたGlu129が孔をふさぐかたちで突き出すことにより形成されていた.もうひとつの狭窄部位は細胞の内側に存在しており,Glu129と同様に高度に保存されたTyr109が孔にはまり込むことにより形成されていた.これら2つの狭窄部位がどのように動くことでチャネル孔が開くのかについては不明な点が多い.しかし,Tyr109の存在するαヘリックスは非常に温度因子が高く,生体においてこのヘリックスが動くことによりTyr109が孔から外れることが予想された.また,Glu129は暗状態ではプロトン化されていることが報告されており全trans型レチナールとの距離も比較的近いため,全trans型レチナールへのプロトン供与基としてはたらいている可能性が考えられた.
筆者のまわりから実際に構造が解けるまでの苦労話をくわしく聞きたい! という声を多数いただいたので,せっかくなので期待に応えてみたい.いま思い返せば,苦労は大別して3段階ほどあった気がする.発現系の構築,結晶化法の導入,位相決定,である.
1つ目は発現系の構築.そもそも,筆者が修士課程の大学院生として研究室に所属した3年前,真核生物の膜タンパク質の構造を解いたことのある人は研究室には誰もおらず,大腸菌以外の宿主で膜タンパク質を発現させたことのある人もいなかった.そのため,まずは大腸菌を用いてチャネルロドプシンを発現させようとしたのだが,数百以上の条件を試してみてもさっぱりうまくいかない.結局,培養細胞や昆虫細胞を試すことになったのだが,当時,培養細胞を培養するシェイカーすら研究室にはない状態だったので,ちょうど同じ年に研究室に移ってきたポスドクの方にひとつひとつ教えていただきながら系を立ち上げることになった.当時は,同期の修士課程の大学院生が構造を解いていくなか,目的のタンパク質を発現させることすらできずに1年近くも時間を浪費している自分が本当に嫌になったものである.
チャネルロドプシンの発現系の構築に成功し,精製もうまくいった.さぁ,これで結晶化だ,というところで再び問題が起こった.蒸気拡散法を用いて得られた結晶はX線を当てても当てても反射が出なかったのである.結晶化の条件の最適化や界面活性剤の交換をしてみてもまったくだめだった.15Åとか10Åとかいうレベルではない.No diff.である.そのため,もともと微生物型ロドプシンの結晶化法として考案されGタンパク質共役受容体の結晶化法として再評価されつつあった脂質キュービック法の導入を決意することになった.いまにしてみると,蒸気拡散法で得た結晶からまったく反射が出なかったのが,かえって脂質キュービック法を導入する決断を早めてくれたように思う.京都大学大学院医学研究科の岩田研究室に直接実験を教わりに行き,米国Scripps Research Instituteの研究グループにメールで疑問点をたずね,試行錯誤でこの結晶化法を立ち上げたが,はじめてチャネルロドプシンのオレンジ色の結晶を見たときは手が震えてプレートの焦点がうまく合わせられなかった.そして,当時,立ち上がったばかりの大型放射光施設SPring-8のBL32XUビームラインで測定を行った際,最初の結晶で一面に反射が見えたとき(3Åくらいは出ていた)は一瞬息が止まったのを覚えている.それ以来,筆者はBL32XUビームラインの虜である.
最後のハードルは位相決定の段階で待ち構えていた.無事,ネイティブ結晶のデータセットをとることはできたのだが,分子置換により位相を決定することができなかったのである.当然ながら,重原子を利用して位相を決めようということになったが,脂質キュービック法で得られた結晶について分子置換以外の方法で位相を決定した例はそれまでなかった.脂質キュービック法で得られた結晶はしばしば脂質に由来する反射が4.4Å~4.6Åの範囲に現われてタンパク質に由来する反射を埋もれさせてしまうことがあり,重原子による異常分散を利用した位相決定が本当に可能なのだろうかという疑問は筆者を悩ませた.そもそも,セレノメチオニンが効率よくチャネルロドプシンに導入できなかったという問題もあった.結局,この問題には半年以上も悩まされることになったわけだが,現状打破のきっかけは,いろいろな重原子化合物とチャネルロドプシンとを混ぜ合わせたとき,いくつかの水銀化合物を混ぜたときだけ試料の色がオレンジから赤に変わったことであった.試料の色が変わったということは水銀がレチナールの近くに結合しているせいではないだろうか.水銀ならいけるのではないか.最終的にこの判断が功を奏し,水銀を利用した多波長異常分散法により位相を決定することができたのだが,得られた構造をみるとレチナールのπ電子系と相互作用するCys残基に確かに水銀が結合しているのを確認することができた.また,いま思えば,BL32XUビームラインのマイクロビームを使うことでひとつの結晶から十分な冗長性をもつデータセットをとることができたことも重要な要因であった.
筆者の苦労話はせいぜいこの3つ,あとは,フランスやドイツ,米国や日本など,各地に競争相手がいると聞いていたため,しばしば胃がキリキリと痛んだことくらいである.しかし,蓋を開けてみれば,スタートしてから3年でチャネルロドプシンの構造を決定することができた.ひとえに研究室のメンバーやビームラインのスタッフの方々の厚意と協力があったからこそだと思い深く感謝している.
さて,実は,原著論文の初期の草稿にはゲート機構に関するつづきの記述があった.リバイスの過程でレフリーに“speculativeなので削除しなさい”といわれ泣く泣く削ったのだが,ちょうど原著論文がオンラインで出版される2週間前に,別のグループが同じ予測を打ち立ててJornal of Biological Chemistry誌に論文を掲載してしまった7).筆者としては少し悔しい想いであったが,予測されたゲート機構を実証するにはまださまざまな実験が必要となるので,今後はゲート機構の実証へと歩を進ませたいと考えている.また,明らかになった構造をもとに性質を改善させた変異型チャネルロドプシンも実際に作製したい.やるべきことはまだまだ山積みである.
略歴:東京大学理学系研究科博士課程 在学中.
研究テーマ:膜タンパク質の立体構造解析.
抱負:結晶構造解析を主眼におきつつも,幅広い手法を身につけながら複雑な分子機械である膜タンパク質を静的および動的にとらえ,その分子機構にせまっていきたい.
石谷 隆一郎(Ryuichiro Ishitani)
東京大学大学院理学系研究科 准教授.
濡木 理(Osamu Nureki)
東京大学大学院理学系研究科 教授.
研究室URL:http://www.nurekilab.net/
© 2012 加藤英明・石谷隆一郎・濡木 理 Licensed under CC 表示 2.1 日本
(東京大学大学院理学系研究科 生物化学専攻)
email:加藤英明,石谷隆一郎,濡木 理
DOI: 10.7875/first.author.2012.019
Crystal structure of the channelrhodopsin light-gated cation channel.
Hideaki E. Kato, Feng Zhang, Ofer Yizhar, Charu Ramakrishnan, Tomohiro Nishizawa, Kunio Hirata, Jumpei Ito, Yusuke Aita, Tomoya Tsukazaki, Shigehiko Hayashi, Peter Hegemann, Andrés D. Maturana, Ryuichiro Ishitani, Karl Deisseroth, Osamu Nureki
Nature, 482, 369-374 (2012)
要 約
緑藻類から単離された光駆動性の陽イオンチャネルであるチャネルロドプシンは,青色光を吸収すると陽イオン,とくにNa+を取り込むという性質をもつ.そのため,このタンパク質をニューロンに発現させ青色光を照射するとおもにNa+が細胞内に流入する結果,脱分極が生じニューロンは興奮する.この性質に着目することで,チャネルロドプシンは自由行動を行っている生物においてニューロンの集団を非常に高い時間分解能および空間分解能で興奮させることのできる有用なツールとして,2005年以降,利用されつづけてきた.しかし,その有用性の認知と応用例の増加とは裏腹に,チャネルロドプシンの分子機構については現在まで驚くほどその知見が不足していた.今回,筆者らは,チャネルロドプシンの結晶構造を2.3Åという高分解能で決定した.さらに,この結晶構造と電気生理学的な解析の結果,発色団であるレチナールの結合部位の詳細な構造や長らく論争となってきたチャネルロドプシンのイオン輸送経路を解明し,同時に,チャネルロドプシンの初期反応を明らかにすることに成功した.今回の結果は,光エネルギーを陽イオンの輸送に変換する分子機構の一端を明らかにしたというだけでなく,神経生物学のツールとしてより有用な変異型チャネルロドプシンをデザインするため必要な構造情報を提供したという点にも大きな意義がある.
はじめに
ヒトから微生物まであらゆる生物は光を受容し,その光情報に応じた行動をとる.多くの場合,この光情報の受容は発色団としてレチナールとよばれる低分子化合物を結合したロドプシンファミリータンパク質により担われている.たとえば,ヒトの眼のなかにある動物型ロドプシン(ロドプシン)は光を吸収するとセカンドメッセンジャーである三量体Gタンパク質を活性化することでヒトの視覚の形成に重要な役割をはたす.また,一部の微生物がもつ微生物型ロドプシン(バクテリオロドプシンなど)は光を吸収すると細胞外へプロトンを汲み出しプロトン濃度勾配を形成することで,とくに嫌気性条件でのエネルギーの獲得に重要なはたらきを示す.このように,ひとくちにロドプシンファミリータンパク質といってもその機能は多岐にわたることが知られていたが,イオンチャネル,とくに,陽イオンチャネルとしてはたらくロドプシンファミリータンパク質は発見されておらず,また,すでに構造が明らかになっていたロドプシンファミリータンパク質からの演繹から,陽イオンチャネルとしてはたらくロドプシンファミリータンパク質というのは原理的にむずかしいのではないかと考える研究者も少なからず存在していた.しかし,1995年,ドイツの研究グループが緑藻類の走光性にかかわる新規の微生物型ロドプシンを発見し,2002年に,電気生理学的な解析によりこのタンパク質が陽イオンチャネルとしてはたらくことを示したことにより,陽イオンチャネル型ロドプシンファミリータンパク質が実際に存在することが明らかになった1).これがチャネルロドプシンである.
青色光を照射すると細胞内に陽イオンを取り込むという性質から,チャネルロドプシンはロドプシン研究者からのみならず神経科学者からの注目も集めることになる.2005年から2006年にかけて,3つの研究グループが,チャネルロドプシンを発現させたニューロンに青色光を照射してこれを興奮させることに成功した.2007年には,生きたマウスのニューロンにチャネルロドプシンを発現させ,光ファイバーを脳内に挿入することでこれを興奮させてマウスの行動を制御することに成功した2).これ以降,チャネルロドプシンを用いた神経科学分野における光遺伝学(optogenetics,オプトジェネティクス)の研究例は現在まで飛躍的に増加しつづけてきた.しかし,こうした研究例の増加とは裏腹に,チャネルロドプシンの分子機構,すなわち,このタンパク質がどうして光を吸収すると陽イオンを透過させるようになるのか,また,そもそも陽イオンはこのタンパク質のどこを透過するのかといった問題には不明な点が多く,ほとんど知見は得られていなかった.また,チャネルロドプシンが神経科学における有用なツールとして認識されはじめて以降,チャネルロドプシンの性質を改善しより使いやすい変異型チャネルロドプシンを創出しようという研究の流れが生まれたが3),構造が既知である微生物型ロドプシンから得られる情報だけでは変異体のデザインには限界があり,チャネルロドプシンそのものの構造情報が待ち望まれていた.
1.チャネルロドプシンの発現と構造決定
膜タンパク質,とくに真核生物に由来する膜タンパク質は,一般に高品質のタンパク質を大量に調製することが困難である.緑藻類から単離された野生型のチャネルロドプシンは発現量が低くその性質も良好ではなかったため,筆者らは,既知の4種のチャネルロドプシンに関して多数のキメラ体を作製し,その発現量と性質をC末端側に融合させた蛍光タンパク質EGFPの蛍光により評価した(FSEC法4)).発現量および性質においてもっとも良好であったキメラ体に関して,三次元的に連続した脂質膜のなかに膜タンパク質を再構成してから結晶化する脂質キュービック法を適用して結晶化を行ったところ,X線結晶構造解析に適した良質な結晶を得ることに成功した.そののち,水銀化合物との共結晶に関し多波長異常分散法を用いて位相決定を行い,最終的には2.3Åという高分解能で結晶構造を決定することに成功した(PDB ID:3UG9).
2.チャネルロドプシンの全体構造とバクテリオロドプシンとの比較
チャネルロドプシンはN末端側の細胞外ドメイン(Nドメイン),7回膜貫通領域,C末端側の細胞内ドメイン(Cドメイン)により構成されており,ほかの微生物型ロドプシンが三量体構造や四量体構造を形成しているのと対照的に,二量体構造を形成していた(図1a).また,二量体のあいだには3箇所のジスルフィド結合が形成されていたため,この二量体構造は結晶化によるアーティファクトではないと考えられた.また,このチャネルロドプシンの構造をこれまでもっともよく研究されている微生物型ロドプシンであるバクテリオロドプシンと比較したところ,両者の構造はレチナールの位置を含め非常によく一致していることがわかった.しかし,チャネルロドプシンにはバクテリオロドプシンに存在しない細胞外ドメインおよび細胞内ドメインが存在していた点,2本のαヘリックスがバクテリオロドプシンと比較して外側に大きく傾いていた点などが異なっていた.
3.初期反応に重要な役割をはたすプロトン受容基の同定
あらゆる微生物型ロドプシンにおいて,発色団である全trans型レチナールはタンパク質部分のもつ特定のLys残基とシッフ塩基結合を形成しており,暗状態ではこのシッフ塩基の窒素原子がプロトン化されていることが知られている.青色光が全trans型レチナールに照射されると全trans型レチナールは13-cis-型レチナールに異性化され,シッフ塩基のプロトンはプロトン受容基としてはたらく酸性アミノ酸残基へと移動する.これがチャネルロドプシンをはじめ多くの微生物型ロドプシンで起こる光サイクルの初期反応である.バクテリオロドプシンの場合,シッフ塩基の近傍にはAsp85とAsp212の2つの酸性アミノ酸残基が存在しているが,主たるプロトン受容基としてはたらくのはAsp85であることが知られている5).この理由には,Asp85がAsp212よりシッフ塩基に近い点,Asp212が2つのTyr残基(Tyr57,Tyr185)により位置を固定されているため光サイクルにおいてpKaを変化させてプロトンを受け取ったり離したりすることができない点,などがあげられる.しかし,チャネルロドプシンではAsp85に対応するGlu162よりもAsp212に対応するAsp292のほうがわずかにシッフ塩基との距離が近く,また,2つのTyr残基はPhe残基(Phe133,Phe265)に置換されていた(図1b).そのため,Asp292は光サイクルにおいて比較的自由にその位置を変え,pKaを変化させることでシッフ塩基のプロトン受容基としてはたらいている可能性が考えられた.Glu162およびAsp292をそれぞれAla残基に置換した変異体を作製しその性質を調べたところ,Asp292をAla残基に置換した変異体ではイオン電流が著しく低下し光照射からチャネル孔が開くまでの時間も長くなることがわかった.これらの実験結果は,バクテリオロドプシンにおいてプロトン受容基としてはたらくAsp85に対応するGlu162ではなく,Asp212に対応するAsp292こそがチャネルロドプシンのプロトン受容基だろう,という筆者らの仮説を強く支持するものであった.
4.イオン輸送経路の解明
チャネルロドプシンの分子機構を理解するためには,実際にイオンがどこを透過するのか,その輸送経路を解明することが必要不可欠である.先行研究ではチャネルロドプシンのイオン輸送経路は二量体の境界面にあるという説と単量体のなかに存在しているという説が入り乱れていたが,どちらの説が正しいのか決定的なデータは得られていなかった6).得られた結晶構造をもとにチャネルロドプシンの分子表面を描いたところ,二量体の境界面にはイオンの透過できそうな空間は存在せず,また,その境界面に並んでいる残基はどれも疎水性の残基であった一方で,単量体の内部の4つのαヘリックスにより囲まれた領域には強い負電荷を帯びた空間が存在していることがわかった(図2).この空間はバクテリオロドプシンと比較して外側に傾いている2本のαヘリックスにより形成されていたため,この空間はチャネルロドプシンに特有のものであり,イオンの透過に重要である可能性が高いものと考えられた.実際,この経路に存在する4つのアミノ酸残基をAla残基に置換した変異体を作製しそのNa+電流を測定したところ,酸性アミノ酸残基をAla残基に置換した3つの変異体ではどれもNa+電流が低下した.また,4つの残基のうち3つの残基についてはAla残基に置換したことによりイオンの選択性が大きく変化した.これらの結果から,チャネルロドプシンのイオン輸送経路はこの4本のαヘリックスにより囲まれた領域,つまり,二量体の境界面ではなく単量体の内部に存在している可能性が強く示唆された.
5.輸送経路に存在する2つの狭窄部位とその役割
今回の研究で明らかにされたのはチャネルロドプシンの暗状態,つまり,閉状態の構造であった.そのため,チャネルロドプシンのイオン輸送経路は細胞の外側には開いていたが,細胞の内側では2つの狭窄部位により閉じていた.ひとつ目の狭窄部位は輸送経路の中央付近に存在しており,保存されたGlu129が孔をふさぐかたちで突き出すことにより形成されていた.もうひとつの狭窄部位は細胞の内側に存在しており,Glu129と同様に高度に保存されたTyr109が孔にはまり込むことにより形成されていた.これら2つの狭窄部位がどのように動くことでチャネル孔が開くのかについては不明な点が多い.しかし,Tyr109の存在するαヘリックスは非常に温度因子が高く,生体においてこのヘリックスが動くことによりTyr109が孔から外れることが予想された.また,Glu129は暗状態ではプロトン化されていることが報告されており全trans型レチナールとの距離も比較的近いため,全trans型レチナールへのプロトン供与基としてはたらいている可能性が考えられた.
おわりに
筆者のまわりから実際に構造が解けるまでの苦労話をくわしく聞きたい! という声を多数いただいたので,せっかくなので期待に応えてみたい.いま思い返せば,苦労は大別して3段階ほどあった気がする.発現系の構築,結晶化法の導入,位相決定,である.
1つ目は発現系の構築.そもそも,筆者が修士課程の大学院生として研究室に所属した3年前,真核生物の膜タンパク質の構造を解いたことのある人は研究室には誰もおらず,大腸菌以外の宿主で膜タンパク質を発現させたことのある人もいなかった.そのため,まずは大腸菌を用いてチャネルロドプシンを発現させようとしたのだが,数百以上の条件を試してみてもさっぱりうまくいかない.結局,培養細胞や昆虫細胞を試すことになったのだが,当時,培養細胞を培養するシェイカーすら研究室にはない状態だったので,ちょうど同じ年に研究室に移ってきたポスドクの方にひとつひとつ教えていただきながら系を立ち上げることになった.当時は,同期の修士課程の大学院生が構造を解いていくなか,目的のタンパク質を発現させることすらできずに1年近くも時間を浪費している自分が本当に嫌になったものである.
チャネルロドプシンの発現系の構築に成功し,精製もうまくいった.さぁ,これで結晶化だ,というところで再び問題が起こった.蒸気拡散法を用いて得られた結晶はX線を当てても当てても反射が出なかったのである.結晶化の条件の最適化や界面活性剤の交換をしてみてもまったくだめだった.15Åとか10Åとかいうレベルではない.No diff.である.そのため,もともと微生物型ロドプシンの結晶化法として考案されGタンパク質共役受容体の結晶化法として再評価されつつあった脂質キュービック法の導入を決意することになった.いまにしてみると,蒸気拡散法で得た結晶からまったく反射が出なかったのが,かえって脂質キュービック法を導入する決断を早めてくれたように思う.京都大学大学院医学研究科の岩田研究室に直接実験を教わりに行き,米国Scripps Research Instituteの研究グループにメールで疑問点をたずね,試行錯誤でこの結晶化法を立ち上げたが,はじめてチャネルロドプシンのオレンジ色の結晶を見たときは手が震えてプレートの焦点がうまく合わせられなかった.そして,当時,立ち上がったばかりの大型放射光施設SPring-8のBL32XUビームラインで測定を行った際,最初の結晶で一面に反射が見えたとき(3Åくらいは出ていた)は一瞬息が止まったのを覚えている.それ以来,筆者はBL32XUビームラインの虜である.
最後のハードルは位相決定の段階で待ち構えていた.無事,ネイティブ結晶のデータセットをとることはできたのだが,分子置換により位相を決定することができなかったのである.当然ながら,重原子を利用して位相を決めようということになったが,脂質キュービック法で得られた結晶について分子置換以外の方法で位相を決定した例はそれまでなかった.脂質キュービック法で得られた結晶はしばしば脂質に由来する反射が4.4Å~4.6Åの範囲に現われてタンパク質に由来する反射を埋もれさせてしまうことがあり,重原子による異常分散を利用した位相決定が本当に可能なのだろうかという疑問は筆者を悩ませた.そもそも,セレノメチオニンが効率よくチャネルロドプシンに導入できなかったという問題もあった.結局,この問題には半年以上も悩まされることになったわけだが,現状打破のきっかけは,いろいろな重原子化合物とチャネルロドプシンとを混ぜ合わせたとき,いくつかの水銀化合物を混ぜたときだけ試料の色がオレンジから赤に変わったことであった.試料の色が変わったということは水銀がレチナールの近くに結合しているせいではないだろうか.水銀ならいけるのではないか.最終的にこの判断が功を奏し,水銀を利用した多波長異常分散法により位相を決定することができたのだが,得られた構造をみるとレチナールのπ電子系と相互作用するCys残基に確かに水銀が結合しているのを確認することができた.また,いま思えば,BL32XUビームラインのマイクロビームを使うことでひとつの結晶から十分な冗長性をもつデータセットをとることができたことも重要な要因であった.
筆者の苦労話はせいぜいこの3つ,あとは,フランスやドイツ,米国や日本など,各地に競争相手がいると聞いていたため,しばしば胃がキリキリと痛んだことくらいである.しかし,蓋を開けてみれば,スタートしてから3年でチャネルロドプシンの構造を決定することができた.ひとえに研究室のメンバーやビームラインのスタッフの方々の厚意と協力があったからこそだと思い深く感謝している.
さて,実は,原著論文の初期の草稿にはゲート機構に関するつづきの記述があった.リバイスの過程でレフリーに“speculativeなので削除しなさい”といわれ泣く泣く削ったのだが,ちょうど原著論文がオンラインで出版される2週間前に,別のグループが同じ予測を打ち立ててJornal of Biological Chemistry誌に論文を掲載してしまった7).筆者としては少し悔しい想いであったが,予測されたゲート機構を実証するにはまださまざまな実験が必要となるので,今後はゲート機構の実証へと歩を進ませたいと考えている.また,明らかになった構造をもとに性質を改善させた変異型チャネルロドプシンも実際に作製したい.やるべきことはまだまだ山積みである.
文 献
- Nagel, G., Ollig, D., Fuhrmann, M. et al.: Channelrhodopsin-1: a light-gated proton channel in green algae. Science, 296, 2395-2398 (2002)[PubMed]
- Adamantidis, A. R., Zhang, F., Aravanis, A. M. et al.: Neural substrates of awakening probed with optogenetic control of hypocretin neurons. Nature, 450, 420-424 (2007)[PubMed]
- Zhang, F., Vierock, J., Yizhar, O. et al.: The microbial opsin family of optogenetic tools. Cell, 147, 1446-1457 (2011)[PubMed]
- Kawate, T. & Gouaux, E.: Fluorescence-detection size-exclusion chromatography for precrystallization screening of integral membrane proteins. Structure, 14, 673-681 (2006)[PubMed]
- Lanyi, J. K.: Proton transfers in the bacteriorhodopsin photocycle. Biochim. Biophys. Acta, 1757, 1012-1018 (2006)[PubMed]
- Muller, M., Bamann, C., Bamberg, E. et al.: Projection structure of channelrhodopsin-2 at 6Å resolution by electron crystallography. J. Mol. Biol., 414, 86-95 (2011)[PubMed]
- Eisenhauer, K., Uhne. J., Ritter. E. et al.: In channelrhodopsin-2 E90 is crucial for ion selectivity and is deprotonated during the photocycle. J. Biol. Chem., 287, 6904-6911 (2012)[PubMed]
著者プロフィール
略歴:東京大学理学系研究科博士課程 在学中.
研究テーマ:膜タンパク質の立体構造解析.
抱負:結晶構造解析を主眼におきつつも,幅広い手法を身につけながら複雑な分子機械である膜タンパク質を静的および動的にとらえ,その分子機構にせまっていきたい.
石谷 隆一郎(Ryuichiro Ishitani)
東京大学大学院理学系研究科 准教授.
濡木 理(Osamu Nureki)
東京大学大学院理学系研究科 教授.
研究室URL:http://www.nurekilab.net/
© 2012 加藤英明・石谷隆一郎・濡木 理 Licensed under CC 表示 2.1 日本