RNA結合タンパク質SAM68はシナプス形成タンパク質Neurexinの選択的スプライシングを神経活動に依存的に制御する
飯島 崇利
(スイスBasel大学,Biozentrum)
email:飯島崇利
DOI: 10.7875/first.author.2012.012
SAM68 regulates neuronal activity-dependent alternative splicing of Neurexin-1.
Takatoshi Iijima, Karen Wu, Harald Witte, Yoko Hanno-Iijima, Timo Glatter, Stéphane Richard, Peter Scheiffele
Cell, 147, 1601-1614 (2011)
ヒトの脳はその発達の過程において遺伝的なプログラムにもとづき複雑かつ精密なネットワークを構築する.この神経回路ネットワークの複雑さはシナプスの機能的および構造的な多様性により特徴づけられる.神経系における選択的スプライシングはシナプスタンパク質に豊富な多様性をあたえこのようなシナプスの特異性に大きく寄与しているものと考えられるが,それがどのようにプログラムされ維持されているのか,まだ多くが未解明である.今回,筆者らは,シナプス形成タンパク質Neurexinの選択的スプライシングについて解析を行い,これが時間的かつ空間的に制御されていること,SAM68とよばれるRNA結合タンパク質がNeurexinのmRNA前駆体に結合し,神経活動に依存的にその選択的スプライシングを変化させていることを明らかにした.以上のことから,SAM68が中枢神経系において神経活動に依存的な選択的スプライシングにかかわる重要なRNA結合タンパク質であることが示唆された.
ヒトの脳は1000億個ものニューロンからなっており,発達の過程において遺伝的なプログラムにもとづき複雑かつ精密なネットワークを構築する.また,成熟した脳においても学習や経験など後天的な要因により,いったん形成された神経回路ネットワークはダイナミックに変化する.神経回路ネットワークの形成の鍵はニューロンどうしのつなぎ目であるシナプスとよばれる構造にある.とくに,シナプス肥厚部には多種類のタンパク質が凝集し,複合体を形成してシナプスの形成および機能に重要な役割を担っている.成熟した脳には実に100兆個から500兆個ものシナプスが存在すると推定されている.これらは形態的および機能的にかなりの多様性をもっており,このシナプスの特異性が神経回路ネットワークの複雑さを特徴づけるものと考えられる.しかしながら,神経回路ネットワークの複雑さおよび精密さがどのように遺伝的にプログラムされ維持されているのか,まだその多くが未解明である.2000年前後に行われたゲノム解読プロジェクトの結果,われわれヒトを構成する遺伝子はわずか3万個にも満たないことがわかった.これは,哺乳類でのシナプスの多様性や神経回路ネットワークの複雑さを説明するうえであまりに少ないように思われる.
生物には,ひとつの遺伝子から少しずつ異なった複数の遺伝子産物(アイソフォーム)を生み出す選択的スプライシングとよばれる機構が存在する.これは,ごくかぎられた数の遺伝子から機能的に異なった複数の遺伝子産物を生み出すための非常にパワフルなしくみであるといえる.興味深いことに,シナプスタンパク質の大半はこの選択的スプライシングをうけており,これがどのように制御されどのようにシナプスの特異性に関与しているのかという点は複雑な神経回路ネットワークの構築を理解するうえで非常に重要であると考えられる.そこで今回,筆者らは,シナプスの形成においてとくに重要とされる細胞接着分子のひとつNeurexinに着目し,その選択的スプライシング機構について解析を行った.
神経系において選択的スプライシングがさかんなタンパク質としてはイオンチャネルや細胞接着分子などがある.とくに,一部の細胞接着分子の細胞外領域は多くの選択的スプライシング部位をもつことが知られており,細胞外における受容体との親和性にかかわっていることが明らかになりつつある.
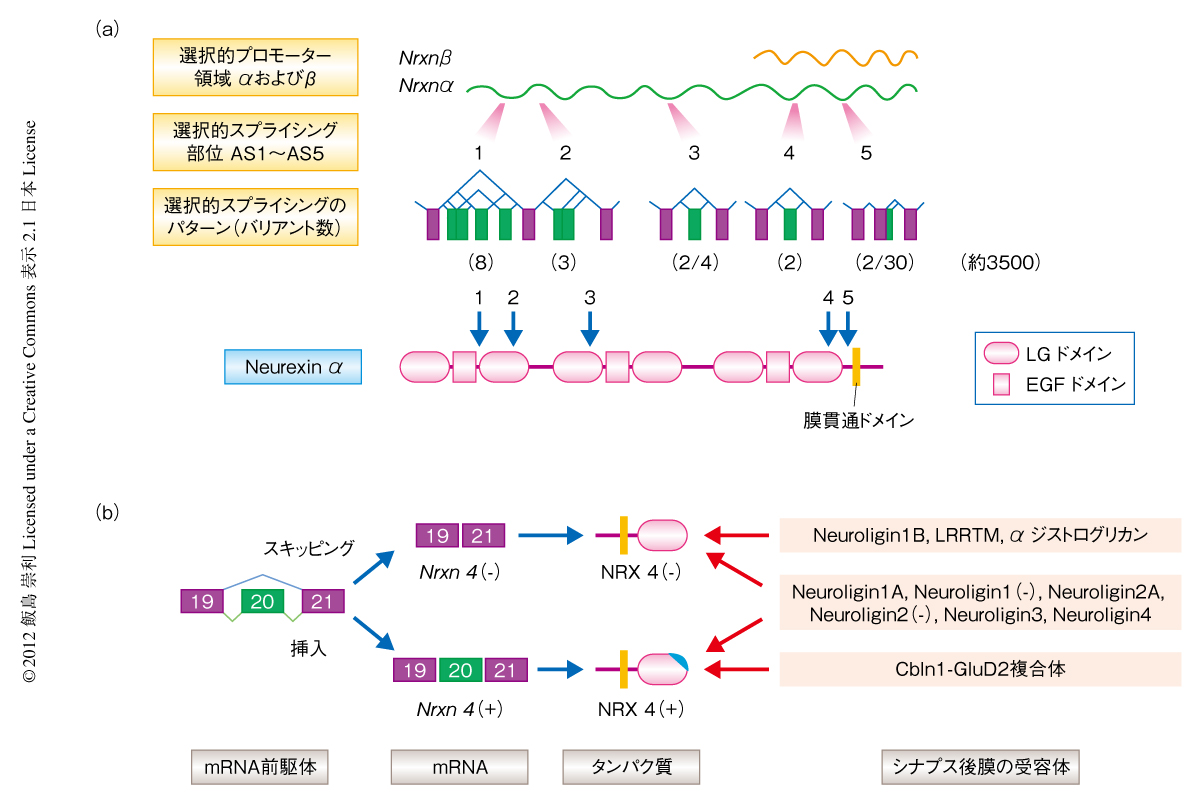
今回,筆者らは,Neurexinとよばれる細胞接着分子に注目した.Neurexinはシナプス前終末に局在し,シナプス後膜に存在する複数の種類の受容体との結合を介してシナプスの形成を誘導する1,2).Neurexinは3種類の遺伝子にコードされており,5箇所の選択的スプライシングにより多数のアイソフォームが生み出される3)(図1a).なかでも,スプライシング部位4における選択的スプライシング,すなわち,エクソン20の挿入の有無がシナプス後膜に存在する複数の受容体との結合に大きな影響をあたえることが知られている(図1b).たとえば,エクソン20がスキッピングにより欠損したNeurexinアイソフォームはNeuroligin1BやLRRTMに強く結合するが,エクソン20が挿入されたNeurexinアイソフォームではこの結合が著しく阻害される4-6).一方で,Cbln1-GluD2複合体はこのエクソン20をもつNeurexinに特異的に結合し小脳でのシナプスの形成に関与することが知られている7).
はじめに,脳においてNeurexinのスプライシング部位4における選択的スプライシングの比率についてRT-PCR法を用いて調べたところ,発達時期や領域により大きく差異のあることがわかった.このことから,Neurexinのスプライシング部位4における選択的スプライシングが複数の受容体との結合能を制御することが時期および領域に特異的なシナプスの形成に関与している可能性が示唆された.
つぎに,Neurexinの選択的スプライシングが神経活動により制御されているかどうかを検討した.成熟した小脳顆粒細胞ではエクソン20をもつNeurexinが豊富に生み出されているが,小脳顆粒細胞を分散培養し高K+処理により脱分極させたところ,エクソン20をもつアイソフォームからもたないアイソフォームへと発現がシフトすることがわかった.また,グルタミン酸受容体のアゴニストであるカイニン酸による処理,より生理的な条件での電気刺激などでも同様の現象が観察された.さらに,この選択的スプライシングの変化はL型電位依存性Ca2+チャネルを介したCa2+流入,および,Ca2+依存性カルモジュリンキナーゼIVの活性に依存的であることが明らかになった.
組換えNeuroliginなどシナプス後膜の形成タンパク質を発現させたHEK293細胞などの非神経系細胞株と海馬や大脳皮質に由来するニューロンとを共培養すると,非神経系細胞においてシナプス前終末が分化誘導されることが知られている8).そこで,Neuroligin1BあるいはGluD2をそれぞれ発現したHEK293細胞と小脳顆粒細胞との共培養を行いそのシナプス誘導能を調べたところ,エクソン20をもつNeurexinに特異的に結合するGluD2を発現させたHEK293細胞においてはシナプス前終末の分化が強く誘導されたのに対し,エクソン20をもたないNeurexinにより強い親和性を示すNeuroligin1Bを発現させたHEK293細胞ではシナプス前終末の分化は著しく低かった.しかしながら興味深いことに,高K+処理された小脳顆粒細胞ではNeuroligin1Bによるシナプスの分化誘導が促進され,一方で,GluD2に依存したシナプスの誘導は逆に低下した.以上のことから,神経活動に依存したNeurexinの選択的スプライシングの変化が受容体との相互作用を介したシナプスの形成に強く影響を及ぼすことが示唆された.
Neurexinの選択的スプライシングの制御にかかわるタンパク質として,in vitroでのスプライシングレポーターアッセイによりRNA結合タンパク質であるSAM68を同定した.SAM68はKH型のRNA結合ドメインをもつスプライシングタンパク質として知られ,2種類の類似したタンパク質SLM1およびSLM2とともにSTAR(signal transduction and activation of RNA)ファミリーを構成する.さらなる解析により,SAM68はNeurexinのmRNA前駆体のイントロン20にあるAUリッチ領域に結合し,エクソン20の成熟mRNAへの挿入を抑制していることがわかった.SAM68は神経系では広範に発現しており,in vivoの解析において,SAM68ノックアウトマウスでは小脳をはじめとした複数の脳領域でエクソン20をもたないNeurexinの割合が著しく減少していることが明らかになった.このことから,実際にSAM68が神経系においてNeurexinの選択的スプライシングに関与していることが確かめられた.
さらに,神経活動に依存的な選択的スプライシングの変化をSAM68ノックアウトマウスの小脳において調べたところ,脱分極あるいはカイニン酸により誘導されるNeurexinの選択的スプライシングの変化は起こらなかった.また,神経活動によりSAM68の細胞内における局在および発現量は大きく変化しないこと,SAM68のN末端の部位が神経活動に依存的に(おそらくは,Ca2+依存性カルモジュリンキナーゼIVにより)リン酸化されることから,SAM68が神経活動により活性化され選択的スプライシングの変化を誘導していることが示唆された.以上のことから,少なくとも小脳顆粒細胞において,SAM68が神経活動に依存的にNeurexinの選択的スプライシングを変化させ,シナプス後膜における受容体との親和性にダイナミックな変化をあたえることにより,平行線維とプルキンエ細胞とのあいだのシナプスの機能を制御している可能性が示唆された(図2).
この研究により,大まかに以下の2つのことが明らかにされた.ひとつは,Neurexinの受容体との結合を決める部位をコードするスプライシング部位4における選択的スプライシングが神経活動に依存的に制御されていること,もうひとつは,RNA結合タンパク質SAM68が神経活動により活性化されNeurexinの選択的スプライシングの変化を誘導すること,である.これまで,神経活動により制御されるmRNA前駆体は多く知られてきた10).また,神経系に発現するNovaやPTBなどRNA結合タンパク質による組織に特異的な選択的スプライシングの制御も報告されてきたが,選択的スプライシングを神経活動に依存的に直接に制御するスプライシングタンパク質はまったく知られておらず,この研究が最初の発見となった.
このことから,SAM68がほかにどのようなmRNA前駆体の選択的スプライシングを神経活動に依存して制御しているのかという点が非常に興味深い.当然ながら,シナプスタンパク質だけでなく,ほかにもさまざまなmRNA前駆体がこの制御をうけているものと予想される.また,SAM68にはファミリータンパク質としてSLM1とSLM2があり,これらもNeurexinのin vitroでのスプライシングレポーターアッセイにおいてSAM68と同様に強い活性をみせた.興味深いことに,SLM1とSLM2は神経系にとくに強く発現しており,成熟した脳ではそれぞれ特徴的な発現パターンを示した(筆者ら,未発表データ).今後,SLM1とSLM2を含めたSTARファミリーの解析により,神経系における選択的スプライシングの普遍的な分子機構をはじめ,複雑かつ精密な神経回路ネットワークの構築の謎が少しずつ解明されるかもしれない.また,興味深いことに,神経精神疾患の患者において多くのスプライシング異常がみられることから,自閉症や統合失調症をはじめとした疾患の理解につながることも期待される.
略歴:2004年 大阪大学大学院医学系研究科博士課程 修了,慶應義塾大学医学部 特任助教を経て,2009年よりスイスBasel大学 博士研究員.
研究テーマ:神経活動に依存的なシナプスタンパク質の発現制御機構.
抱負:人生をエンジョイしつつ,コツコツと自分らしい仕事をやっていきたい.
© 2012 飯島 崇利 Licensed under CC 表示 2.1 日本
(スイスBasel大学,Biozentrum)
email:飯島崇利
DOI: 10.7875/first.author.2012.012
SAM68 regulates neuronal activity-dependent alternative splicing of Neurexin-1.
Takatoshi Iijima, Karen Wu, Harald Witte, Yoko Hanno-Iijima, Timo Glatter, Stéphane Richard, Peter Scheiffele
Cell, 147, 1601-1614 (2011)
要 約
ヒトの脳はその発達の過程において遺伝的なプログラムにもとづき複雑かつ精密なネットワークを構築する.この神経回路ネットワークの複雑さはシナプスの機能的および構造的な多様性により特徴づけられる.神経系における選択的スプライシングはシナプスタンパク質に豊富な多様性をあたえこのようなシナプスの特異性に大きく寄与しているものと考えられるが,それがどのようにプログラムされ維持されているのか,まだ多くが未解明である.今回,筆者らは,シナプス形成タンパク質Neurexinの選択的スプライシングについて解析を行い,これが時間的かつ空間的に制御されていること,SAM68とよばれるRNA結合タンパク質がNeurexinのmRNA前駆体に結合し,神経活動に依存的にその選択的スプライシングを変化させていることを明らかにした.以上のことから,SAM68が中枢神経系において神経活動に依存的な選択的スプライシングにかかわる重要なRNA結合タンパク質であることが示唆された.
はじめに
ヒトの脳は1000億個ものニューロンからなっており,発達の過程において遺伝的なプログラムにもとづき複雑かつ精密なネットワークを構築する.また,成熟した脳においても学習や経験など後天的な要因により,いったん形成された神経回路ネットワークはダイナミックに変化する.神経回路ネットワークの形成の鍵はニューロンどうしのつなぎ目であるシナプスとよばれる構造にある.とくに,シナプス肥厚部には多種類のタンパク質が凝集し,複合体を形成してシナプスの形成および機能に重要な役割を担っている.成熟した脳には実に100兆個から500兆個ものシナプスが存在すると推定されている.これらは形態的および機能的にかなりの多様性をもっており,このシナプスの特異性が神経回路ネットワークの複雑さを特徴づけるものと考えられる.しかしながら,神経回路ネットワークの複雑さおよび精密さがどのように遺伝的にプログラムされ維持されているのか,まだその多くが未解明である.2000年前後に行われたゲノム解読プロジェクトの結果,われわれヒトを構成する遺伝子はわずか3万個にも満たないことがわかった.これは,哺乳類でのシナプスの多様性や神経回路ネットワークの複雑さを説明するうえであまりに少ないように思われる.
生物には,ひとつの遺伝子から少しずつ異なった複数の遺伝子産物(アイソフォーム)を生み出す選択的スプライシングとよばれる機構が存在する.これは,ごくかぎられた数の遺伝子から機能的に異なった複数の遺伝子産物を生み出すための非常にパワフルなしくみであるといえる.興味深いことに,シナプスタンパク質の大半はこの選択的スプライシングをうけており,これがどのように制御されどのようにシナプスの特異性に関与しているのかという点は複雑な神経回路ネットワークの構築を理解するうえで非常に重要であると考えられる.そこで今回,筆者らは,シナプスの形成においてとくに重要とされる細胞接着分子のひとつNeurexinに着目し,その選択的スプライシング機構について解析を行った.
1.シナプス形成タンパク質Neurexinの選択的スプライシングは複数の受容体との相互作用に重要である
神経系において選択的スプライシングがさかんなタンパク質としてはイオンチャネルや細胞接着分子などがある.とくに,一部の細胞接着分子の細胞外領域は多くの選択的スプライシング部位をもつことが知られており,細胞外における受容体との親和性にかかわっていることが明らかになりつつある.
今回,筆者らは,Neurexinとよばれる細胞接着分子に注目した.Neurexinはシナプス前終末に局在し,シナプス後膜に存在する複数の種類の受容体との結合を介してシナプスの形成を誘導する1,2).Neurexinは3種類の遺伝子にコードされており,5箇所の選択的スプライシングにより多数のアイソフォームが生み出される3)(図1a).なかでも,スプライシング部位4における選択的スプライシング,すなわち,エクソン20の挿入の有無がシナプス後膜に存在する複数の受容体との結合に大きな影響をあたえることが知られている(図1b).たとえば,エクソン20がスキッピングにより欠損したNeurexinアイソフォームはNeuroligin1BやLRRTMに強く結合するが,エクソン20が挿入されたNeurexinアイソフォームではこの結合が著しく阻害される4-6).一方で,Cbln1-GluD2複合体はこのエクソン20をもつNeurexinに特異的に結合し小脳でのシナプスの形成に関与することが知られている7).
はじめに,脳においてNeurexinのスプライシング部位4における選択的スプライシングの比率についてRT-PCR法を用いて調べたところ,発達時期や領域により大きく差異のあることがわかった.このことから,Neurexinのスプライシング部位4における選択的スプライシングが複数の受容体との結合能を制御することが時期および領域に特異的なシナプスの形成に関与している可能性が示唆された.
2.Neurexinの選択的スプライシングは神経活動により制御されている
つぎに,Neurexinの選択的スプライシングが神経活動により制御されているかどうかを検討した.成熟した小脳顆粒細胞ではエクソン20をもつNeurexinが豊富に生み出されているが,小脳顆粒細胞を分散培養し高K+処理により脱分極させたところ,エクソン20をもつアイソフォームからもたないアイソフォームへと発現がシフトすることがわかった.また,グルタミン酸受容体のアゴニストであるカイニン酸による処理,より生理的な条件での電気刺激などでも同様の現象が観察された.さらに,この選択的スプライシングの変化はL型電位依存性Ca2+チャネルを介したCa2+流入,および,Ca2+依存性カルモジュリンキナーゼIVの活性に依存的であることが明らかになった.
組換えNeuroliginなどシナプス後膜の形成タンパク質を発現させたHEK293細胞などの非神経系細胞株と海馬や大脳皮質に由来するニューロンとを共培養すると,非神経系細胞においてシナプス前終末が分化誘導されることが知られている8).そこで,Neuroligin1BあるいはGluD2をそれぞれ発現したHEK293細胞と小脳顆粒細胞との共培養を行いそのシナプス誘導能を調べたところ,エクソン20をもつNeurexinに特異的に結合するGluD2を発現させたHEK293細胞においてはシナプス前終末の分化が強く誘導されたのに対し,エクソン20をもたないNeurexinにより強い親和性を示すNeuroligin1Bを発現させたHEK293細胞ではシナプス前終末の分化は著しく低かった.しかしながら興味深いことに,高K+処理された小脳顆粒細胞ではNeuroligin1Bによるシナプスの分化誘導が促進され,一方で,GluD2に依存したシナプスの誘導は逆に低下した.以上のことから,神経活動に依存したNeurexinの選択的スプライシングの変化が受容体との相互作用を介したシナプスの形成に強く影響を及ぼすことが示唆された.
3.RNA結合タンパク質SAM68がNeurexinの神経活動に依存的な選択的スプライシングを制御する
Neurexinの選択的スプライシングの制御にかかわるタンパク質として,in vitroでのスプライシングレポーターアッセイによりRNA結合タンパク質であるSAM68を同定した.SAM68はKH型のRNA結合ドメインをもつスプライシングタンパク質として知られ,2種類の類似したタンパク質SLM1およびSLM2とともにSTAR(signal transduction and activation of RNA)ファミリーを構成する.さらなる解析により,SAM68はNeurexinのmRNA前駆体のイントロン20にあるAUリッチ領域に結合し,エクソン20の成熟mRNAへの挿入を抑制していることがわかった.SAM68は神経系では広範に発現しており,in vivoの解析において,SAM68ノックアウトマウスでは小脳をはじめとした複数の脳領域でエクソン20をもたないNeurexinの割合が著しく減少していることが明らかになった.このことから,実際にSAM68が神経系においてNeurexinの選択的スプライシングに関与していることが確かめられた.
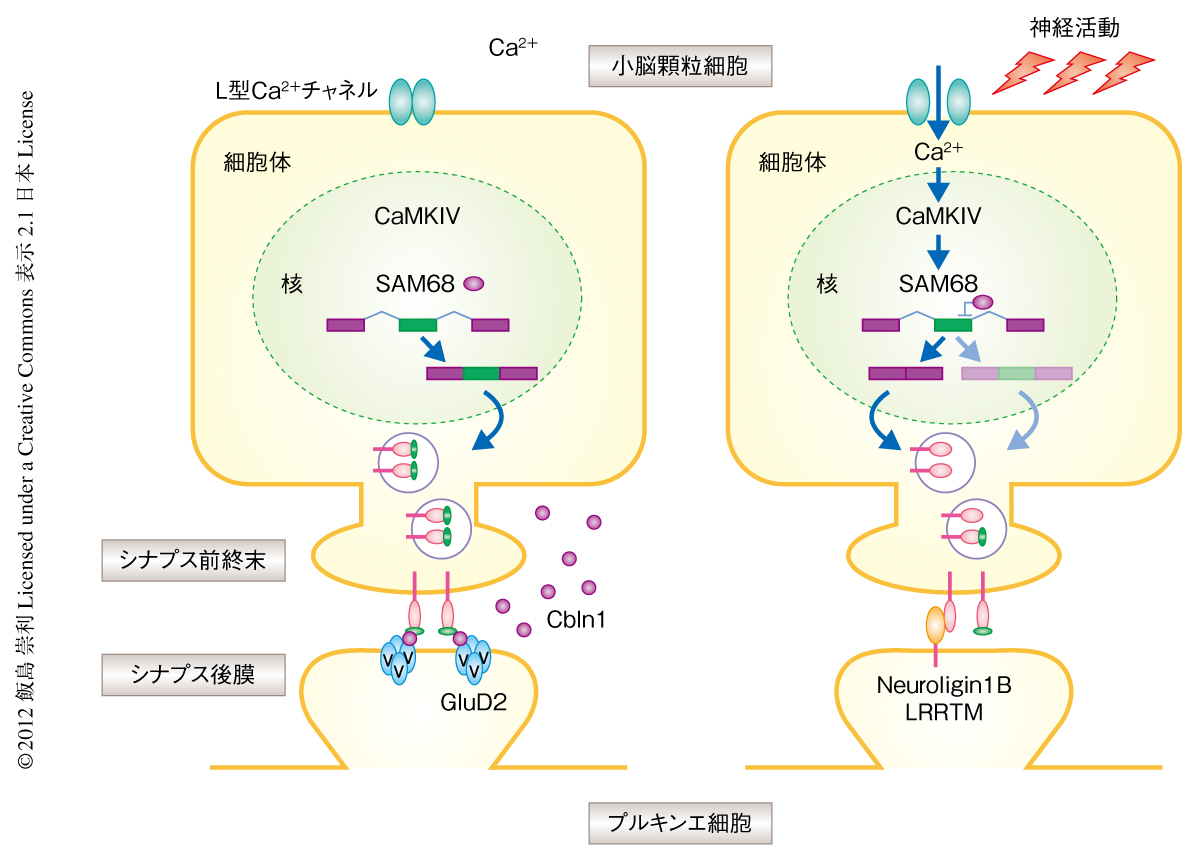
さらに,神経活動に依存的な選択的スプライシングの変化をSAM68ノックアウトマウスの小脳において調べたところ,脱分極あるいはカイニン酸により誘導されるNeurexinの選択的スプライシングの変化は起こらなかった.また,神経活動によりSAM68の細胞内における局在および発現量は大きく変化しないこと,SAM68のN末端の部位が神経活動に依存的に(おそらくは,Ca2+依存性カルモジュリンキナーゼIVにより)リン酸化されることから,SAM68が神経活動により活性化され選択的スプライシングの変化を誘導していることが示唆された.以上のことから,少なくとも小脳顆粒細胞において,SAM68が神経活動に依存的にNeurexinの選択的スプライシングを変化させ,シナプス後膜における受容体との親和性にダイナミックな変化をあたえることにより,平行線維とプルキンエ細胞とのあいだのシナプスの機能を制御している可能性が示唆された(図2).
おわりに
この研究により,大まかに以下の2つのことが明らかにされた.ひとつは,Neurexinの受容体との結合を決める部位をコードするスプライシング部位4における選択的スプライシングが神経活動に依存的に制御されていること,もうひとつは,RNA結合タンパク質SAM68が神経活動により活性化されNeurexinの選択的スプライシングの変化を誘導すること,である.これまで,神経活動により制御されるmRNA前駆体は多く知られてきた10).また,神経系に発現するNovaやPTBなどRNA結合タンパク質による組織に特異的な選択的スプライシングの制御も報告されてきたが,選択的スプライシングを神経活動に依存的に直接に制御するスプライシングタンパク質はまったく知られておらず,この研究が最初の発見となった.
このことから,SAM68がほかにどのようなmRNA前駆体の選択的スプライシングを神経活動に依存して制御しているのかという点が非常に興味深い.当然ながら,シナプスタンパク質だけでなく,ほかにもさまざまなmRNA前駆体がこの制御をうけているものと予想される.また,SAM68にはファミリータンパク質としてSLM1とSLM2があり,これらもNeurexinのin vitroでのスプライシングレポーターアッセイにおいてSAM68と同様に強い活性をみせた.興味深いことに,SLM1とSLM2は神経系にとくに強く発現しており,成熟した脳ではそれぞれ特徴的な発現パターンを示した(筆者ら,未発表データ).今後,SLM1とSLM2を含めたSTARファミリーの解析により,神経系における選択的スプライシングの普遍的な分子機構をはじめ,複雑かつ精密な神経回路ネットワークの構築の謎が少しずつ解明されるかもしれない.また,興味深いことに,神経精神疾患の患者において多くのスプライシング異常がみられることから,自閉症や統合失調症をはじめとした疾患の理解につながることも期待される.
文 献
- Baudouin, S. & Scheiffele, P.: SnapShot: Neuroligin-neurexin complexes. Cell, 141, 908 (2010)[PubMed]
- Dean, C., Scholl, F. G., Choih, J. et al.: Neurexin mediates the assembly of presynaptic terminals. Nat. Neurosci., 6, 708-716 (2003)[PubMed]
- Ushkaryov, Y. A., Petrenko, A. G., Geppert, M. et al.: Neurexins: synaptic cell surface proteins related to the α-latrotoxin receptor and laminin. Science, 257, 50-56 (1992)[PubMed]
- Boucard, A. A., Chubykin, A. A., Comoletti, D. et al.: A splice code for trans-synaptic cell adhesion mediated by binding of neuroligin 1 to α- and β-neurexins. Neuron, 48, 229-236 (2005)[PubMed]
- Chih, B., Gollan, L. & Scheiffele, P.: Alternative splicing controls selective trans-synaptic interactions of the neuroligin-neurexin complex. Neuron, 51, 171-178 (2006)[PubMed]
- Siddiqui, T. J., Pancaroglu, R., Kang, Y. et al.: LRRTMs and neuroligins bind neurexins with a differential code to cooperate in glutamate synapse development. J. Neurosci., 30, 7495-7506 (2010)[PubMed]
- Uemura, T., Lee, S. J., Yasumura, M. et al.: Trans-synaptic interaction of GluRδ2 and Neurexin through Cbln1 mediates synapse formation in the cerebellum. Cell, 141, 1068-1079 (2010)[PubMed]
- Scheiffele, P., Fan, J., Choih, J. et al.: Neuroligin expressed in nonneuronal cells triggers presynaptic development in contacting axons. Cell, 101, 657-669 (2000)[PubMed]
- Iijima, T., Emi, K. & Yuzaki, M.: Activity-dependent repression of Cbln1 expression: mechanism for developmental and homeostatic regulation of synapses in the cerebellum. J. Neurosci., 29, 5425-5434 (2009)[PubMed]
- Li, Q., Lee, J. A. & Black, D. L.: Neuronal regulation of alternative pre-mRNA splicing. Nat. Rev. Neurosci., 8, 819-831 (2007)[PubMed]
著者プロフィール
略歴:2004年 大阪大学大学院医学系研究科博士課程 修了,慶應義塾大学医学部 特任助教を経て,2009年よりスイスBasel大学 博士研究員.
研究テーマ:神経活動に依存的なシナプスタンパク質の発現制御機構.
抱負:人生をエンジョイしつつ,コツコツと自分らしい仕事をやっていきたい.
© 2012 飯島 崇利 Licensed under CC 表示 2.1 日本