植物の色素体に局在するNa+依存性のピルビン酸輸送体の同定
古本 強
(広島大学大学院理学研究科 生物科学専攻植物生理化学研究室)
email:古本 強
DOI: 10.7875/first.author.2011.147
A plastidial sodium-dependent pyruvate transporter.
Tsuyoshi Furumoto, Teppei Yamaguchi, Yumiko Ohshima-Ichie, Masayoshi Nakamura, Yoshiko Tsuchida-Iwata, Masaki Shimamura, Junichi Ohnishi, Shingo Hata, Udo Gowik, Peter Westhoff, Andrea Bräutigam, Andreas P. M. Weber, Katsura Izui
Nature, 476, 472-475 (2011)
植物においてピルビン酸は,脂肪酸合成,テルペノイド合成,分枝アミノ酸合成など,色素体に局在する多くの生合成経路の代謝前駆体として機能している.こうしたピルビン酸の重要性にもかかわらず,細胞質から色素体へのピルビン酸の取り込みの分子機構は十分に理解されていない.今回,筆者らは,フラベリア属におけるC3植物とC4植物とのあいだでのディファレンシャルな遺伝子発現の解析から,C4植物に豊富に発現する新規の遺伝子BASS2を発見した.その産物であるBASS2は葉肉細胞にある葉緑体の包膜に局在し,Na+依存性のピルビン酸輸送体をもつC4植物に広く豊富に存在した.大腸菌において組換えBASS2はNa+依存性のピルビン酸の取り込み活性を示した.BASS2による葉緑体へのNa+の取り込みはNa+/H+アンチポーターであるNHD1により相殺され,これはBASS2とNHD1の両方を発現させた大腸菌において再構成された.この結果は,色素体の包膜におけるNa+依存性のピルビン酸輸送体の分子的な実体とその輸送機構を示すものであった.
細胞質に取り込まれたグルコースは解糖系によりピルビン酸にまで分解され,ひきつづきミトコンドリアや色素体に輸送されて種々のエネルギー代謝や生合成に用いられる.このようにオルガネラへのピルビン酸の輸送は生命活動の根幹を担う反応でありながら,この輸送をささえる分子的な実体はこれまで明らかにされていなかった.
バイオテクノロジーによる植物の生産能力の増強は,大気のCO2濃度を低減させる有力な手段のひとつと目されている.また,バイオエタノールやバイオディーゼルといった植物の生産物の産業利用(バイオマスエネルギーの利用)もさかんになってきている.バイオテクノロジーを利用して生産力をより強化した植物を作出する試みにおいて,これらの光合成や脂質合成に必要な色素体へのピルビン酸輸送の分子機構が解明されていないことは大きな障壁であった.
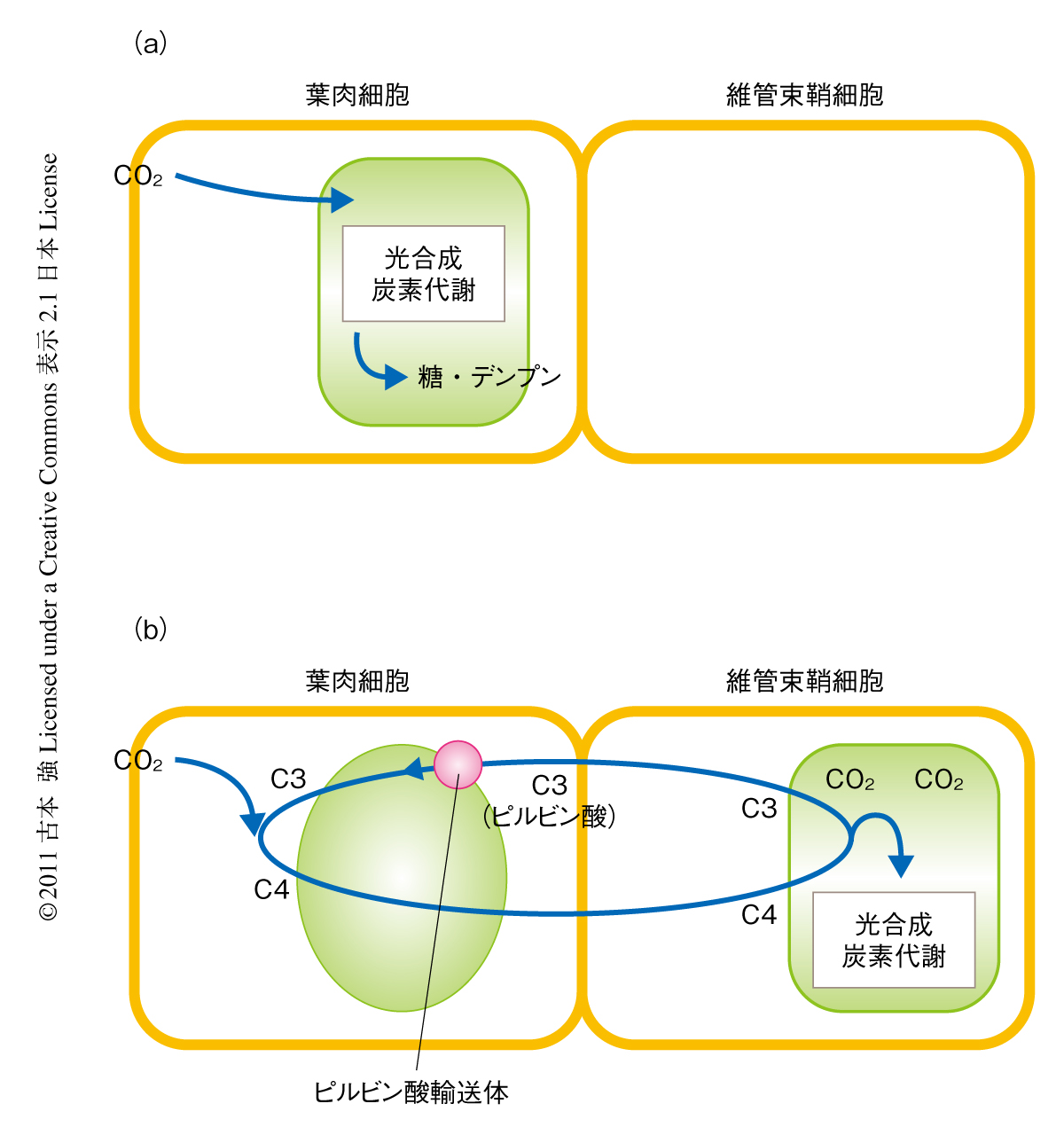
C4植物とよばれる一群の植物は,主要穀物であるイネやコムギなどのC3植物に比べ,一般に高い光合成能を示す.大気にあるCO2を濃縮する炭素代謝回路(C4回路)を進化的に獲得していることがその理由で,トウモロコシやサトウキビなどの作物のほか,多くの雑草がC4回路を発達させている.C4回路には葉肉細胞にある葉緑体にピルビン酸(C3)を取り込む活性が認められ,これが色素体におけるピルビン酸輸送の研究例であった(図1).これまでの生化学的な解析によると,C4植物はNa+依存性のピルビン酸輸送を示す植物とH+依存性のピルビン酸輸送を示す植物に大別され1),また,こうしたNa+濃度勾配あるいはH+濃度勾配への依存性は暗所に順応させた葉緑体でのみ認められることが明らかにされている2).ピルビン酸輸送体が同定できれば,こうした生化学的な特徴をささえる分子基盤についても情報が得られるものと期待された.
筆者らは,この葉緑体へのピルビン酸輸送をつかさどるタンパク質の同定をめざし,フラベリア属においてC3植物である種(Flaveria pringlei)とC4植物である種(F. trinervia)を用いて遺伝子発現の解析を行った.C4植物である種にはC3植物である種と比べ,既知のC4植物と同様に,葉緑体におけるピルビン酸輸送体をコードする遺伝子が高発現していることが期待できる.ディファレンシャルスクリーニング法とRNAシークエンス法という異なる2つの方法により,BASS2遺伝子,BASS4遺伝子,NHD1遺伝子と名づけた,葉緑体への局在を推定させる新規の膜タンパク質をコードする3つの遺伝子を見い出すことに成功した.
筆者らのスクリーニングの成功を知り,イギリスとドイツの研究グループがほぼ同様のスクリーニングを異なる植物で行い報告している3).フラベリア属以外にも,フウチョウソウ属などいくつかの植物にはC3植物である種とC4植物である種が認められる.フウチョウソウ属はシロイヌナズナを含むアブラナ科と近縁な関係にあり,シロイヌナズナにおいて開発されている分子ツールを部分的に利用することが可能である.筆者らの実施したフラベリア属,そして,すでに報告されているフウチョウソウ属におけるディファレンシャルな遺伝子発現の解析において,共通して発現の上昇していた遺伝子はBASS2遺伝子とNHD1遺伝子であった.この結果から,この2つの遺伝子の産物によりピルビン酸の輸送がささえられている可能性が考えられた.BASS2遺伝子は“bile acid sodium symporter family protein 2”,NHD1遺伝子は“sodium hydrogen exchanger 1”としてあたえられた名称である.植物では胆汁酸(bile acid)の存在は疑問視されており,BASS2はおそらく異なる物質を輸送しているであろうと考えられた.一方,NHD1については近縁のタンパク質がNa+とH+の交換輸送能を示したことから4),BASS2がピルビン酸を輸送する本体ではないかと仮説をたてた.
BASS2は7回膜貫通型あるいは9回膜貫通型の膜タンパク質であり,C末端に電荷に富む可溶性の領域をもっていた.この部位に相当するペプチドを合成し,これに対する抗体を作製した.この抗体と交差するタンパク質は,C3植物である種には検出限界以下しか存在しなかったにもかかわらず,C4植物である2種(F. bidentis,F. trinervia)においてともに高発現していた.また,単離した葉肉細胞にある葉緑体の包膜に強く交差を示すタンパク質の存在が認められた.この知見は,葉の横断切片に対する免疫組織染色の結果でも追認され,色素体の表面に交差タンパク質の存在が示された.GFPを付加したBASS2により形質転換したタバコにおいては,根の色素体にその局在性を示した.ついで,C4植物における普遍性を調べたところ,かつてNa+依存性のピルビン酸輸送を示すとされた植物に交差タンパク質が広く認められ,その一方で,H+依存性のピルビン酸輸送を示した植物(トウモロコシおよびソルガム)には交差タンパク質は認められなかった.これらの結果は,BASS2が既知の知見と合致したNa+依存性のピルビン酸輸送体の候補としてふさわしいことを示すとともに,H+依存性のピルビン酸輸送体とは区別されることを示唆した.
大腸菌において発現させたBASS2は細胞膜に存在した.このBASS2を発現させた大腸菌と発現していない大腸菌とのあいだでピルビン酸の輸送活性に違いがあるかどうかを検討した.その結果,短い時間においてBASS2に依存するピルビン酸の取り込みを認め,さらに,Na+の濃度に依存して取り込み速度が変化するという結果を得た.これらの結果は,BASS2がNa+依存性のピルビン酸輸送活性をもつ分子実体であることを示していた.
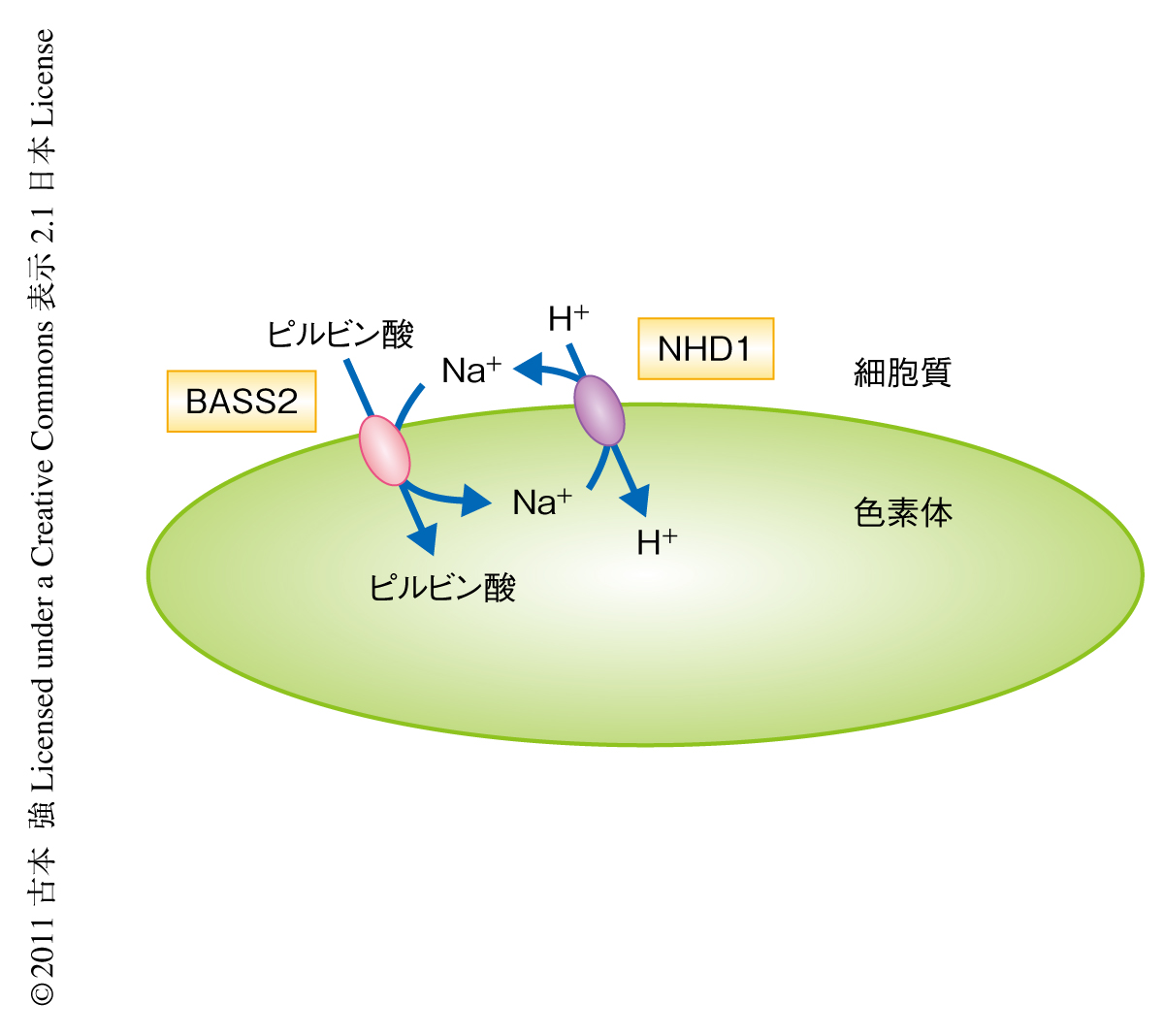
BASS2遺伝子と同じ過程でクローニングされたNHD1遺伝子は,さきにも述べたとおり,Na+/H+アンチポーターをコードするものと推定された.この推定された機能とBASS2のNa+依存的なピルビン酸輸送活性とを考えあわせ,ひとつの興味深い仮説を導いた.それは,“BASS2によるピルビン酸の輸送にともない色素体に取り込まれたNa+が,NHD1のはたらきにより排出されより毒性の低いH+に置き換わる”というものである.この仮説では,Na+は共役反応剤として用いられるだけで色素体に蓄積することはない.このBASS2とNHD1との共役によるピルビン酸の輸送機構は,大腸菌においてこの2つを同時に発現させることで検討することができる.その結果,細胞の内外のH+の濃度勾配に依存してNa+の濃度に非依存的にピルビン酸が取り込まれることが確認できた.この結果は,BASS2とNHD1との共役反応が大腸菌において再構成できたことを意味した.
BASS2遺伝子に相同な遺伝子はこれまでにゲノム解析されたすべての植物のゲノムに存在する.C3植物におけるその生理機能を明らかにするため,シロイヌナズナにおいて遺伝子の発現解析を行った.その結果,成熟した本葉での発現は低いが,子葉,若い本葉,発達中の種子においてある程度まで発現していることを確認した.貯蔵脂質の分解をエネルギーの初発とする子葉では炭素骨格は細胞質にリンゴ酸として供給されるが,リンゴ酸からピルビン酸へは容易に代謝変換されうる.こうした背景から,子葉などの未発達な色素体ではBASS2を介したピルビン酸の取り込みがあり,これが色素体での代謝をささえている可能性が考えられた.そこでとくに,BASS2が色素体におけるピルビン酸を初発とするイソプレノイド代謝に寄与しているかどうかを,特異的な阻害剤と遺伝子破壊植物を用いて検討した.
シロイヌナズナの野生株には播種後1週間目からの抽出液に抗BASS2抗体と交差するタンパク質が存在したが,bass2破壊株には認められなかった.これらの植物から無傷の葉緑体を単離しピルビン酸輸送活性を測定したところ,野生株の葉緑体にはNa+依存性のピルビン酸輸送活性を認めたが,bass2遺伝子破壊株には認められなかった.これらの結果は,C3植物であるシロイヌナズナにおいても生育時期を限定すればBASS2に依存したピルビン輸送活性を観察できることとともに,bass2破壊株ではピルビン酸輸送活性が失われていることを示していた.細胞質におけるイソプレノイド合成経路(メバロン酸経路)と対比して,色素体におけるイソプレノイド合成経路は非メバロン酸経路とよばれている.このように,細胞には2つの独立した代謝経路があり,イソペンテニル二リン酸が細胞質と色素体とを行き来している5).メバロン酸経路の律速酵素の阻害剤を投与しても野生型の植物は大きな形態異常を示さないが,これは色素体におけるイソプレノイド合成により相補されるからであると説明されている.もし,非メバロン酸経路の初発反応におけるピルビン酸の供給にBASS2が寄与しているなら,bass2破壊株はそれが不全となっているため阻害剤に対する相補性が示されなくなっているはずで,阻害剤に対し強い感受性をもつものと期待された.この期待のとおり,bass2変異体は阻害剤への高い感受性を示し,とくに子葉の緑化が遅れるという表現型を示した.
オルガネラにおけるピルビン酸の輸送について,今回,はじめてピルビン酸輸送体の同定に成功し,その分子機構についてもNHD1との共役によるという知見を得た(図2).単離したC4植物の葉肉細胞の葉緑体に対し光を照射するとピルビン酸の取り込みにおいてNa+依存性の消失することが報告されているが,この現象はここで得られた知見によりつぎのように説明できる.つまり,光照射により駆動された電子伝達によりチラコイドにおいてH+の組み込みが起こりストロマ側がアルカリ化する.この現象により生じたH+の濃度勾配がNHD1を駆動しBASS2が機能するために細胞質とストロマとのあいだに十分な大きさのNa+濃度勾配が生じ,外液へのNa+の添加のない状態でもピルビン酸の取り込みが可能になるものと考えられる.こうした推察は生化学的な知見をもとにすでになされているが6),今回,ピルビン酸輸送体が同定されたことによりこれを分子レベルで検討することができるようになった.
今後は,脂質合成への寄与を調べる実験をとおしその関与を検討するほか,こうした基礎知見を利用して脂質の含有量を高めた種子をもつ植物を分子育種により開発するという可能性もみえてきた.また,C3植物であるイネにC4植物の光合成能を付与させようという国際プロジェクトが進行中であるが,葉緑体膜を介したピルビン酸の輸送機構がこれまでわからなかったため,こうした研究プロジェクトは停滞を余儀なくされていた.ピルビン酸輸送体の同定によりこれが加速することが期待される.BASS2はトウモロコシなどのH+依存性のピルビン酸輸送体とは区別されたことから,今後,H+依存性のピルビン酸輸送体を同定する試みも必要となろう.また,広範な雑草種でBASS2が検出された一方,トウモロコシにおいて検出されなかったことは,このBASS2の特異的な阻害剤の開発が雑草種に選択的な特性を示す新規の農薬の開発に直結する可能性を示唆している.
略歴:1999年 京都大学大学院生命科学研究科 修了,同年 東京大学大学院理学系研究科 助手,2000年 京都大学大学院生命科学研究科 助手を経て,2005年より広島大学大学院理学研究科 准教授.
研究テーマ:植物の環境応答の分子機構.
関心事:植物の環境応答能力の高さ(温度やCO2濃度など)に不思議だと感じます.だれも知らない未知の植物の能力に気がつくことができれば,と願っています.
© 2011 古本 強 Licensed under CC 表示 2.1 日本
(広島大学大学院理学研究科 生物科学専攻植物生理化学研究室)
email:古本 強
DOI: 10.7875/first.author.2011.147
A plastidial sodium-dependent pyruvate transporter.
Tsuyoshi Furumoto, Teppei Yamaguchi, Yumiko Ohshima-Ichie, Masayoshi Nakamura, Yoshiko Tsuchida-Iwata, Masaki Shimamura, Junichi Ohnishi, Shingo Hata, Udo Gowik, Peter Westhoff, Andrea Bräutigam, Andreas P. M. Weber, Katsura Izui
Nature, 476, 472-475 (2011)
要 約
植物においてピルビン酸は,脂肪酸合成,テルペノイド合成,分枝アミノ酸合成など,色素体に局在する多くの生合成経路の代謝前駆体として機能している.こうしたピルビン酸の重要性にもかかわらず,細胞質から色素体へのピルビン酸の取り込みの分子機構は十分に理解されていない.今回,筆者らは,フラベリア属におけるC3植物とC4植物とのあいだでのディファレンシャルな遺伝子発現の解析から,C4植物に豊富に発現する新規の遺伝子BASS2を発見した.その産物であるBASS2は葉肉細胞にある葉緑体の包膜に局在し,Na+依存性のピルビン酸輸送体をもつC4植物に広く豊富に存在した.大腸菌において組換えBASS2はNa+依存性のピルビン酸の取り込み活性を示した.BASS2による葉緑体へのNa+の取り込みはNa+/H+アンチポーターであるNHD1により相殺され,これはBASS2とNHD1の両方を発現させた大腸菌において再構成された.この結果は,色素体の包膜におけるNa+依存性のピルビン酸輸送体の分子的な実体とその輸送機構を示すものであった.
はじめに
細胞質に取り込まれたグルコースは解糖系によりピルビン酸にまで分解され,ひきつづきミトコンドリアや色素体に輸送されて種々のエネルギー代謝や生合成に用いられる.このようにオルガネラへのピルビン酸の輸送は生命活動の根幹を担う反応でありながら,この輸送をささえる分子的な実体はこれまで明らかにされていなかった.
バイオテクノロジーによる植物の生産能力の増強は,大気のCO2濃度を低減させる有力な手段のひとつと目されている.また,バイオエタノールやバイオディーゼルといった植物の生産物の産業利用(バイオマスエネルギーの利用)もさかんになってきている.バイオテクノロジーを利用して生産力をより強化した植物を作出する試みにおいて,これらの光合成や脂質合成に必要な色素体へのピルビン酸輸送の分子機構が解明されていないことは大きな障壁であった.
C4植物とよばれる一群の植物は,主要穀物であるイネやコムギなどのC3植物に比べ,一般に高い光合成能を示す.大気にあるCO2を濃縮する炭素代謝回路(C4回路)を進化的に獲得していることがその理由で,トウモロコシやサトウキビなどの作物のほか,多くの雑草がC4回路を発達させている.C4回路には葉肉細胞にある葉緑体にピルビン酸(C3)を取り込む活性が認められ,これが色素体におけるピルビン酸輸送の研究例であった(図1).これまでの生化学的な解析によると,C4植物はNa+依存性のピルビン酸輸送を示す植物とH+依存性のピルビン酸輸送を示す植物に大別され1),また,こうしたNa+濃度勾配あるいはH+濃度勾配への依存性は暗所に順応させた葉緑体でのみ認められることが明らかにされている2).ピルビン酸輸送体が同定できれば,こうした生化学的な特徴をささえる分子基盤についても情報が得られるものと期待された.
1.BASS2遺伝子のスクリーニング
筆者らは,この葉緑体へのピルビン酸輸送をつかさどるタンパク質の同定をめざし,フラベリア属においてC3植物である種(Flaveria pringlei)とC4植物である種(F. trinervia)を用いて遺伝子発現の解析を行った.C4植物である種にはC3植物である種と比べ,既知のC4植物と同様に,葉緑体におけるピルビン酸輸送体をコードする遺伝子が高発現していることが期待できる.ディファレンシャルスクリーニング法とRNAシークエンス法という異なる2つの方法により,BASS2遺伝子,BASS4遺伝子,NHD1遺伝子と名づけた,葉緑体への局在を推定させる新規の膜タンパク質をコードする3つの遺伝子を見い出すことに成功した.
筆者らのスクリーニングの成功を知り,イギリスとドイツの研究グループがほぼ同様のスクリーニングを異なる植物で行い報告している3).フラベリア属以外にも,フウチョウソウ属などいくつかの植物にはC3植物である種とC4植物である種が認められる.フウチョウソウ属はシロイヌナズナを含むアブラナ科と近縁な関係にあり,シロイヌナズナにおいて開発されている分子ツールを部分的に利用することが可能である.筆者らの実施したフラベリア属,そして,すでに報告されているフウチョウソウ属におけるディファレンシャルな遺伝子発現の解析において,共通して発現の上昇していた遺伝子はBASS2遺伝子とNHD1遺伝子であった.この結果から,この2つの遺伝子の産物によりピルビン酸の輸送がささえられている可能性が考えられた.BASS2遺伝子は“bile acid sodium symporter family protein 2”,NHD1遺伝子は“sodium hydrogen exchanger 1”としてあたえられた名称である.植物では胆汁酸(bile acid)の存在は疑問視されており,BASS2はおそらく異なる物質を輸送しているであろうと考えられた.一方,NHD1については近縁のタンパク質がNa+とH+の交換輸送能を示したことから4),BASS2がピルビン酸を輸送する本体ではないかと仮説をたてた.
2.抗BASS2抗体によるBASS2の局在の解析
BASS2は7回膜貫通型あるいは9回膜貫通型の膜タンパク質であり,C末端に電荷に富む可溶性の領域をもっていた.この部位に相当するペプチドを合成し,これに対する抗体を作製した.この抗体と交差するタンパク質は,C3植物である種には検出限界以下しか存在しなかったにもかかわらず,C4植物である2種(F. bidentis,F. trinervia)においてともに高発現していた.また,単離した葉肉細胞にある葉緑体の包膜に強く交差を示すタンパク質の存在が認められた.この知見は,葉の横断切片に対する免疫組織染色の結果でも追認され,色素体の表面に交差タンパク質の存在が示された.GFPを付加したBASS2により形質転換したタバコにおいては,根の色素体にその局在性を示した.ついで,C4植物における普遍性を調べたところ,かつてNa+依存性のピルビン酸輸送を示すとされた植物に交差タンパク質が広く認められ,その一方で,H+依存性のピルビン酸輸送を示した植物(トウモロコシおよびソルガム)には交差タンパク質は認められなかった.これらの結果は,BASS2が既知の知見と合致したNa+依存性のピルビン酸輸送体の候補としてふさわしいことを示すとともに,H+依存性のピルビン酸輸送体とは区別されることを示唆した.
3.大腸菌におけるBASS2に依存したピルビン酸の取り込み活性
大腸菌において発現させたBASS2は細胞膜に存在した.このBASS2を発現させた大腸菌と発現していない大腸菌とのあいだでピルビン酸の輸送活性に違いがあるかどうかを検討した.その結果,短い時間においてBASS2に依存するピルビン酸の取り込みを認め,さらに,Na+の濃度に依存して取り込み速度が変化するという結果を得た.これらの結果は,BASS2がNa+依存性のピルビン酸輸送活性をもつ分子実体であることを示していた.
4.大腸菌におけるBASS2とNHD1との共役によるピルビン酸輸送の再構成
BASS2遺伝子と同じ過程でクローニングされたNHD1遺伝子は,さきにも述べたとおり,Na+/H+アンチポーターをコードするものと推定された.この推定された機能とBASS2のNa+依存的なピルビン酸輸送活性とを考えあわせ,ひとつの興味深い仮説を導いた.それは,“BASS2によるピルビン酸の輸送にともない色素体に取り込まれたNa+が,NHD1のはたらきにより排出されより毒性の低いH+に置き換わる”というものである.この仮説では,Na+は共役反応剤として用いられるだけで色素体に蓄積することはない.このBASS2とNHD1との共役によるピルビン酸の輸送機構は,大腸菌においてこの2つを同時に発現させることで検討することができる.その結果,細胞の内外のH+の濃度勾配に依存してNa+の濃度に非依存的にピルビン酸が取り込まれることが確認できた.この結果は,BASS2とNHD1との共役反応が大腸菌において再構成できたことを意味した.
5.シロイヌナズナにおけるBASS2の解析
BASS2遺伝子に相同な遺伝子はこれまでにゲノム解析されたすべての植物のゲノムに存在する.C3植物におけるその生理機能を明らかにするため,シロイヌナズナにおいて遺伝子の発現解析を行った.その結果,成熟した本葉での発現は低いが,子葉,若い本葉,発達中の種子においてある程度まで発現していることを確認した.貯蔵脂質の分解をエネルギーの初発とする子葉では炭素骨格は細胞質にリンゴ酸として供給されるが,リンゴ酸からピルビン酸へは容易に代謝変換されうる.こうした背景から,子葉などの未発達な色素体ではBASS2を介したピルビン酸の取り込みがあり,これが色素体での代謝をささえている可能性が考えられた.そこでとくに,BASS2が色素体におけるピルビン酸を初発とするイソプレノイド代謝に寄与しているかどうかを,特異的な阻害剤と遺伝子破壊植物を用いて検討した.
シロイヌナズナの野生株には播種後1週間目からの抽出液に抗BASS2抗体と交差するタンパク質が存在したが,bass2破壊株には認められなかった.これらの植物から無傷の葉緑体を単離しピルビン酸輸送活性を測定したところ,野生株の葉緑体にはNa+依存性のピルビン酸輸送活性を認めたが,bass2遺伝子破壊株には認められなかった.これらの結果は,C3植物であるシロイヌナズナにおいても生育時期を限定すればBASS2に依存したピルビン輸送活性を観察できることとともに,bass2破壊株ではピルビン酸輸送活性が失われていることを示していた.細胞質におけるイソプレノイド合成経路(メバロン酸経路)と対比して,色素体におけるイソプレノイド合成経路は非メバロン酸経路とよばれている.このように,細胞には2つの独立した代謝経路があり,イソペンテニル二リン酸が細胞質と色素体とを行き来している5).メバロン酸経路の律速酵素の阻害剤を投与しても野生型の植物は大きな形態異常を示さないが,これは色素体におけるイソプレノイド合成により相補されるからであると説明されている.もし,非メバロン酸経路の初発反応におけるピルビン酸の供給にBASS2が寄与しているなら,bass2破壊株はそれが不全となっているため阻害剤に対する相補性が示されなくなっているはずで,阻害剤に対し強い感受性をもつものと期待された.この期待のとおり,bass2変異体は阻害剤への高い感受性を示し,とくに子葉の緑化が遅れるという表現型を示した.
おわりに
オルガネラにおけるピルビン酸の輸送について,今回,はじめてピルビン酸輸送体の同定に成功し,その分子機構についてもNHD1との共役によるという知見を得た(図2).単離したC4植物の葉肉細胞の葉緑体に対し光を照射するとピルビン酸の取り込みにおいてNa+依存性の消失することが報告されているが,この現象はここで得られた知見によりつぎのように説明できる.つまり,光照射により駆動された電子伝達によりチラコイドにおいてH+の組み込みが起こりストロマ側がアルカリ化する.この現象により生じたH+の濃度勾配がNHD1を駆動しBASS2が機能するために細胞質とストロマとのあいだに十分な大きさのNa+濃度勾配が生じ,外液へのNa+の添加のない状態でもピルビン酸の取り込みが可能になるものと考えられる.こうした推察は生化学的な知見をもとにすでになされているが6),今回,ピルビン酸輸送体が同定されたことによりこれを分子レベルで検討することができるようになった.
今後は,脂質合成への寄与を調べる実験をとおしその関与を検討するほか,こうした基礎知見を利用して脂質の含有量を高めた種子をもつ植物を分子育種により開発するという可能性もみえてきた.また,C3植物であるイネにC4植物の光合成能を付与させようという国際プロジェクトが進行中であるが,葉緑体膜を介したピルビン酸の輸送機構がこれまでわからなかったため,こうした研究プロジェクトは停滞を余儀なくされていた.ピルビン酸輸送体の同定によりこれが加速することが期待される.BASS2はトウモロコシなどのH+依存性のピルビン酸輸送体とは区別されたことから,今後,H+依存性のピルビン酸輸送体を同定する試みも必要となろう.また,広範な雑草種でBASS2が検出された一方,トウモロコシにおいて検出されなかったことは,このBASS2の特異的な阻害剤の開発が雑草種に選択的な特性を示す新規の農薬の開発に直結する可能性を示唆している.
文 献
- Aoki, N., Ohnishi, J. & Kanai, R.: Two different mechanisms for transport of pyruvate into mesophyll chloroplasts of C4 plants: a comparative study. Plant Cell Physiol., 33, 805-809 (1992)
- Ohnishi, J. & Kanai, R.: Na+-induced uptake of pyruvate into mesophyll chloroplasts of a C4 plant, Panicum miliaceum. FEBS Lett., 219, 347-350 (1987)
- Brautigam, A., Kajala, K., Wullenweber, J. et al.: An mRNA blueprint for C4 photosynthesis derived from comparative transcriptomics of closely related C3 and C4 species. Plant Physiol., 155, 142-156 (2011)[PubMed]
- Cellier, F., Conejero, G., Lilian Ricaud, L. et al.: Characterization of AtCHX17, a member of the cation/H+ exchangers, CHX family, from Arabidopsis thaliana suggests a role in K+ homeostasis. Plant J., 39, 834-846 (2004)[PubMed]
- Hemmerlin, A., Hoeffler, J. F., Meyer, O. et al.: Cross-talk between the cytosolic mevalonate and the plastidial methylerythritol phosphate pathways in tobacco Bright Yellow-2 cells. J. Biol. Chem., 278, 26666-26676 (2003)[PubMed]
- Aoki, N. & Kanai, R.: Reappraisal of the role of sodium in the light-dependent active transport of pyruvate into mesophyll chloroplasts of C4 plants. Plant Cell Physiol., 38, 1217-1225 (1997)
著者プロフィール
略歴:1999年 京都大学大学院生命科学研究科 修了,同年 東京大学大学院理学系研究科 助手,2000年 京都大学大学院生命科学研究科 助手を経て,2005年より広島大学大学院理学研究科 准教授.
研究テーマ:植物の環境応答の分子機構.
関心事:植物の環境応答能力の高さ(温度やCO2濃度など)に不思議だと感じます.だれも知らない未知の植物の能力に気がつくことができれば,と願っています.
© 2011 古本 強 Licensed under CC 表示 2.1 日本