TRICチャネルの血圧調節への寄与とその遺伝子多型による本態性高血圧のリスク
竹島 浩・山崎大樹
(京都大学大学院薬学研究科 生体分子認識学分野)
email:竹島 浩
DOI: 10.7875/first.author.2011.126
TRIC-A channels in vascular smooth muscle contribute to blood pressure maintenance.
Daiju Yamazaki, Yasuharu Tabara, Satomi Kita, Hironori Hanada, Shinji Komazaki, Daisuke Naitou, Aya Mishima, Miyuki Nishi, Hisao Yamamura, Shinichiro Yamamoto, Sho Kakizawa, Hitoshi Miyachi, Shintaro Yamamoto, Toshiyuki Miyata, Yuhei Kawano, Kei Kamide, Toshio Ogihara, Akira Hata, Satoshi Umemura, Masayoshi Soma, Norio Takahashi, Yuji Imaizumi, Tetsuro Miki, Takahiro Iwamoto, Hiroshi Takeshima
Cell Metabolism, 14, 231-241 (2011)
一価陽イオン透過性のTRICチャネルのサブタイプであるTRIC-AチャネルとTRIC-Bチャネルは,小胞体にカウンターイオンを供給することにより効率的なCa2+放出の成立に寄与していることが推定されている.高血圧を示すTRIC-Aノックアウトマウスの血管平滑筋細胞では,小胞体のリアノジン受容体と細胞膜のCa2+依存性K+チャネルとの共役により発生する過分極シグナルが障害されており,興奮性の亢進による電位依存性Ca2+チャネルの異常な活性化が観察された.したがって,TRIC-Aチャネルはリアノジン受容体によるCa2+放出機構を支援する機能をもつものと思われた.一方,正常血圧群と高血圧患者群においてヒトTRIC-A遺伝子における一塩基多型を検討した結果,日本人の約7%に観察される遺伝子型において本態性高血圧の発症が約18%上昇するものと考察された.さらに,この高血圧リスクを示す遺伝子型をもつ高血圧患者では,一般に処方される降圧薬に対し抵抗性を示すことも判明した.
小胞体はCa2+ストア機能を備えており,小胞体からのCa2+放出による細胞質におけるCa2+濃度の上昇は生体恒常性や細胞機能の維持に不可欠である.小胞体からのCa2+放出を担当するイオンチャネルとしてはリアノジン受容体とイノシトールトリスリン酸受容体が知られ,それぞれ独自の機構により開口することで小胞体Ca2+シグナルを発生させる.これらチャネルの開口にともない小胞体より陽イオンであるCa2+が流出すると,小胞体の内腔に負電荷が発生するため以降の小胞体からのCa2+放出は抑制されることが想像される1).生理的な条件で観察される数十ミリ秒にも及ぶ小胞体からのCa2+放出が持続するためには,この負電荷を中和する機構が必要であると古くから想定されている2).この機構の一翼を担う分子的な実体であるカウンターイオンチャネルとして,筆者らは数年前,一価陽イオン透過性のTRICチャネルを同定した3,4).動物においてはTRIC-AチャネルとTRIC-Bチャネルの2種類のサブタイプが独自の組織特異的なパターンにより分布している.この2つのサブタイプは3本の膜貫通セグメントをもち核膜や小胞体膜においてホモ三量体を形成し,細胞内環境においてはおもにK+透過性チャネルとして機能している.TRIC-AチャネルとTRIC-Bチャネルのダブルノックアウトマウスは胎生期に心不全により致死となり3),TRIC-Bノックアウトマウスは出生時に肺胞の機能障害による呼吸不全により致死となる5).TRIC-Aノックアウトマウスは致死性を示さず,骨格筋にて軽度の形態および生理的な異常が観察されていたが6),興奮性の組織に分布するTRIC-Aチャネルの生理機能の詳細は検討されていなかった.
マウスは夜行性であり,交感神経系が優位な夜間に血圧が上昇する.テレメトリー血圧計測によりTRIC-Aノックアウトマウスは昼間の時間帯のみ高血圧を示すことが明らかになった.テールカフ法により各種の降圧薬(ほぼ最大効果の投薬量)に対する効果を正常マウスとTRIC-Aノックアウトマウスとで比較したところ,多くの薬物で同じ程度の効果が観察されたものの,電位依存性Ca2+チャネル阻害薬でのみTRIC-Aノックアウトマウスにて顕著な降圧効果が観察された.したがって,TRIC-Aノックアウトマウスは脳梗塞や心筋梗塞の発生リスクがとくに高いとされる夜間高血圧症の有用な動物モデルであり,Ca2+チャネル阻害薬の標的となる血管の収縮亢進が高血圧の原因であると推定された.
血圧の動態は末梢動脈である抵抗血管の収縮により支配されているため,代表的な抵抗血管である腸間膜動脈を調製しその血管径を測定した.最大弛緩を誘導するCa2+非含有溶液においてはTRIC-Aノックアウトマウスの血管に異常はないが,通常のCa2+含有溶液においてはTRIC-Aノックアウトマウスの血管は正常な血管に比べ顕著に細いことが判明した.したがって,TRIC-Aの欠損による血管平滑筋の収縮の亢進が高血圧の主原因であることが再確認された.
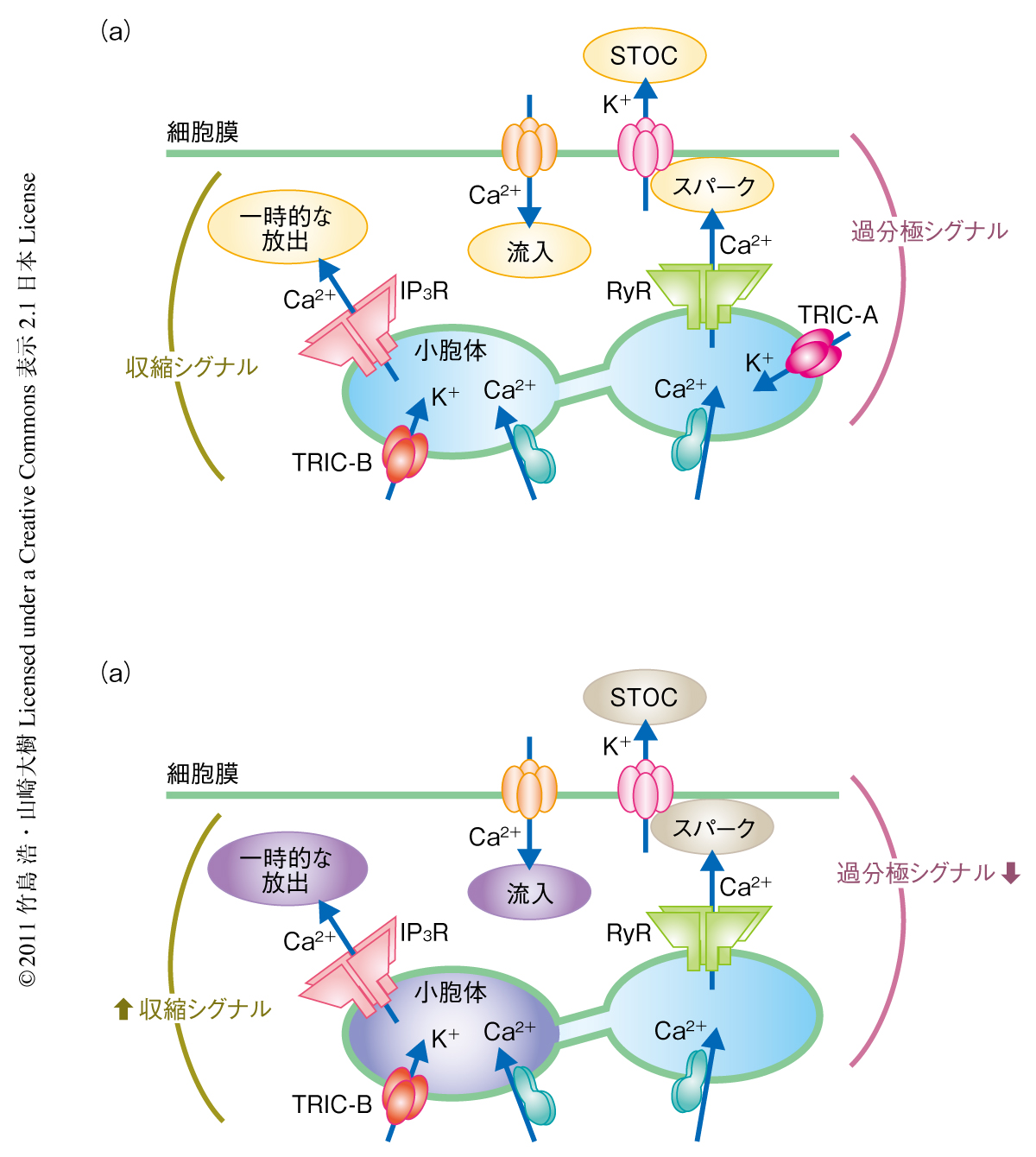
細胞におけるCa2+濃度を蛍光色素法により測定したところ,TRIC-Aノックアウトマウスの血管平滑筋細胞では定常状態における細胞内Ca2+濃度が顕著に上昇していることが観察された.細胞外液からのCa2+除去や電位依存性Ca2+チャネル阻害薬により正常な血管平滑筋細胞と同じ程度まで細胞内Ca2+濃度は低下することから,TRIC-Aチャネルを欠損した細胞におけるCa2+濃度の上昇は,電位依存性Ca2+チャネルが仲介する細胞外からのCa2+流入の亢進が原因であると考えられた(図1).さらに,TRIC-Aチャネルを欠損した血管平滑筋細胞では小胞体におけるCa2+貯蔵量の増大やアドレナリン刺激によるイノシトールトリスリン酸受容体を介したCa2+放出の増強も観察されたが,これらの異常が直接的な高血圧の原因とは考えられなかった.
血管平滑筋におけるリアノジン受容体の自発的な開口によるCa2+放出はCa2+スパークとして観察され,細胞膜にあるCa2+依存性K+チャネルを活性化して細胞膜を過分極させることにより,電位依存性Ca2+チャネルを不活性化させてCa2+流入を抑制する結果,血管を弛緩させる(血圧低下)ことが知られている7,8).蛍光イメージングやパッチクランプ測定により,TRIC-Aチャネルを欠損した血管平滑筋細胞ではCa2+スパークの発生頻度の低下,Ca2+依存性K+チャネルによる一過性外向き電流の発生頻度の減少,静止膜電位の上昇が観察された.したがって,このTRIC-Aチャネルを欠損した血管平滑筋細胞では過分極シグナルの発生が障害されていることにより,電気的興奮性が亢進し電位依存性Ca2+チャネルが顕著に活性化されていることが判明した.この異常は静止状態でのCa2+濃度の上昇と血管収縮性の亢進を誘導し,TRIC-Aノックアウトマウスの高血圧の直接の原因になるものと考えられた.
日本人集団の高血圧ケースコントロール試験において,PCR法により一塩基多型(SNP)を検討した結果,TRIC-A遺伝子を中心とする約100 kbに分布する連鎖SNPは本態性高血圧のリスクを上昇させることが示唆された.代表的なSNP例として,TRIC-A遺伝子領域に存在するrs17796739において日本人ゲノム集団ではCが74%,Tが26%の頻度で存在した.この部位での低頻度Tのホモ接合体(14人に1人の確率)では,統計的に有意(p = 0.018)に高血圧を発症するとともに,発症リスクが約18%上昇するものと算出された.また,rs901792においても低頻度Cのホモ接合体では,統計的に有意(p = 0.048)に高血圧を発症するとともに,発症リスクが約14%上昇すると算出された.
すでに,汎用される降圧薬であるサイアザイド利尿薬,アンジオテンシンII受容体拮抗薬,Ca2+チャネル阻害薬を約130名の高血圧患者に処方し,それぞれの降圧効果を検討するとともに,血液試料から遺伝子を抽出する臨床試験が行われていた.この臨床試験においてTRIC-A遺伝子多型に注目したところ,高血圧のリスクを示す多型は降圧作用を規定していることが示された.たとえば,rs901792では高血圧のリスクを示す多型であるCのホモ接合体において3つの降圧薬に対する抵抗性が示された.降圧効果は薬物治療まえの血圧値に依存することから,より正確な薬理効果の検討においては前値補正とともに,収縮期血圧,平均血圧,拡張期血圧に分割した評価が求められる.前値補正を含めた検討においても,TRIC-A遺伝子多型において高血圧のリスクを示す多型であるホモ接合体では降圧薬に対する抵抗性が確認された.
血管平滑筋細胞ではリアノジン受容体とイノシトールトリスリン酸受容体とが共存しており,TRIC-AチャネルとTRIC-Bチャネルも共発現している(図1).TRIC-Aチャネルの欠損によりリアノジン受容体の活性抑制は観察されたものの,イノシトールトリスリン酸受容体の機能障害は認められなかった.したがって,TRIC-Aチャネルとリアノジン受容体,TRIC-Bチャネルとイノシトールトリスリン酸受容体という機能共役ペアが想像されるものの,どのような機序で選択的な機能共役が成立するのかについては今後の課題である.また,TRIC-Aチャネルの欠損によりイノシトールトリスリン酸感受性ストアのCa2+過剰負荷が観察されたが,その形成の機構も不明である.一方,ヒトにおける遺伝子解析により得られた結果からは,TRIC-A遺伝子多型の検査が高血圧予防,降圧薬の選択や用量決定などの個別化医療に貢献することも期待される.
略歴:1989年 京都大学大学院医学研究科 修了,同年 京都大学医学部 助手,1995年 東京大学医学部 助教授,2001年 東北大学大学院医学系研究科 教授を経て,2006年より京都大学大学院薬学研究科 教授.
研究テーマ:小胞体Ca2+シグナル伝達.
関心事:生物学領域でのアカデミック研究人材の確保と再生産.
研究室URL:http://www.pharm.kyoto-u.ac.jp/biochem/index.html
山崎 大樹(Daiju Yamazaki)
京都大学大学院薬学研究科 特定講師.
© 2011 竹島 浩・山崎大樹 Licensed under CC 表示 2.1 日本
(京都大学大学院薬学研究科 生体分子認識学分野)
email:竹島 浩
DOI: 10.7875/first.author.2011.126
TRIC-A channels in vascular smooth muscle contribute to blood pressure maintenance.
Daiju Yamazaki, Yasuharu Tabara, Satomi Kita, Hironori Hanada, Shinji Komazaki, Daisuke Naitou, Aya Mishima, Miyuki Nishi, Hisao Yamamura, Shinichiro Yamamoto, Sho Kakizawa, Hitoshi Miyachi, Shintaro Yamamoto, Toshiyuki Miyata, Yuhei Kawano, Kei Kamide, Toshio Ogihara, Akira Hata, Satoshi Umemura, Masayoshi Soma, Norio Takahashi, Yuji Imaizumi, Tetsuro Miki, Takahiro Iwamoto, Hiroshi Takeshima
Cell Metabolism, 14, 231-241 (2011)
要 約
一価陽イオン透過性のTRICチャネルのサブタイプであるTRIC-AチャネルとTRIC-Bチャネルは,小胞体にカウンターイオンを供給することにより効率的なCa2+放出の成立に寄与していることが推定されている.高血圧を示すTRIC-Aノックアウトマウスの血管平滑筋細胞では,小胞体のリアノジン受容体と細胞膜のCa2+依存性K+チャネルとの共役により発生する過分極シグナルが障害されており,興奮性の亢進による電位依存性Ca2+チャネルの異常な活性化が観察された.したがって,TRIC-Aチャネルはリアノジン受容体によるCa2+放出機構を支援する機能をもつものと思われた.一方,正常血圧群と高血圧患者群においてヒトTRIC-A遺伝子における一塩基多型を検討した結果,日本人の約7%に観察される遺伝子型において本態性高血圧の発症が約18%上昇するものと考察された.さらに,この高血圧リスクを示す遺伝子型をもつ高血圧患者では,一般に処方される降圧薬に対し抵抗性を示すことも判明した.
はじめに
小胞体はCa2+ストア機能を備えており,小胞体からのCa2+放出による細胞質におけるCa2+濃度の上昇は生体恒常性や細胞機能の維持に不可欠である.小胞体からのCa2+放出を担当するイオンチャネルとしてはリアノジン受容体とイノシトールトリスリン酸受容体が知られ,それぞれ独自の機構により開口することで小胞体Ca2+シグナルを発生させる.これらチャネルの開口にともない小胞体より陽イオンであるCa2+が流出すると,小胞体の内腔に負電荷が発生するため以降の小胞体からのCa2+放出は抑制されることが想像される1).生理的な条件で観察される数十ミリ秒にも及ぶ小胞体からのCa2+放出が持続するためには,この負電荷を中和する機構が必要であると古くから想定されている2).この機構の一翼を担う分子的な実体であるカウンターイオンチャネルとして,筆者らは数年前,一価陽イオン透過性のTRICチャネルを同定した3,4).動物においてはTRIC-AチャネルとTRIC-Bチャネルの2種類のサブタイプが独自の組織特異的なパターンにより分布している.この2つのサブタイプは3本の膜貫通セグメントをもち核膜や小胞体膜においてホモ三量体を形成し,細胞内環境においてはおもにK+透過性チャネルとして機能している.TRIC-AチャネルとTRIC-Bチャネルのダブルノックアウトマウスは胎生期に心不全により致死となり3),TRIC-Bノックアウトマウスは出生時に肺胞の機能障害による呼吸不全により致死となる5).TRIC-Aノックアウトマウスは致死性を示さず,骨格筋にて軽度の形態および生理的な異常が観察されていたが6),興奮性の組織に分布するTRIC-Aチャネルの生理機能の詳細は検討されていなかった.
1.TRIC-Aノックアウトマウスにおける高血圧
マウスは夜行性であり,交感神経系が優位な夜間に血圧が上昇する.テレメトリー血圧計測によりTRIC-Aノックアウトマウスは昼間の時間帯のみ高血圧を示すことが明らかになった.テールカフ法により各種の降圧薬(ほぼ最大効果の投薬量)に対する効果を正常マウスとTRIC-Aノックアウトマウスとで比較したところ,多くの薬物で同じ程度の効果が観察されたものの,電位依存性Ca2+チャネル阻害薬でのみTRIC-Aノックアウトマウスにて顕著な降圧効果が観察された.したがって,TRIC-Aノックアウトマウスは脳梗塞や心筋梗塞の発生リスクがとくに高いとされる夜間高血圧症の有用な動物モデルであり,Ca2+チャネル阻害薬の標的となる血管の収縮亢進が高血圧の原因であると推定された.
2.TRIC-Aチャネルを欠損した血管平滑筋の収縮とCa2+動態の異常
血圧の動態は末梢動脈である抵抗血管の収縮により支配されているため,代表的な抵抗血管である腸間膜動脈を調製しその血管径を測定した.最大弛緩を誘導するCa2+非含有溶液においてはTRIC-Aノックアウトマウスの血管に異常はないが,通常のCa2+含有溶液においてはTRIC-Aノックアウトマウスの血管は正常な血管に比べ顕著に細いことが判明した.したがって,TRIC-Aの欠損による血管平滑筋の収縮の亢進が高血圧の主原因であることが再確認された.
細胞におけるCa2+濃度を蛍光色素法により測定したところ,TRIC-Aノックアウトマウスの血管平滑筋細胞では定常状態における細胞内Ca2+濃度が顕著に上昇していることが観察された.細胞外液からのCa2+除去や電位依存性Ca2+チャネル阻害薬により正常な血管平滑筋細胞と同じ程度まで細胞内Ca2+濃度は低下することから,TRIC-Aチャネルを欠損した細胞におけるCa2+濃度の上昇は,電位依存性Ca2+チャネルが仲介する細胞外からのCa2+流入の亢進が原因であると考えられた(図1).さらに,TRIC-Aチャネルを欠損した血管平滑筋細胞では小胞体におけるCa2+貯蔵量の増大やアドレナリン刺激によるイノシトールトリスリン酸受容体を介したCa2+放出の増強も観察されたが,これらの異常が直接的な高血圧の原因とは考えられなかった.
3.TRIC-Aチャネルを欠損した血管平滑筋細胞における過分極シグナル障害
血管平滑筋におけるリアノジン受容体の自発的な開口によるCa2+放出はCa2+スパークとして観察され,細胞膜にあるCa2+依存性K+チャネルを活性化して細胞膜を過分極させることにより,電位依存性Ca2+チャネルを不活性化させてCa2+流入を抑制する結果,血管を弛緩させる(血圧低下)ことが知られている7,8).蛍光イメージングやパッチクランプ測定により,TRIC-Aチャネルを欠損した血管平滑筋細胞ではCa2+スパークの発生頻度の低下,Ca2+依存性K+チャネルによる一過性外向き電流の発生頻度の減少,静止膜電位の上昇が観察された.したがって,このTRIC-Aチャネルを欠損した血管平滑筋細胞では過分極シグナルの発生が障害されていることにより,電気的興奮性が亢進し電位依存性Ca2+チャネルが顕著に活性化されていることが判明した.この異常は静止状態でのCa2+濃度の上昇と血管収縮性の亢進を誘導し,TRIC-Aノックアウトマウスの高血圧の直接の原因になるものと考えられた.
4.ヒトにおけるTRIC-A遺伝子多型と高血圧
日本人集団の高血圧ケースコントロール試験において,PCR法により一塩基多型(SNP)を検討した結果,TRIC-A遺伝子を中心とする約100 kbに分布する連鎖SNPは本態性高血圧のリスクを上昇させることが示唆された.代表的なSNP例として,TRIC-A遺伝子領域に存在するrs17796739において日本人ゲノム集団ではCが74%,Tが26%の頻度で存在した.この部位での低頻度Tのホモ接合体(14人に1人の確率)では,統計的に有意(p = 0.018)に高血圧を発症するとともに,発症リスクが約18%上昇するものと算出された.また,rs901792においても低頻度Cのホモ接合体では,統計的に有意(p = 0.048)に高血圧を発症するとともに,発症リスクが約14%上昇すると算出された.
5.ヒトにおけるTRIC-A遺伝子多型と降圧薬の薬理効果
すでに,汎用される降圧薬であるサイアザイド利尿薬,アンジオテンシンII受容体拮抗薬,Ca2+チャネル阻害薬を約130名の高血圧患者に処方し,それぞれの降圧効果を検討するとともに,血液試料から遺伝子を抽出する臨床試験が行われていた.この臨床試験においてTRIC-A遺伝子多型に注目したところ,高血圧のリスクを示す多型は降圧作用を規定していることが示された.たとえば,rs901792では高血圧のリスクを示す多型であるCのホモ接合体において3つの降圧薬に対する抵抗性が示された.降圧効果は薬物治療まえの血圧値に依存することから,より正確な薬理効果の検討においては前値補正とともに,収縮期血圧,平均血圧,拡張期血圧に分割した評価が求められる.前値補正を含めた検討においても,TRIC-A遺伝子多型において高血圧のリスクを示す多型であるホモ接合体では降圧薬に対する抵抗性が確認された.
おわりに
血管平滑筋細胞ではリアノジン受容体とイノシトールトリスリン酸受容体とが共存しており,TRIC-AチャネルとTRIC-Bチャネルも共発現している(図1).TRIC-Aチャネルの欠損によりリアノジン受容体の活性抑制は観察されたものの,イノシトールトリスリン酸受容体の機能障害は認められなかった.したがって,TRIC-Aチャネルとリアノジン受容体,TRIC-Bチャネルとイノシトールトリスリン酸受容体という機能共役ペアが想像されるものの,どのような機序で選択的な機能共役が成立するのかについては今後の課題である.また,TRIC-Aチャネルの欠損によりイノシトールトリスリン酸感受性ストアのCa2+過剰負荷が観察されたが,その形成の機構も不明である.一方,ヒトにおける遺伝子解析により得られた結果からは,TRIC-A遺伝子多型の検査が高血圧予防,降圧薬の選択や用量決定などの個別化医療に貢献することも期待される.
文 献
- Yamazaki, T., Yamazaki, D. & Takeshima, H.: New molecular components supporting ryanodine receptor-mediated Ca2+ release: roles of junctophilin and TRIC channel in embryonic cardiomyocyes. Pharmacol. Ther., 121, 265-272 (2009)[PubMed]
- Meissner, G.: Monovalent ion and calcium ion fluxes in sarcoplasmic reticulum. Mol. Cell. Biochem., 55, 65-82 (1983)[PubMed]
- Yazawa, M., Ferrante, C., Feng, J. et al.: TRIC channels are essential for Ca2+ handling in intracellular stores. Nature, 448, 78-82 (2007)[PubMed]
- Pitt, S. J., Park, K. -H., Nishi, M. et al.: Charade of the SR K+-channel: two ion-channels, TRIC-A and TRIC-B, masquerade as a single K+-channel. Biophys. J., 99, 417-426 (2010)[PubMed]
- Yamazaki, D., Komazaki, S., Nakanishi, H. et al.: Essential role of TRIC-B channel in Ca2+-handling of alveolar epithelium and perinatal lung maturation. Development, 136, 2355-2361 (2009)[PubMed]
- Zhao, X., Yamazaki, D., Park, K. -H. et al.: Ca2+ overload and sarcoplasmic reticulum instability in tric-a null skeletal muscle. J. Biol. Chem., 285, 37370-37376 (2010)[PubMed]
- Berridge, M. J.: Smooth muscle cell calcium activation mechanisms. J. Physiol., 586, 5047-5061 (2008)[PubMed]
- Amberg, G. C., Navedo, M. F., Nieves-Cintron, M. et al.: Calcium sparklets regulate local and global calcium in murine arterial smooth muscle. J. Physiol., 579, 187-201 (2007)[PubMed]
著者プロフィール
略歴:1989年 京都大学大学院医学研究科 修了,同年 京都大学医学部 助手,1995年 東京大学医学部 助教授,2001年 東北大学大学院医学系研究科 教授を経て,2006年より京都大学大学院薬学研究科 教授.
研究テーマ:小胞体Ca2+シグナル伝達.
関心事:生物学領域でのアカデミック研究人材の確保と再生産.
研究室URL:http://www.pharm.kyoto-u.ac.jp/biochem/index.html
山崎 大樹(Daiju Yamazaki)
京都大学大学院薬学研究科 特定講師.
© 2011 竹島 浩・山崎大樹 Licensed under CC 表示 2.1 日本