ヒトにおける栄養膜幹細胞の樹立
岡江寛明・有馬隆博
(東北大学大学院医学系研究科 環境遺伝医学総合研究センター情報遺伝学分野)
email:岡江寛明
DOI: 10.7875/first.author.2018.004
Derivation of human trophoblast stem cells.
Hiroaki Okae, Hidehiro Toh, Tetsuya Sato, Hitoshi Hiura, Sota Takahashi, Kenjiro Shirane, Yuka Kabayama, Mikita Suyama, Hiroyuki Sasaki, Takahiro Arima
Cell Stem Cell, 22, 50-63.e6 (2018)
胎盤は胎児の発育に欠かすことのできない重要な器官である.胎盤において主要な機能を担う細胞は栄養膜細胞とよばれ,栄養膜幹細胞より分化する.マウスにおいて栄養膜幹細胞を培養する技術が確立されて20年近くがたったが,これまで,ヒトにおいて栄養膜幹細胞は樹立されていない.この研究において,筆者らは,ヒトの胎盤より分離した栄養膜細胞において遺伝子の発現を解析し,栄養膜細胞の増殖を促進するシグナルをつきとめた.この結果をもとに培養の条件を検討することにより,栄養膜細胞の長期培養系が確立された.得られた細胞株は多分化能を維持したまま5カ月以上にわたり培養することが可能で,生体の栄養膜細胞とよく似た遺伝子の発現パターンおよびDNAメチル化のパターンを保持していた.さらに,ヒトの胚盤胞からも同様の性質をもつ細胞株が樹立された.以上より,栄養膜細胞および胚盤胞より樹立した細胞株はヒトの栄養膜幹細胞であると結論づけられた.ヒトの栄養膜幹細胞は胎盤の分化および機能を研究するうえですぐれたモデルとなるとともに,流早産や妊娠高血圧症候群など胎盤の形成不全によりひき起こされる疾患の病態の解明に役だつと期待される.
胎盤は母体と胎児とをつなぐ重要な器官であり,胎児の呼吸器,消化器,内分泌器としてはたらくとともに,母体の免疫系から胎児をまもる役割を担う.胎盤において主要な機能を担う細胞は栄養膜細胞とよばれ,ヒトの場合,細胞性栄養膜細胞,絨毛外性栄養膜細胞,合胞体性栄養膜細胞の3種類に大別される(図1).細胞性栄養膜細胞は高い増殖能をもつ上皮細胞であり,絨毛外性栄養膜細胞および合胞体性栄養膜細胞へと分化する能力をもつ.絨毛外性栄養膜細胞は子宮内膜に浸潤し,らせん動脈を再構築することにより母体血の流れを制御する.合胞体性栄養膜細胞は細胞性栄養膜細胞の融合によりつくられる多核の細胞であり,栄養およびガスの交換やホルモンの産生にはたらく.
胎盤を構成するすべての栄養膜細胞は胚盤胞期の栄養外胚葉に由来する.マウスにおいては,栄養外胚葉あるいは着床後胚の胚体外外胚葉をFGF4の存在下において培養することにより栄養膜幹細胞が樹立されることが報告されている1).マウスの栄養膜幹細胞は半永久的に増殖が可能で,胚盤胞に注入すると胎盤を構成するすべての栄養膜細胞に分化する能力をもつ.マウスにおける栄養膜幹細胞の樹立をうけ,これまで,多くの研究者がヒトにおいて栄養膜幹細胞の樹立を試みたが成功したという報告はない.
細胞性栄養膜細胞は生体においては高い増殖能をもつが,汎用の培地にて培養するとすみやかに増殖を停止し,合胞体性栄養膜細胞へと分化することが知られている.生体において細胞性栄養膜細胞の増殖がどのように制御されているのかを理解するため,妊娠初期のヒトの胎盤より細胞性栄養膜細胞,絨毛外性栄養膜細胞,合胞体性栄養膜細胞を高純度で分離した.これらをRNA-seq法により解析したところ,それぞれの細胞種に特異的に発現する遺伝子が同定された.細胞性栄養膜細胞に特異的に発現する遺伝子に着目してパスウェイ解析を行ったところ,WntシグナルやEGFシグナルに関与するシグナル伝達経路が濃縮されていた.
パスウェイ解析の結果をもとに,Wntシグナルを活性化するGSK3阻害剤およびEGFの存在下において細胞性栄養膜細胞の培養を試みたが,この条件においては長期の培養はできなかった.そこで,上皮系の幹細胞の増殖を促進する増殖因子や小分子化合物をさまざまな組合せで培養液に添加した.その結果,GSK3阻害剤,EGF,TGFβ阻害剤,ヒストン脱アセチル化酵素阻害剤,ROCK阻害剤を用いることにより,細胞性栄養膜細胞は5カ月以上にわたり培養が可能であった.これは,約150回の細胞分裂に相当した.GSK3阻害剤およびEGFは細胞性栄養膜細胞の生存および増殖に必須であり,ROCK阻害剤は細胞性栄養膜細胞の培養プレートへの接着に重要であった.また,TGFβ阻害剤およびヒストン脱アセチル化酵素阻害剤は細胞の増殖を有意に促進した.得られた細胞性栄養膜細胞株は栄養膜細胞の特異的なマーカーであるKRT7に陽性かつHLAクラスI分子に陰性であった.
ヒトの胚盤胞より細胞性栄養膜細胞株に類似した細胞株が樹立されるかどうか検討した.計16個の胚盤胞をさきと同じ培養液を用いて培養したところ,細胞性栄養膜細胞株と非常によく似た8系統の細胞株が樹立された.以下に示すように,細胞性栄養膜細胞株および胚盤胞より樹立した細胞株は絨毛外性栄養膜細胞および合胞体性栄養膜細胞への分化能をもっていたことから,これらの細胞株はヒトの栄養膜幹細胞であると結論づけた.
ヒトの絨毛がん細胞株を用いた研究により,合胞体性栄養膜細胞への分化においてcAMPが重要であることが知られていた2).そこで,cAMPの濃度を上昇させるフォルスコリンによりヒトの栄養膜幹細胞を処理したところ,細胞融合が起こり大部分の細胞が多核の合胞体性栄養膜細胞様の細胞へと分化した(図2).この細胞は合胞体性栄養膜細胞の特異的なマーカーであるSDC1に陽性であり,妊娠中に産生されるホルモンのひとつであるヒトの絨毛性ゴナドトロピンを大量に放出していた.さらに,RNA-seq法による解析により,合胞体性栄養膜細胞様の細胞と生体の合胞体性栄養膜細胞とは非常によく似た遺伝子の発現パターンをもつことが明らかにされた.
ヒトの栄養膜幹細胞の培養の条件を検討する過程において,TGFβ阻害剤が細胞性栄養膜細胞から絨毛外性栄養膜細胞への分化を促進することが見い出された.これにくわえ,ヒトの胎盤絨毛の体外培養系を用いた研究により,NRG1およびマトリゲルが絨毛外性栄養膜細胞への分化を促進することが示唆されていた3,4).そこで,TGFβ阻害剤,NRG1,マトリゲルの存在においてヒトの栄養膜幹細胞を培養したところ,上皮間葉転換が起こり紡錘形の絨毛外性栄養膜細胞様の細胞へと分化した(図2).この細胞は絨毛外性栄養膜細胞の特異的なマーカーであるHLA-Gに陽性であり,さらに生体の絨毛外性栄養膜細胞と非常によく似た遺伝子の発現パターンをもっていた.
ヒトの栄養膜細胞は以下に示すユニークなDNAメチル化のパターンをもつことが知られている.1)通常,体細胞のゲノムはプロモーター領域やエンハンサー領域を除いて高メチル化の状態にあるが,ヒトの栄養膜細胞はゲノムの約40%が中程度のメチル化の状態を示す5).2)胎児および胎児に由来する細胞において高メチル化の状態にあるプロモーター領域の一部が,ヒトの栄養膜細胞においては低メチル化の状態にある.3)ヒトの栄養膜細胞においてのみアレルに特異的なDNAメチル化を示す領域が多く存在する6,7).これらの特徴がヒトの栄養膜幹細胞において維持されているかどうかを調べるため,バイサルファイトシークエンス法により解析した結果,一部に例外はあったものの,これらの特徴はヒトの栄養膜幹細胞においておおむね維持されていた.
ヒトの栄養膜幹細胞が生体においても機能するかどうか解析するため,免疫不全マウスであるNOD-SCIDマウスの皮下へと移植した.ヒトの栄養膜幹細胞は移植されたマウスの真皮および皮下組織に浸潤し,辺縁部の細胞の一部はHLA-Gに陽性の絨毛外性栄養膜細胞様の細胞やSDC1に陽性の合胞体性栄養膜細胞様の細胞へと分化した.一部の合胞体性栄養膜細胞様の細胞には空胞が生じ血液が流入していた.この構造は,ヒトの胚盤胞が子宮に着床する際につくられる原始合胞体性栄養膜細胞と酷似していた8).さらに,移植されたマウスの血中には多量のヒトの絨毛性ゴナドトロピンが認められた.以上より,免疫不全マウスにヒトの栄養膜幹細胞を移植することにより,着床の現象の一部が再現されることが明らかにされた.
この研究においてもっとも苦労したのは,ヒトの栄養膜幹細胞の樹立そのものではなく,樹立した細胞株が栄養膜幹細胞であることをいかに証明するかということであった.マウスの場合,胚盤胞に注入した細胞が胎盤に寄与するかどうかを解析することにより栄養膜幹細胞であることは簡単に証明される.一方,ヒトの胚を用いたキメラの作製は倫理的に許されない.そのため,この研究においては,樹立した細胞株をさまざまな角度から解析することによりヒトの栄養膜幹細胞であることが“ほぼ”証明されたと考えている.ヒトの栄養膜幹細胞がキメラの形成能をもつかどうかという問題は残されたままであるが,今後,異種間のキメラの作製や非ヒト霊長類における栄養膜幹細胞の樹立などにより解決される可能性がある.
略歴:2010年 東京大学大学院理学系研究科 修了,同年 東北大学大学院医学系研究科 研究員を経て,2012年より同 助教.
研究テーマ:胎盤とゲノムインプリンティング.
抱負:胎盤の機能は哺乳類のあいだで保存されているものの,その形態や構成する細胞はきわめて多様です.このような多様性がなぜ,どのように生じるのかを理解したいと考えています.
有馬 隆博(Takahiro Arima)
東北大学大学院医学系研究科 教授.
© 2018 岡江寛明・有馬隆博 Licensed under CC 表示 2.1 日本
(東北大学大学院医学系研究科 環境遺伝医学総合研究センター情報遺伝学分野)
email:岡江寛明
DOI: 10.7875/first.author.2018.004
Derivation of human trophoblast stem cells.
Hiroaki Okae, Hidehiro Toh, Tetsuya Sato, Hitoshi Hiura, Sota Takahashi, Kenjiro Shirane, Yuka Kabayama, Mikita Suyama, Hiroyuki Sasaki, Takahiro Arima
Cell Stem Cell, 22, 50-63.e6 (2018)
この論文に出現する遺伝子・タンパク質のUniprot ID
FGF4(P11403), Wnt, EGF(P01133), GSK3, TGFβ, ヒストン脱アセチル化酵素, ROCK, KRT7(P08729), HLAクラスI, SDC1(P18827), 絨毛性ゴナドトロピン, NRG1(Q02297), HLA-G(P17693), HDAC
要 約
胎盤は胎児の発育に欠かすことのできない重要な器官である.胎盤において主要な機能を担う細胞は栄養膜細胞とよばれ,栄養膜幹細胞より分化する.マウスにおいて栄養膜幹細胞を培養する技術が確立されて20年近くがたったが,これまで,ヒトにおいて栄養膜幹細胞は樹立されていない.この研究において,筆者らは,ヒトの胎盤より分離した栄養膜細胞において遺伝子の発現を解析し,栄養膜細胞の増殖を促進するシグナルをつきとめた.この結果をもとに培養の条件を検討することにより,栄養膜細胞の長期培養系が確立された.得られた細胞株は多分化能を維持したまま5カ月以上にわたり培養することが可能で,生体の栄養膜細胞とよく似た遺伝子の発現パターンおよびDNAメチル化のパターンを保持していた.さらに,ヒトの胚盤胞からも同様の性質をもつ細胞株が樹立された.以上より,栄養膜細胞および胚盤胞より樹立した細胞株はヒトの栄養膜幹細胞であると結論づけられた.ヒトの栄養膜幹細胞は胎盤の分化および機能を研究するうえですぐれたモデルとなるとともに,流早産や妊娠高血圧症候群など胎盤の形成不全によりひき起こされる疾患の病態の解明に役だつと期待される.
はじめに
胎盤は母体と胎児とをつなぐ重要な器官であり,胎児の呼吸器,消化器,内分泌器としてはたらくとともに,母体の免疫系から胎児をまもる役割を担う.胎盤において主要な機能を担う細胞は栄養膜細胞とよばれ,ヒトの場合,細胞性栄養膜細胞,絨毛外性栄養膜細胞,合胞体性栄養膜細胞の3種類に大別される(図1).細胞性栄養膜細胞は高い増殖能をもつ上皮細胞であり,絨毛外性栄養膜細胞および合胞体性栄養膜細胞へと分化する能力をもつ.絨毛外性栄養膜細胞は子宮内膜に浸潤し,らせん動脈を再構築することにより母体血の流れを制御する.合胞体性栄養膜細胞は細胞性栄養膜細胞の融合によりつくられる多核の細胞であり,栄養およびガスの交換やホルモンの産生にはたらく.
胎盤を構成するすべての栄養膜細胞は胚盤胞期の栄養外胚葉に由来する.マウスにおいては,栄養外胚葉あるいは着床後胚の胚体外外胚葉をFGF4の存在下において培養することにより栄養膜幹細胞が樹立されることが報告されている1).マウスの栄養膜幹細胞は半永久的に増殖が可能で,胚盤胞に注入すると胎盤を構成するすべての栄養膜細胞に分化する能力をもつ.マウスにおける栄養膜幹細胞の樹立をうけ,これまで,多くの研究者がヒトにおいて栄養膜幹細胞の樹立を試みたが成功したという報告はない.
1.栄養膜細胞の増殖を制御するシグナルの同定
細胞性栄養膜細胞は生体においては高い増殖能をもつが,汎用の培地にて培養するとすみやかに増殖を停止し,合胞体性栄養膜細胞へと分化することが知られている.生体において細胞性栄養膜細胞の増殖がどのように制御されているのかを理解するため,妊娠初期のヒトの胎盤より細胞性栄養膜細胞,絨毛外性栄養膜細胞,合胞体性栄養膜細胞を高純度で分離した.これらをRNA-seq法により解析したところ,それぞれの細胞種に特異的に発現する遺伝子が同定された.細胞性栄養膜細胞に特異的に発現する遺伝子に着目してパスウェイ解析を行ったところ,WntシグナルやEGFシグナルに関与するシグナル伝達経路が濃縮されていた.
2.ヒトの栄養膜幹細胞の樹立
パスウェイ解析の結果をもとに,Wntシグナルを活性化するGSK3阻害剤およびEGFの存在下において細胞性栄養膜細胞の培養を試みたが,この条件においては長期の培養はできなかった.そこで,上皮系の幹細胞の増殖を促進する増殖因子や小分子化合物をさまざまな組合せで培養液に添加した.その結果,GSK3阻害剤,EGF,TGFβ阻害剤,ヒストン脱アセチル化酵素阻害剤,ROCK阻害剤を用いることにより,細胞性栄養膜細胞は5カ月以上にわたり培養が可能であった.これは,約150回の細胞分裂に相当した.GSK3阻害剤およびEGFは細胞性栄養膜細胞の生存および増殖に必須であり,ROCK阻害剤は細胞性栄養膜細胞の培養プレートへの接着に重要であった.また,TGFβ阻害剤およびヒストン脱アセチル化酵素阻害剤は細胞の増殖を有意に促進した.得られた細胞性栄養膜細胞株は栄養膜細胞の特異的なマーカーであるKRT7に陽性かつHLAクラスI分子に陰性であった.
ヒトの胚盤胞より細胞性栄養膜細胞株に類似した細胞株が樹立されるかどうか検討した.計16個の胚盤胞をさきと同じ培養液を用いて培養したところ,細胞性栄養膜細胞株と非常によく似た8系統の細胞株が樹立された.以下に示すように,細胞性栄養膜細胞株および胚盤胞より樹立した細胞株は絨毛外性栄養膜細胞および合胞体性栄養膜細胞への分化能をもっていたことから,これらの細胞株はヒトの栄養膜幹細胞であると結論づけた.
3.ヒトの栄養膜幹細胞の選択的な分化
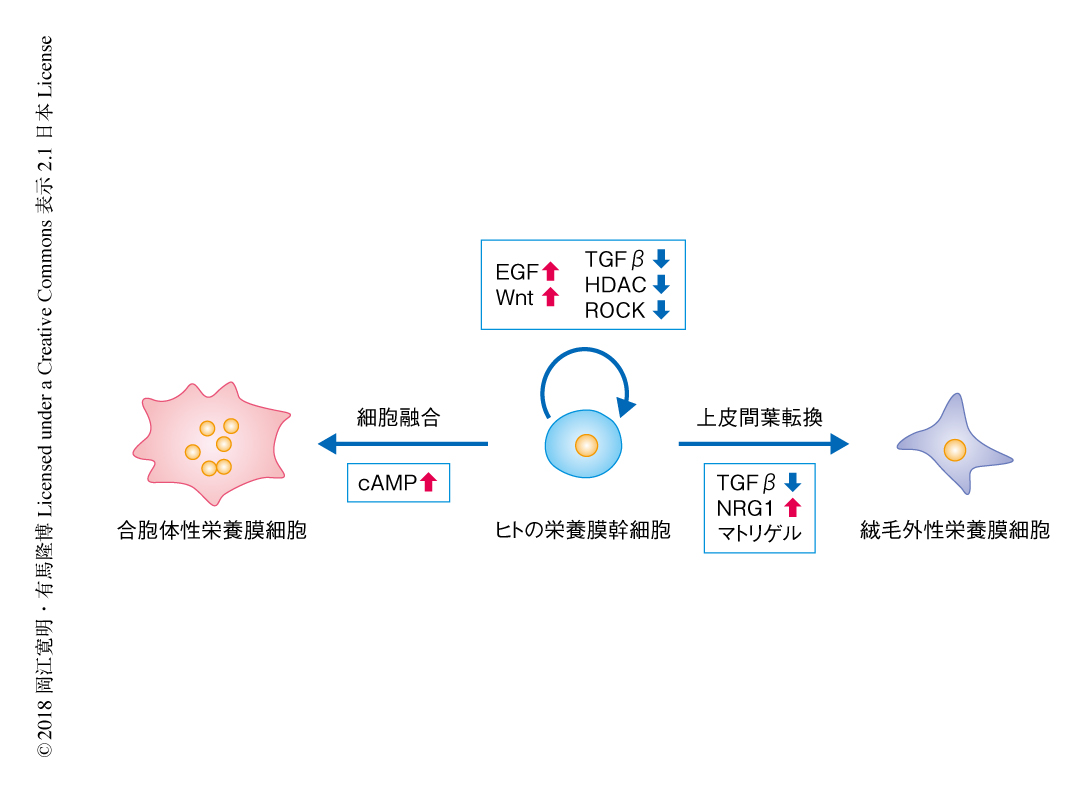
ヒトの絨毛がん細胞株を用いた研究により,合胞体性栄養膜細胞への分化においてcAMPが重要であることが知られていた2).そこで,cAMPの濃度を上昇させるフォルスコリンによりヒトの栄養膜幹細胞を処理したところ,細胞融合が起こり大部分の細胞が多核の合胞体性栄養膜細胞様の細胞へと分化した(図2).この細胞は合胞体性栄養膜細胞の特異的なマーカーであるSDC1に陽性であり,妊娠中に産生されるホルモンのひとつであるヒトの絨毛性ゴナドトロピンを大量に放出していた.さらに,RNA-seq法による解析により,合胞体性栄養膜細胞様の細胞と生体の合胞体性栄養膜細胞とは非常によく似た遺伝子の発現パターンをもつことが明らかにされた.
ヒトの栄養膜幹細胞の培養の条件を検討する過程において,TGFβ阻害剤が細胞性栄養膜細胞から絨毛外性栄養膜細胞への分化を促進することが見い出された.これにくわえ,ヒトの胎盤絨毛の体外培養系を用いた研究により,NRG1およびマトリゲルが絨毛外性栄養膜細胞への分化を促進することが示唆されていた3,4).そこで,TGFβ阻害剤,NRG1,マトリゲルの存在においてヒトの栄養膜幹細胞を培養したところ,上皮間葉転換が起こり紡錘形の絨毛外性栄養膜細胞様の細胞へと分化した(図2).この細胞は絨毛外性栄養膜細胞の特異的なマーカーであるHLA-Gに陽性であり,さらに生体の絨毛外性栄養膜細胞と非常によく似た遺伝子の発現パターンをもっていた.
4.ヒトの栄養膜幹細胞におけるDNAメチル化の解析
ヒトの栄養膜細胞は以下に示すユニークなDNAメチル化のパターンをもつことが知られている.1)通常,体細胞のゲノムはプロモーター領域やエンハンサー領域を除いて高メチル化の状態にあるが,ヒトの栄養膜細胞はゲノムの約40%が中程度のメチル化の状態を示す5).2)胎児および胎児に由来する細胞において高メチル化の状態にあるプロモーター領域の一部が,ヒトの栄養膜細胞においては低メチル化の状態にある.3)ヒトの栄養膜細胞においてのみアレルに特異的なDNAメチル化を示す領域が多く存在する6,7).これらの特徴がヒトの栄養膜幹細胞において維持されているかどうかを調べるため,バイサルファイトシークエンス法により解析した結果,一部に例外はあったものの,これらの特徴はヒトの栄養膜幹細胞においておおむね維持されていた.
5.ヒトの栄養膜幹細胞の免疫不全マウスへの移植
ヒトの栄養膜幹細胞が生体においても機能するかどうか解析するため,免疫不全マウスであるNOD-SCIDマウスの皮下へと移植した.ヒトの栄養膜幹細胞は移植されたマウスの真皮および皮下組織に浸潤し,辺縁部の細胞の一部はHLA-Gに陽性の絨毛外性栄養膜細胞様の細胞やSDC1に陽性の合胞体性栄養膜細胞様の細胞へと分化した.一部の合胞体性栄養膜細胞様の細胞には空胞が生じ血液が流入していた.この構造は,ヒトの胚盤胞が子宮に着床する際につくられる原始合胞体性栄養膜細胞と酷似していた8).さらに,移植されたマウスの血中には多量のヒトの絨毛性ゴナドトロピンが認められた.以上より,免疫不全マウスにヒトの栄養膜幹細胞を移植することにより,着床の現象の一部が再現されることが明らかにされた.
おわりに
この研究においてもっとも苦労したのは,ヒトの栄養膜幹細胞の樹立そのものではなく,樹立した細胞株が栄養膜幹細胞であることをいかに証明するかということであった.マウスの場合,胚盤胞に注入した細胞が胎盤に寄与するかどうかを解析することにより栄養膜幹細胞であることは簡単に証明される.一方,ヒトの胚を用いたキメラの作製は倫理的に許されない.そのため,この研究においては,樹立した細胞株をさまざまな角度から解析することによりヒトの栄養膜幹細胞であることが“ほぼ”証明されたと考えている.ヒトの栄養膜幹細胞がキメラの形成能をもつかどうかという問題は残されたままであるが,今後,異種間のキメラの作製や非ヒト霊長類における栄養膜幹細胞の樹立などにより解決される可能性がある.
文 献
- Tanaka, S., Kunath, T., Hadjantonakis, A. K. et al .: Promotion of trophoblast stem cell proliferation by FGF4. Science, 282, 2072-2075 (1998)[PubMed]
- Strauss, J. F. 3rd, Kido, S., Sayegh, R. et al .: The cAMP signalling system and human trophoblast function. Placenta, 13, 389-403 (1992)[PubMed]
- Miller, R. K., Genbacev, O., Turner, M. A. et al .: Human placental explants in culture: approaches and assessments. Placenta, 26, 439-448 (2005)[PubMed]
- Fock, V., Plessl, K., Draxler, P. et al .: Neuregulin-1-mediated ErbB2-ErbB3 signalling protects human trophoblasts against apoptosis to preserve differentiation. J. Cell Sci., 128, 4306-4316 (2015)[PubMed]
- Schroeder, D. I., Blair, J. D., Lott, P. et al .: The human placenta methylome. Proc. Natl. Acad. Sci. USA, 110, 6037-6042 (2013)[PubMed]
- Court, F., Tayama, C., Romanelli, V. et al .: Genome-wide parent-of-origin DNA methylation analysis reveals the intricacies of human imprinting and suggests a germline methylation-independent mechanism of establishment. Genome Res., 24, 554-569 (2014)[PubMed]
- Hamada, H., Okae, H., Toh, H. et al .: Allele-specific methylome and transcriptome analysis reveals widespread imprinting in the human placenta. Am J. Hum. Genet., 99, 1045-1058 (2016)[PubMed]
- James, J. L., Carter, A. M. & Chamley, L. W .: Human placentation from nidation to 5 weeks of gestation. Part I: What do we know about formative placental development following implantation? Placenta, 33, 327-334 (2012)[PubMed]
活用したデータベースにかかわるキーワードと統合TVへのリンク
著者プロフィール
略歴:2010年 東京大学大学院理学系研究科 修了,同年 東北大学大学院医学系研究科 研究員を経て,2012年より同 助教.
研究テーマ:胎盤とゲノムインプリンティング.
抱負:胎盤の機能は哺乳類のあいだで保存されているものの,その形態や構成する細胞はきわめて多様です.このような多様性がなぜ,どのように生じるのかを理解したいと考えています.
有馬 隆博(Takahiro Arima)
東北大学大学院医学系研究科 教授.
© 2018 岡江寛明・有馬隆博 Licensed under CC 表示 2.1 日本