オルガノイドの形成下におけるヒトのiPS細胞に由来する肺胞幹細胞の長期培養
山本佑樹・後藤慎平
(京都大学大学院医学研究科 呼吸器内科学分野)
email:後藤慎平
DOI: 10.7875/first.author.2017.117
Long-term expansion of alveolar stem cells derived from human iPS cells in organoids.
Yuki Yamamoto, Shimpei Gotoh, Yohei Korogi, Masahide Seki, Satoshi Konishi, Satoshi Ikeo, Naoyuki Sone, Tadao Nagasaki, Hisako Matsumoto, Shigeo Muro, Isao Ito, Toyohiro Hirai, Takashi Kohno, Yutaka Suzuki, Michiaki Mishima
Nature Methods, 14, 1097-1106 (2017)
II型肺胞上皮細胞は組織幹細胞であり,肺胞における恒常性の維持に重要である.しかし,安定して培養することが困難なため,ヒトのII型肺胞上皮細胞を活用した研究には限界があった.この研究において,筆者らは,ヒトのiPS細胞からII型肺胞上皮細胞への分化をオルガノイド形成下において効率的に誘導する方法を確立し,線維芽細胞とともにオルガノイドを形成させて培養することにより継代が可能になった.iPS細胞に由来するII型肺胞上皮細胞は肺サーファクタントやII型肺胞上皮細胞に特徴的なマーカーの発現を維持しつつ,自己複製能およびI型肺胞上皮様の細胞への分化能をもち,肺胞幹細胞としての性質を維持したまま長期間にわたり安定に増殖した.また,iPS細胞に由来するII型肺胞上皮細胞およびその前段階の細胞のトランスクリプトームを1細胞RNAシークエンシング法により解析したところ,分化の過程および細胞集団の不均一性が詳細に示された.これらの解析により,この分化系はヒトにおけるII型肺胞上皮細胞の発生の過程を試験管内において再現するモデルであることが示唆された.長期培養した肺胞のオルガノイドを用いた薬剤毒性試験により,試験管内にてヒトに由来するII型肺胞上皮細胞において特異的な現象が検出された.この研究は,iPS細胞を細胞源としてこれまで困難であったヒトのII型肺胞上皮細胞を活用する研究を可能にし,将来的には,疾患のモデリングや再生医療への応用が期待される.
一般に,組織幹細胞を安定に培養するのはむずかしいとされてきたが,近年,臓器に類似した3次元構造であるオルガノイドの形成下において培養することにより,種々の臓器に特異的な組織幹細胞を長期にわたり維持できるようになり,その制御機構の解明などに貢献している1).肺においてII型肺胞上皮細胞が肺胞の組織幹細胞として知られており,自己複製能および肺胞の90%以上をおおうI型肺胞上皮細胞への分化能をもつとともに,肺サーファクタントを分泌して肺の虚脱をふせぐ.II型肺胞上皮細胞の異常は慢性閉塞性肺疾患,間質性肺炎,肺がんといった難治性の呼吸器疾患に関与することが示唆されている.しかし,ヒトのII型肺胞上皮細胞の入手には成人の肺から初代細胞として単離する必要があり,相当量の肺を外科的に切除した検体が必要になるなど倫理的なハードルも高く,単離できても長期培養が困難で,有力な研究プラットホームが存在しなかった.
このような状況の解決の手段として,ヒトのiPS細胞からII型肺胞上皮細胞の分化を誘導する研究が世界的に進められてきたが2-5),分化の効率が不十分なものが多く,長期培養の報告もなかった.筆者らも,先行研究として,オルガノイドの培養を用いたII型肺胞上皮細胞6) および気道上皮細胞7) への分化法を報告したが,II型肺胞上皮細胞に関しては分化の効率が低く十分な数の細胞が得られなかったため詳細には解析できなかった.
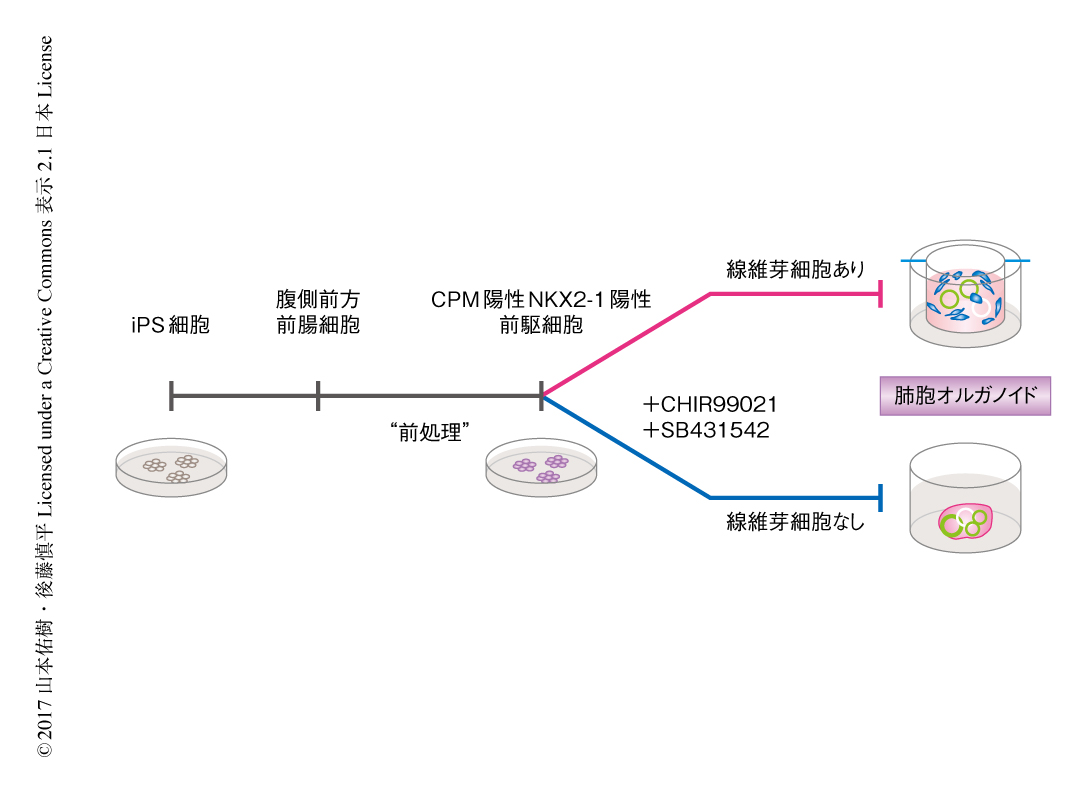
肺はNKX2-1陽性の腹側前方前腸より発生する内胚葉性の臓器であり,筆者らの先行研究において,iPS細胞から内胚葉,前方前腸をへてNKX2-1陽性の腹側前方前腸細胞を分化させ,CPMという表面タンパク質を用いて単離する方法が確立されていた.そこで,NKX2-1陽性の腹側前方前腸細胞をII型肺胞上皮細胞に分化しやすい状態にする“前処理”ができれば分化の効率を改善できるのではないかと考え,種々の培養条件を検討した.その結果,Wntシグナル伝達経路の促進作用をもつCHIR99021にくわえ,FGF10,KGF,そして,Notchシグナル伝達経路を抑制するDAPTを添加した培地にて7日間培養する“前処理”をしたNKX2-1陽性細胞と,ヒトの胎児肺線維芽細胞とを共培養して肺胞のオルガノイドを形成させると,約50%の効率でII型肺胞上皮細胞の特異的なマーカーであるSFTPCに陽性を示す細胞が分化した(図1).形成されたオルガノイドを透過型電子顕微鏡により観察したところ,ラメラ体とよばれる肺サーファクタントを貯留する特徴的なオルガネラの存在が確認された.生細胞イメージング法により,これらのラメラ体が肺サーファクタントの主成分であるホスファチジルコリンを貯留する機能をもつことも示された.また,蛍光免疫染色法およびRT-qPCR法により肺サーファクタントやラメラ体に局在するタンパク質の発現が確認された.オルガノイドから単離したiPS細胞に由来するII型肺胞上皮細胞についてマイクロアレイ法により遺伝子発現を網羅的に解析したところ,II型肺胞上皮細胞において特徴的な発現を示す多数の遺伝子が確認された.
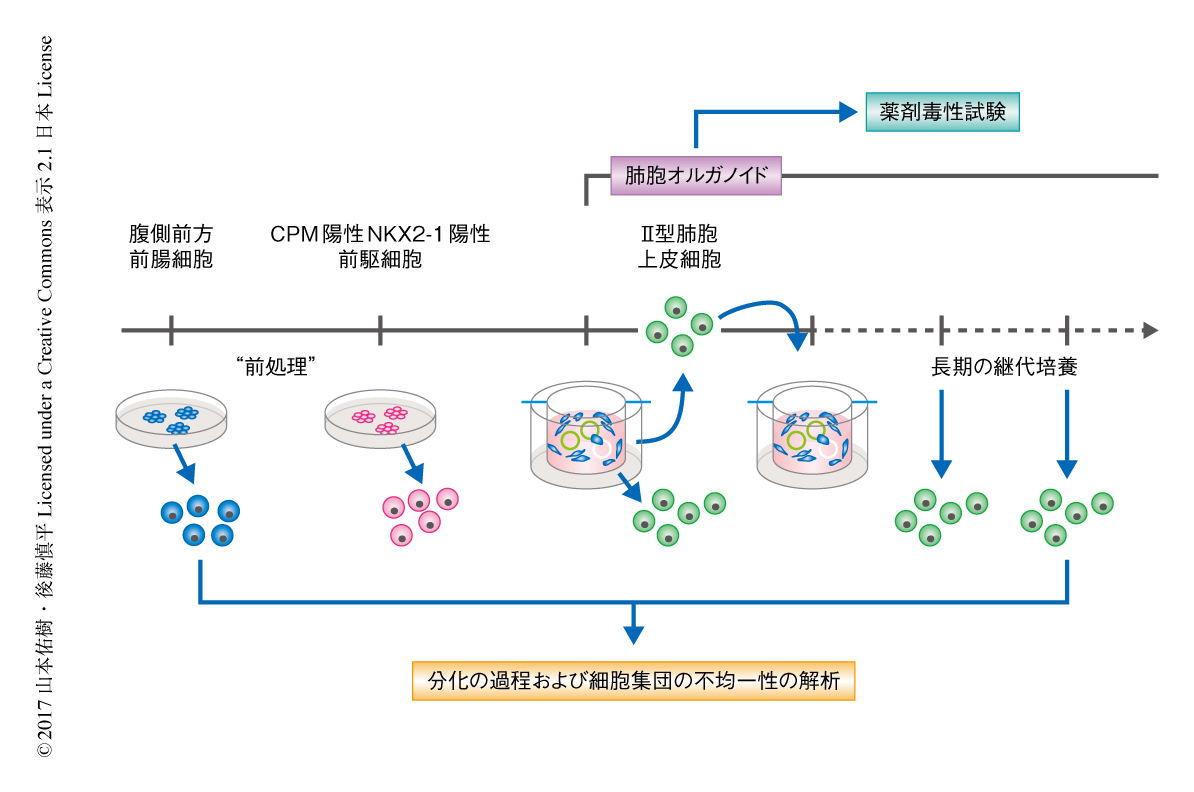
“前処理”をへてII型肺胞上皮細胞が分化する過程における遺伝子発現の変化を1細胞RNAシークエンシング法により解析した(図2).トランスクリプトームの主成分解析の結果,“前処理”によりNKX2-1陽性の腹側前方前腸細胞がよりII型肺胞上皮細胞に近い状態へと移行することが示唆された.また,この過程において発現の変動した遺伝子を解析したところ,II型肺胞上皮細胞への分化が進むとともに転写因子であるETV5およびCEBPDの発現が上昇することが判明した.
II型肺胞上皮細胞の分化法の汎用性を高めるため,胎児の肺線維芽細胞を用いずに肺胞のオルガノイドを形成する方法について検討した.“前処理”をしたNKX2-1陽性細胞を非接着性のウェルプレートにおいて集塊状にしたのち3次元基質に包埋し,CHIR99021およびTGFβシグナル伝達経路の阻害薬であるSB431542を添加した培地にて培養することにより,約20%の効率でII型肺胞上皮細胞が分化した(図1).CHIR99021あるいはSB431542のいずれかを欠いた培地で培養しても分化の効率は大幅に低下した.このことから,II型肺胞上皮細胞の分化においてはWntシグナル伝達経路の活性化とTGFβシグナル伝達経路の抑制の相乗効果が重要と考えられた.また,iPS細胞から線維芽細胞を用いてあるいは用いずに分化させたII型肺胞上皮細胞,および,成人の肺から単離されたII型肺胞上皮細胞のトランスクリプトームを1分子RNAシークエンシング法により比較したところ,iPS細胞に由来するII型肺胞上皮細胞は成人の肺のII型肺胞上皮細胞と比較的近い遺伝子の発現パターンをもつことがわかった.
iPS細胞に由来するII型肺胞上皮細胞の長期培養法の開発を試みた.オルガノイドからiPS細胞に由来するII型肺胞上皮細胞を単離し,それを再度,ヒトの胎児肺線維芽細胞とオルガノイドを形成させ継代するという操作をくり返したところ,SFTPC陽性細胞は3カ月間をこえて増殖しつづけた.継代をつづけたオルガノイドは50%をこえる効率でSFTPC陽性細胞を維持しており,ラメラ体はより成熟した形態を呈していた.オルガノイドにおいてはSFTPC陰性AQP5陽性PDPN陽性のI型肺胞上皮様細胞への分化も確認された.SFTPC陽性細胞の核型解析においては明らかな染色体の異常は認められず,非腫瘍性の増殖が示唆された.iPS細胞に由来するII型肺胞上皮細胞の初代,2回継代,5回継代ののちのトランスクリプトームについて,前段階のCPM陽性細胞,iPS細胞に由来する気道上皮細胞,成人の肺のII型肺胞上皮細胞と主成分解析法,クラスター解析法,相関解析法により比較したところ,SFTPC陽性細胞は継代をつづけても成人の肺のII型肺胞上皮細胞に比較的近い遺伝子の発現パターンを維持することがわかった.
ここまで,iPS細胞に由来するII型肺胞上皮細胞の単離および継代にはSFTPCのGFPレポーターとしての機能をもつiPS細胞株を用いていたが,汎用性の高い継代法の開発が必要と考えた.II型肺胞上皮細胞に特異的なラメラ体はリソソームに関連するオルガネラであり,LysoTrackerにより標識されるという性質に注目した.LysoTracker強陽性細胞を単離して同様にオルガノイドの形成をくり返したところ,複数の細胞株において同様にiPS細胞に由来するII型肺胞上皮細胞を継代することができた.これらの結果から,iPS細胞に由来するII型肺胞上皮細胞はオルガノイド形成下において自己複製能およびI型肺胞上皮細胞への分化能をもつ肺胞幹細胞として長期培養が可能であることが明らかにされた.
近年のマウスにおける肺の発生学的な研究から,I型肺胞上皮細胞およびII型肺胞上皮細胞は双方のマーカーを共発現する両能性の細胞から分化することがわかってきた8,9).iPS細胞に由来するII型肺胞上皮細胞にはI型肺胞上皮細胞のマーカーであるPDPNに対しても陽性の細胞が存在し,透過型電子顕微鏡により胎生期のII型肺胞上皮細胞に形態の近い幼弱な細胞から成熟したラメラ体をもつ細胞までが観察されることから,両能性の細胞を含む不均一な細胞集団であると考えた.1細胞RNAシークエンシング法により,iPS細胞に由来するII型肺胞上皮細胞はI型肺胞上皮細胞のマーカーの共発現の程度により大きく3つの細胞集団に分けられた.トランスクリプトームの主成分解析においてiPS細胞に由来するII型肺胞上皮細胞は2方向性の分布をとり,ローディングプロットにおけるI型肺胞上皮細胞のマーカーの分布はI型肺胞上皮細胞のマーカーを高発現する細胞集団の分布と一致した.おのおのの細胞集団を比較することにより特徴的な遺伝子を抽出しクラスター解析したところ,異なる遺伝子オントロジーに関連づけられる3つの遺伝子セットが見い出され,I型肺胞上皮細胞のマーカーの多くが含まれた.また,同じ遺伝子セットを用いてマウスの肺胞発生期における1細胞RNAシークエンシング法のデータを解析し対比したところ,iPS細胞に由来するII型肺胞上皮細胞は両能性の細胞を多く含み,ヒトにおいて肺胞上皮細胞の発生する過程を知るためのよいモデルになることが示唆された.
種々の薬剤が有害事象として肺に障害の起こることが知られている.iPS細胞に由来するII型肺胞上皮細胞を含む肺胞のオルガノイドをヒトの細胞における試験管内での薬剤毒性試験に応用できるのではないかと考え,とくに,II型肺胞上皮細胞に異常をきたすことの知られているアミオダロンおよびGNE7915の2種類の薬剤に対する肺胞のオルガノイドの応答について調べた.アミオダロンは汎用される抗不整脈薬であるが,ときに薬剤性の肺障害をきたすことが知られている.GNE7915はLRRK2というキナーゼの阻害薬であり,家族性パーキンソン病の治療薬の候補ともなっているが,サルへの投与において肺線維症はきたさないもののII型肺胞上皮細胞のラメラ体が腫大するという報告がある10).2~3回の継代をへた肺胞のオルガノイドに10日間にわたりアミオダロンあるいはGNE7915を曝露し透過型電子顕微鏡により観察したところ,生体において報告されていたのと同様にラメラ体の増加および腫大が観察され,肺胞のオルガノイドのラメラ体をLysoTrackerにより標識して生細胞イメージングしたところ,細胞内にLysoTracker強陽性のオルガネラが充満するようすが観察された.ラメラ体の変化を定量的に評価するため,LysoTrackerにより標識した肺胞のオルガノイドをバラバラにし構成する細胞をフローサイトメトリーにより解析したところ,アミオダロンあるいはGNE7915の曝露によりiPS細胞に由来するII型肺胞上皮細胞においてLysoTrackerの蛍光強度は有意に上昇した.また,肺胞のオルガノイドからiPS細胞に由来するII型肺胞上皮細胞を回収しトランスクリプトームを比較したところ,アミオダロンおよびGNE7915の曝露により発現が共通に変化する遺伝子と,それぞれの曝露により発現が特徴的に変化する遺伝子が同定された.とくに,アミオダロンの投与により発現の変化する遺伝子として,創傷の治癒,サイトカインの分泌,インターロイキン6の産生に関連する遺伝子が多く含まれており,生体において薬剤性の肺障害が起こることと関連する可能性が示唆された.
この研究において,筆者らは,ヒトのiPS細胞からII型肺胞上皮細胞の分化を効率的に誘導する方法を確立した.また,iPS細胞に由来するII型肺胞上皮細胞をオルガノイドの形成下において長期培養することにより,組織幹細胞としての性質を維持したまま増殖が可能であることも示された.さらに,1細胞RNAシークエンシング法により分化の過程および分化したII型肺胞上皮細胞を解析することにより,この分化系はヒトのII型肺胞上皮細胞の発生の過程を近似したモデルである可能性が示唆された.ヒトのiPS細胞に由来するII型肺胞上皮細胞は,成人の肺に由来するII型肺胞上皮細胞と免疫系に関連した機能などにおいて差異はあるものの,肺の薬剤毒性試験への応用は可能と考えられた.今後,これらの方法を用いて,疾患モデリングをつうじた創薬や再生医療への応用を発展させていきたい.
略歴:京都大学医学部附属病院 医員.
研究テーマ:ヒトのiPS細胞を用いた肺の再生.
関心事:進化および比較生物学.
後藤 慎平(Shimpei Gotoh)
京都大学大学院医学研究科 特定准教授.
© 2017 山本佑樹・後藤慎平 Licensed under CC 表示 2.1 日本
(京都大学大学院医学研究科 呼吸器内科学分野)
email:後藤慎平
DOI: 10.7875/first.author.2017.117
Long-term expansion of alveolar stem cells derived from human iPS cells in organoids.
Yuki Yamamoto, Shimpei Gotoh, Yohei Korogi, Masahide Seki, Satoshi Konishi, Satoshi Ikeo, Naoyuki Sone, Tadao Nagasaki, Hisako Matsumoto, Shigeo Muro, Isao Ito, Toyohiro Hirai, Takashi Kohno, Yutaka Suzuki, Michiaki Mishima
Nature Methods, 14, 1097-1106 (2017)
要 約
II型肺胞上皮細胞は組織幹細胞であり,肺胞における恒常性の維持に重要である.しかし,安定して培養することが困難なため,ヒトのII型肺胞上皮細胞を活用した研究には限界があった.この研究において,筆者らは,ヒトのiPS細胞からII型肺胞上皮細胞への分化をオルガノイド形成下において効率的に誘導する方法を確立し,線維芽細胞とともにオルガノイドを形成させて培養することにより継代が可能になった.iPS細胞に由来するII型肺胞上皮細胞は肺サーファクタントやII型肺胞上皮細胞に特徴的なマーカーの発現を維持しつつ,自己複製能およびI型肺胞上皮様の細胞への分化能をもち,肺胞幹細胞としての性質を維持したまま長期間にわたり安定に増殖した.また,iPS細胞に由来するII型肺胞上皮細胞およびその前段階の細胞のトランスクリプトームを1細胞RNAシークエンシング法により解析したところ,分化の過程および細胞集団の不均一性が詳細に示された.これらの解析により,この分化系はヒトにおけるII型肺胞上皮細胞の発生の過程を試験管内において再現するモデルであることが示唆された.長期培養した肺胞のオルガノイドを用いた薬剤毒性試験により,試験管内にてヒトに由来するII型肺胞上皮細胞において特異的な現象が検出された.この研究は,iPS細胞を細胞源としてこれまで困難であったヒトのII型肺胞上皮細胞を活用する研究を可能にし,将来的には,疾患のモデリングや再生医療への応用が期待される.
はじめに
一般に,組織幹細胞を安定に培養するのはむずかしいとされてきたが,近年,臓器に類似した3次元構造であるオルガノイドの形成下において培養することにより,種々の臓器に特異的な組織幹細胞を長期にわたり維持できるようになり,その制御機構の解明などに貢献している1).肺においてII型肺胞上皮細胞が肺胞の組織幹細胞として知られており,自己複製能および肺胞の90%以上をおおうI型肺胞上皮細胞への分化能をもつとともに,肺サーファクタントを分泌して肺の虚脱をふせぐ.II型肺胞上皮細胞の異常は慢性閉塞性肺疾患,間質性肺炎,肺がんといった難治性の呼吸器疾患に関与することが示唆されている.しかし,ヒトのII型肺胞上皮細胞の入手には成人の肺から初代細胞として単離する必要があり,相当量の肺を外科的に切除した検体が必要になるなど倫理的なハードルも高く,単離できても長期培養が困難で,有力な研究プラットホームが存在しなかった.
このような状況の解決の手段として,ヒトのiPS細胞からII型肺胞上皮細胞の分化を誘導する研究が世界的に進められてきたが2-5),分化の効率が不十分なものが多く,長期培養の報告もなかった.筆者らも,先行研究として,オルガノイドの培養を用いたII型肺胞上皮細胞6) および気道上皮細胞7) への分化法を報告したが,II型肺胞上皮細胞に関しては分化の効率が低く十分な数の細胞が得られなかったため詳細には解析できなかった.
1.肺胞のオルガノイドの形成下におけるiPS細胞からII型肺胞上皮細胞への効率のよい分化
肺はNKX2-1陽性の腹側前方前腸より発生する内胚葉性の臓器であり,筆者らの先行研究において,iPS細胞から内胚葉,前方前腸をへてNKX2-1陽性の腹側前方前腸細胞を分化させ,CPMという表面タンパク質を用いて単離する方法が確立されていた.そこで,NKX2-1陽性の腹側前方前腸細胞をII型肺胞上皮細胞に分化しやすい状態にする“前処理”ができれば分化の効率を改善できるのではないかと考え,種々の培養条件を検討した.その結果,Wntシグナル伝達経路の促進作用をもつCHIR99021にくわえ,FGF10,KGF,そして,Notchシグナル伝達経路を抑制するDAPTを添加した培地にて7日間培養する“前処理”をしたNKX2-1陽性細胞と,ヒトの胎児肺線維芽細胞とを共培養して肺胞のオルガノイドを形成させると,約50%の効率でII型肺胞上皮細胞の特異的なマーカーであるSFTPCに陽性を示す細胞が分化した(図1).形成されたオルガノイドを透過型電子顕微鏡により観察したところ,ラメラ体とよばれる肺サーファクタントを貯留する特徴的なオルガネラの存在が確認された.生細胞イメージング法により,これらのラメラ体が肺サーファクタントの主成分であるホスファチジルコリンを貯留する機能をもつことも示された.また,蛍光免疫染色法およびRT-qPCR法により肺サーファクタントやラメラ体に局在するタンパク質の発現が確認された.オルガノイドから単離したiPS細胞に由来するII型肺胞上皮細胞についてマイクロアレイ法により遺伝子発現を網羅的に解析したところ,II型肺胞上皮細胞において特徴的な発現を示す多数の遺伝子が確認された.
“前処理”をへてII型肺胞上皮細胞が分化する過程における遺伝子発現の変化を1細胞RNAシークエンシング法により解析した(図2).トランスクリプトームの主成分解析の結果,“前処理”によりNKX2-1陽性の腹側前方前腸細胞がよりII型肺胞上皮細胞に近い状態へと移行することが示唆された.また,この過程において発現の変動した遺伝子を解析したところ,II型肺胞上皮細胞への分化が進むとともに転写因子であるETV5およびCEBPDの発現が上昇することが判明した.
II型肺胞上皮細胞の分化法の汎用性を高めるため,胎児の肺線維芽細胞を用いずに肺胞のオルガノイドを形成する方法について検討した.“前処理”をしたNKX2-1陽性細胞を非接着性のウェルプレートにおいて集塊状にしたのち3次元基質に包埋し,CHIR99021およびTGFβシグナル伝達経路の阻害薬であるSB431542を添加した培地にて培養することにより,約20%の効率でII型肺胞上皮細胞が分化した(図1).CHIR99021あるいはSB431542のいずれかを欠いた培地で培養しても分化の効率は大幅に低下した.このことから,II型肺胞上皮細胞の分化においてはWntシグナル伝達経路の活性化とTGFβシグナル伝達経路の抑制の相乗効果が重要と考えられた.また,iPS細胞から線維芽細胞を用いてあるいは用いずに分化させたII型肺胞上皮細胞,および,成人の肺から単離されたII型肺胞上皮細胞のトランスクリプトームを1分子RNAシークエンシング法により比較したところ,iPS細胞に由来するII型肺胞上皮細胞は成人の肺のII型肺胞上皮細胞と比較的近い遺伝子の発現パターンをもつことがわかった.
2.iPS細胞に由来するII型肺胞上皮細胞のオルガノイド形成下における長期培養
iPS細胞に由来するII型肺胞上皮細胞の長期培養法の開発を試みた.オルガノイドからiPS細胞に由来するII型肺胞上皮細胞を単離し,それを再度,ヒトの胎児肺線維芽細胞とオルガノイドを形成させ継代するという操作をくり返したところ,SFTPC陽性細胞は3カ月間をこえて増殖しつづけた.継代をつづけたオルガノイドは50%をこえる効率でSFTPC陽性細胞を維持しており,ラメラ体はより成熟した形態を呈していた.オルガノイドにおいてはSFTPC陰性AQP5陽性PDPN陽性のI型肺胞上皮様細胞への分化も確認された.SFTPC陽性細胞の核型解析においては明らかな染色体の異常は認められず,非腫瘍性の増殖が示唆された.iPS細胞に由来するII型肺胞上皮細胞の初代,2回継代,5回継代ののちのトランスクリプトームについて,前段階のCPM陽性細胞,iPS細胞に由来する気道上皮細胞,成人の肺のII型肺胞上皮細胞と主成分解析法,クラスター解析法,相関解析法により比較したところ,SFTPC陽性細胞は継代をつづけても成人の肺のII型肺胞上皮細胞に比較的近い遺伝子の発現パターンを維持することがわかった.
ここまで,iPS細胞に由来するII型肺胞上皮細胞の単離および継代にはSFTPCのGFPレポーターとしての機能をもつiPS細胞株を用いていたが,汎用性の高い継代法の開発が必要と考えた.II型肺胞上皮細胞に特異的なラメラ体はリソソームに関連するオルガネラであり,LysoTrackerにより標識されるという性質に注目した.LysoTracker強陽性細胞を単離して同様にオルガノイドの形成をくり返したところ,複数の細胞株において同様にiPS細胞に由来するII型肺胞上皮細胞を継代することができた.これらの結果から,iPS細胞に由来するII型肺胞上皮細胞はオルガノイド形成下において自己複製能およびI型肺胞上皮細胞への分化能をもつ肺胞幹細胞として長期培養が可能であることが明らかにされた.
3.iPS細胞に由来するII型肺胞上皮細胞は細胞ごとに不均一な遺伝子の発現パターンをとる
近年のマウスにおける肺の発生学的な研究から,I型肺胞上皮細胞およびII型肺胞上皮細胞は双方のマーカーを共発現する両能性の細胞から分化することがわかってきた8,9).iPS細胞に由来するII型肺胞上皮細胞にはI型肺胞上皮細胞のマーカーであるPDPNに対しても陽性の細胞が存在し,透過型電子顕微鏡により胎生期のII型肺胞上皮細胞に形態の近い幼弱な細胞から成熟したラメラ体をもつ細胞までが観察されることから,両能性の細胞を含む不均一な細胞集団であると考えた.1細胞RNAシークエンシング法により,iPS細胞に由来するII型肺胞上皮細胞はI型肺胞上皮細胞のマーカーの共発現の程度により大きく3つの細胞集団に分けられた.トランスクリプトームの主成分解析においてiPS細胞に由来するII型肺胞上皮細胞は2方向性の分布をとり,ローディングプロットにおけるI型肺胞上皮細胞のマーカーの分布はI型肺胞上皮細胞のマーカーを高発現する細胞集団の分布と一致した.おのおのの細胞集団を比較することにより特徴的な遺伝子を抽出しクラスター解析したところ,異なる遺伝子オントロジーに関連づけられる3つの遺伝子セットが見い出され,I型肺胞上皮細胞のマーカーの多くが含まれた.また,同じ遺伝子セットを用いてマウスの肺胞発生期における1細胞RNAシークエンシング法のデータを解析し対比したところ,iPS細胞に由来するII型肺胞上皮細胞は両能性の細胞を多く含み,ヒトにおいて肺胞上皮細胞の発生する過程を知るためのよいモデルになることが示唆された.
4.肺胞のオルガノイドに対する薬剤毒性試験
種々の薬剤が有害事象として肺に障害の起こることが知られている.iPS細胞に由来するII型肺胞上皮細胞を含む肺胞のオルガノイドをヒトの細胞における試験管内での薬剤毒性試験に応用できるのではないかと考え,とくに,II型肺胞上皮細胞に異常をきたすことの知られているアミオダロンおよびGNE7915の2種類の薬剤に対する肺胞のオルガノイドの応答について調べた.アミオダロンは汎用される抗不整脈薬であるが,ときに薬剤性の肺障害をきたすことが知られている.GNE7915はLRRK2というキナーゼの阻害薬であり,家族性パーキンソン病の治療薬の候補ともなっているが,サルへの投与において肺線維症はきたさないもののII型肺胞上皮細胞のラメラ体が腫大するという報告がある10).2~3回の継代をへた肺胞のオルガノイドに10日間にわたりアミオダロンあるいはGNE7915を曝露し透過型電子顕微鏡により観察したところ,生体において報告されていたのと同様にラメラ体の増加および腫大が観察され,肺胞のオルガノイドのラメラ体をLysoTrackerにより標識して生細胞イメージングしたところ,細胞内にLysoTracker強陽性のオルガネラが充満するようすが観察された.ラメラ体の変化を定量的に評価するため,LysoTrackerにより標識した肺胞のオルガノイドをバラバラにし構成する細胞をフローサイトメトリーにより解析したところ,アミオダロンあるいはGNE7915の曝露によりiPS細胞に由来するII型肺胞上皮細胞においてLysoTrackerの蛍光強度は有意に上昇した.また,肺胞のオルガノイドからiPS細胞に由来するII型肺胞上皮細胞を回収しトランスクリプトームを比較したところ,アミオダロンおよびGNE7915の曝露により発現が共通に変化する遺伝子と,それぞれの曝露により発現が特徴的に変化する遺伝子が同定された.とくに,アミオダロンの投与により発現の変化する遺伝子として,創傷の治癒,サイトカインの分泌,インターロイキン6の産生に関連する遺伝子が多く含まれており,生体において薬剤性の肺障害が起こることと関連する可能性が示唆された.
おわりに
この研究において,筆者らは,ヒトのiPS細胞からII型肺胞上皮細胞の分化を効率的に誘導する方法を確立した.また,iPS細胞に由来するII型肺胞上皮細胞をオルガノイドの形成下において長期培養することにより,組織幹細胞としての性質を維持したまま増殖が可能であることも示された.さらに,1細胞RNAシークエンシング法により分化の過程および分化したII型肺胞上皮細胞を解析することにより,この分化系はヒトのII型肺胞上皮細胞の発生の過程を近似したモデルである可能性が示唆された.ヒトのiPS細胞に由来するII型肺胞上皮細胞は,成人の肺に由来するII型肺胞上皮細胞と免疫系に関連した機能などにおいて差異はあるものの,肺の薬剤毒性試験への応用は可能と考えられた.今後,これらの方法を用いて,疾患モデリングをつうじた創薬や再生医療への応用を発展させていきたい.
文 献
- Clevers, H.: Modeling development and disease with organoids. Cell, 165, 1586-1597 (2016)[PubMed]
- Green, M. D., Chen, A., Nostro, M. C. et al.: Generation of anterior foregut endoderm from human embryonic and induced pluripotent stem cells. Nat. Biotechnol., 29, 267-272 (2011)[PubMed]
- Longmire, T. A., Ikonomou, L., Hawkins, F. et al.: Efficient derivation of purified lung and thyroid progenitors from embryonic stem cells. Cell. Stem Cell, 10, 398-411 (2012)[PubMed]
- Huang, S. X., Islam, M. N., O'Neill, J. et al.: Efficient generation of lung and airway epithelial cells from human pluripotent stem cells. Nat. Biotechnol., 32, 84-91 (2014)[PubMed]
- McCauley, K.B., Hawkins, F., Serra, M. et al.: Efficient derivation of functional human airway epithelium from pluripotent stem cells via temporal regulation of Wnt signaling. Cell Stem Cell, 20, 844-857 (2017)[PubMed]
- Gotoh, S., Ito, I., Nagasaki, T. et al.: Generation of alveolar epithelial spheroids via isolated progenitor cells from human pluripotent stem cells. Stem Cell Reports, 3, 394-403 (2014)[PubMed]
- Konishi, S., Gotoh, S., Tateishi, K. et al.: Directed induction of functional multi-ciliated cells in proximal airway epithelial spheroids from human pluripotent stem cells. Stem Cell Reports, 6, 18-25 (2016)[PubMed]
- Desai, T. J., Brownfield, D. G. & Krasnow, M. A.: Alveolar progenitor and stem cells in lung development, renewal and cancer. Nature, 507, 190-194 (2014)[PubMed]
- Treutlein, B., Brownfield, D. G., Wu, A. R. et al.: Reconstructing lineage hierarchies of the distal lung epithelium using single-cell RNA-seq. Nature, 509, 371-375 (2014)[PubMed]
- Fuji, R. N., Flagella, M., Baca, M. et al.: Effect of selective LRRK2 kinase inhibition on nonhuman primate lung. Sci. Transl. Med., 7, 273ra15 (2015)[PubMed]
活用したデータベースにかかわるキーワードと統合TVへのリンク
著者プロフィール
略歴:京都大学医学部附属病院 医員.
研究テーマ:ヒトのiPS細胞を用いた肺の再生.
関心事:進化および比較生物学.
後藤 慎平(Shimpei Gotoh)
京都大学大学院医学研究科 特定准教授.
© 2017 山本佑樹・後藤慎平 Licensed under CC 表示 2.1 日本