ヒトのiPS細胞から作製された腎臓のオルガノイドは腎臓のすべての組織をもちヒトの腎臓の発生を模倣する
高里 実
(オーストラリアMurdoch Childrens Research Institute)
email:高里 実
DOI: 10.7875/first.author.2015.114
Kidney organoids from human iPS cells contain multiple lineages and model human nephrogenesis.
Minoru Takasato, Pei X. Er, Han S. Chiu, Barbara Maier, Gregory J. Baillie, Charles Ferguson, Robert G. Parton, Ernst J. Wolvetang, Matthias S. Roost, Susana M. Chuva de Sousa Lopes, Melissa H. Little
Nature, 526, 564-568 (2015)
ヒトの腎臓は最大で約200万個のネフロンから構成され,血液のろ過,電解質やpHの調節,体内の水分量のバランスを担う重要な器官である.腎臓の発生は2種類の前駆細胞である尿管芽と後腎間葉の相互作用により進行する.尿管芽はおもに集合管,後腎間葉はそれ以外の部分のネフロンへと分化するが,両者とも中間中胚葉に由来する細胞である.近年,種々の報告により,尿管芽はとくに前方中間中胚葉,後腎間葉は後方中間中胚葉に由来することが認識されつつある.筆者らは,この研究において,個体の発生における中間中胚葉の前後軸の形成の機序をモデルとして,尿管芽および後腎間葉をヒトのiPS細胞から任意の割合で分化させることに成功した.この手法を用いて作製された腎臓のオルガノイドはすべての構成要素を含むネフロンをもち,血管系や腎臓間質も同時に発生していた.次世代シークエンサーを用いた解析により,腎臓のオルガノイドとヒトの胎生期における各種の臓器とで転写産物のプロファイルを比較したところ,腎臓のオルガノイドは妊娠3カ月目の胎児の腎臓と近似していた.腎臓のオルガノイドの内部に発生した近位尿細管はエンドサイトーシスによるタンパク質の再吸収が可能で,尿細管としての機能をもっていた.さらに,腎臓のオルガノイドに腎臓に対する毒性をもつシスプラチンを処理したところ,近位尿細管に特異的な細胞死が確認された.この研究においてヒトのiPS細胞から作製された腎臓のオルガノイドは,腎臓のすべての組織をもちあわせていたうえ,in vitroにおいてヒトの腎臓の発生を模倣する系であり,将来的には,腎臓に対する毒性の試験,腎臓の病態モデルの確立,細胞療法などへの応用が期待される.
腎臓は中胚葉系の器官であり,その由来は原始線条にさかのぼる.原始線条は脊椎動物の発生の初期,原腸陥入期にエピブラストの片側に出現する線状の構造体で,前部原始線状は内胚葉への分化能をもち,後部原始線状は沿軸中胚葉,中間中胚葉,側板中胚葉のいずれかの体幹中胚葉に分化する.腎臓のもとになる中間中胚葉はウォルフ管と腎間葉へと分化し,それぞれ,尿管芽と後腎間葉の2種類の前駆細胞へと分化するとされている.しかし近年,マウスの胚の詳細な解析により,ウォルフ管と腎間葉は中間中胚葉において前後に離れて発生することが認識されはじめた1,2).これによると,ウォルフ管は胚の前方の中間中胚葉から発生し,そののち後方へと伸長する.一方,腎間葉は後方中間中胚葉から発生し,前方から伸長してきたウォルフ管と隣接し尿管芽の侵入をうける.腎臓の発生はこの尿管芽と後腎間葉の接触により開始される.以前に筆者らは,尿管芽および後腎間葉をヒトのES細胞から同時に分化させる手法について報告したが3),本来は由来の異なる2種類の前駆細胞をなぜ同時に分化させることができるのかについて疑問が残っていた.その謎を解くには,体幹中胚葉においてどのように前後軸が形成されるのかについて理解する必要があった.
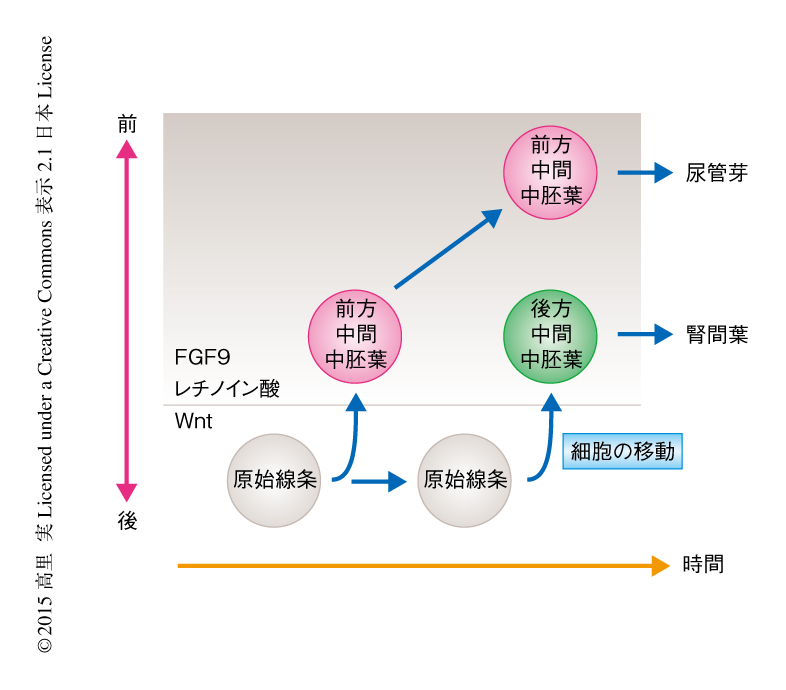
ニワトリの胚の観察によると,成長にともない胚が前後に伸長していく際には,胚の尾部(後方)に位置する原始線状から細胞がつぎつぎと分裂し,胚の体幹(前方)へと送り出される4).これは,さきに体幹へと送り出された細胞が体幹中胚葉の前方に位置し,のちに送り出された細胞は後方に位置することを意味する.では,移動を開始する時期により細胞の運命が左右されるのはどのような機序によるものであろうか.胚の前後軸の形成を支配するモルフォゲンとして,胚の前方において産生されるレチノイン酸,中間中胚葉への分化を誘導するFGF9,胚の尾部において発現するWNTが知られている.ここから筆者らは,原始線状から最初に前方へと移動した細胞は早期にレチノイン酸やFGF9に暴露されるがゆえに前方中間中胚葉へと分化する一方,遅れて移動した細胞はより長いあいだWNTシグナルに影響されるがゆえに後方中間中胚葉へと分化するという,中間中胚葉の前後軸の形成のモデルを仮定した5)(図1).そして,この仮説がヒトの多能性幹細胞から中胚葉への分化においても適用されるのかiPS細胞を用いて検証した.
筆者らは,さきの報告において,ヒトの多能性幹細胞をWNTシグナル刺激物質により数日間にわたり処理することで後部原始線条へと分化させ,そののち,FGF9の処理により中間中胚葉へと分化させた3).この手法は,胚における尾部の古典的WNTシグナルおよび体幹のFGF9シグナルを模倣した系である.そこで,この分化誘導系を使い,最初のWNTシグナル刺激物質による処理の期間を変化させる,つまり,細胞へFGF9の曝露が開始される時期を前後させることにより,前方中間中胚葉と後方中間中胚葉を選択的に分化させることができるかどうか検証した.実験では,ヒトのiPS細胞を4通りの処理期間にわたり培養したのち,FGF9の添加により中間中胚葉を分化させその違いを調べた.すると,短期間の処理からは前方中間中胚葉が分化し,逆に,長期間の処理からは後方中間中胚葉が分化した.これらの中間中胚葉を2次元培養しつづけると,前方中間中胚葉からは尿管芽細胞が発生し,後方中間中胚葉からは後腎間葉が発生した.一方,中期間の処理からは両方の中間中胚葉が同時に分化した.また,レチノイン酸が中間中胚葉の発生にあたえる影響について検証するため,FGF9の処理と同時にレチノイン酸あるいはレチノイン酸阻害剤を添加したところ,レチノイン酸は前方中間中胚葉の分化を促進した一方,レチノイン酸阻害剤はそれを阻害し,逆に,後方中間中胚葉の分化を促進した.以上より,原始線条細胞が体幹の方向へと移動する時間差が前方中間中胚葉および後方中間中胚葉の細胞運命を決定するというモデルは,ヒトのiPS細胞の分化誘導系にも適用されることが確認された.
この結果をふまえ,尿管芽と後腎間葉とを同時に分化させることのできるWNTシグナル刺激物質による4日間の処理の系を用いて腎臓のオルガノイドの作製を試みた.分化の開始から7日後(3日間のFGF9の処理)に細胞を培養皿より分離し,遠心分離により試験管内において再集合体を形成させたのち,メンブレンフィルターのうえで最長で20日間にわたり3次元培養をした.再集合体は時間の経過とともに成長し,3日目には豆状の腎包の形成がみられ,11日目には複雑なネフロンを自発的に構築する直径3~5 mm程度のオルガノイドが形成された.オルガノイドの内部には糸球体,近位尿細管,遠位尿細管,集合管の4つの構成要素をもつネフロンが特徴的な方向性をもち発生していた(図2).実際の腎臓の内部では皮質に糸球体,髄質に集合管が配置されているが,腎臓のオルガノイドでも同様に,底面に枝分かれした集合管が形成され,それが上方の遠位尿細管および近位尿細管へと伸びていき,最上面において糸球体へと終着していた.マウスの後腎間葉細胞を高濃度の古典的WNTシグナルにより刺激するとin vitroにおいてもネフロンへと分化することが知られているが6),オルガノイドにおいても初期における高濃度のWNTシグナル刺激物質による短時間の刺激により最大数のネフロンが形成された.作製された腎臓オルガノイドにおける遺伝子発現プロファイルを調べるため,次世代シークエンサーを用いたRNA-seq法により時系列にトランスクリプトームを解析した.その結果,オルガノイドの形成の過程において,まず腎臓前駆細胞のマーカー遺伝子が失われ,つづいて糸球体や尿細管などネフロンの構成要素のマーカー遺伝子の発現が上昇していた.また,ヒトの胎児の各種の臓器から得られた21のトランスクリプトームのデータセットと比較したところ7),ヒトのiPS細胞から作製された腎臓オルガノイドは妊娠3カ月目の胎児の腎臓にもっとも近似していることがわかった.
生体の腎臓においてはネフロンをとりかこむ腎臓間質には血管が発達している.体内の血液を濾過する役割をもつ腎臓にとり,これら血管の発生は非常に重要である.中間中胚葉は後腎間葉になるだけではなく,腎臓間質細胞や血管内皮細胞にも分化することが知られているため8),ヒトのiPS細胞から中間中胚葉を経由して分化した腎臓オルガノイドに血管系が存在していても不思議ではない.実際に,オルガノイドのネフロンのあいだには腎臓間質細胞が充満しており,そのなかで血管内皮細胞が血管網を形成していた.腎臓間質細胞は血管周皮細胞や糸球体のメザンギウム細胞に分化するが9),オルガノイドにおいても血管周皮細胞や糸球体のメザンギウム細胞が確認された.オルガノイドにみられたPDGFRA陽性のメザンギウム細胞はヒトの胎児期の腎臓においてごく初期の糸球体に存在するもので10),オルガノイドの糸球体が発生の初期の段階にあることが示唆された.透過型電子顕微鏡による観察により,それら初期の糸球体においては足細胞が足突起を糸球体の基底膜へと伸ばしているようすが確認されたが,糸球体の内部には血管系が発達していないためスリット膜は観察されなかった.ただし,一部の糸球体においては血管内皮細胞の侵入がみられ,今後,最適化された培養条件においては血管化された糸球体が形成される可能性が示唆された.また,透過型電子顕微鏡での観察によると,オルガノイドの近位尿細管および遠位尿細管はそれぞれに特徴的な管腔の構造,すなわち,近位尿細管の刷子縁および遠位尿細管の比較的平らな内皮と短い微絨毛をもっていた.これらの結果より,ヒトのiPS細胞から分化させた腎臓オルガノイドは,ネフロンのみならず間質や血管系といった腎臓の発生に必要な組織をすべて内包していることがわかった.
ヒトのiPS細胞から作製された腎臓オルガノイドが将来的に腎臓に対する毒性の試験や腎臓の病態モデルに利用できるかどうかは,ネフロンの機能的な成熟度しだいである.これを調べるため,腎臓においてビタミン,ホルモン,アミノ酸の再吸収を担う近位尿細管に焦点をしぼり解析した.近位尿細管における再吸収はおもにCubilinおよびMegalinの2種類の膜タンパク質を介したエンドサイトーシスによる.その発現を調べたところ,オルガノイドの近位尿細管は管腔側の膜においてCubilinを発現していた.また,蛍光標識したデキストランをオルガノイドの培養液に24時間にわたり添加したところ,デキストランは近位尿細管に特異的に取り込まれ,近位尿細管はほかの細胞よりもより活発にエンドサイトーシスを行っていることがわかった.
近位尿細管はその表面に薬物を取り込むさまざまなトランスポーターを発現しているため,薬剤のもつ毒性におかされやすく,とくに,新薬の開発の段階において腎臓に対する毒性を試験できる系の開発は社会的な要請が大きい.抗がん剤であるシスプラチンは腎臓に対し毒性をもつ薬剤のひとつであり,人体に対する長期間あるいは高濃度の使用により副作用として近位尿細管にアポトーシスをひき起こす11).この毒性がオルガノイドの近位尿細管においても再現できるかどうか調べるため,さまざまな濃度のシスプラチンを培養液に添加し,24時間後にアポトーシスの進行の指標である切断型カスパーゼ3の免疫染色を行った.その結果,高濃度のシスプラチンはオルガノイドの内部のあらゆる細胞にアポトーシスをひき起こしたが,低濃度のシスプラチンは近位尿細管のとくに成熟した部分に有意にアポトーシスをひき起こすことがわかった.この結果から,腎臓オルガノイドの近位尿細管は機能的にある程度まで成熟しており,将来的には,腎臓に対する毒性の試験に利用できる可能性が示された.
この研究においては,中間中胚葉の前後軸の形成の分子機構を解き明かすことにより,ヒトのiPS細胞から腎臓が本来もつ構造的な複雑性をもつオルガノイドの作製に成功した.オルガノイドはすべての構成要素からなるネフロン,および,血管系や腎臓間質などの周辺組織も内包し,その遺伝子発現プロファイルはヒトの胎生期の腎臓と類似していた.一方,その成熟度に関してはさらなる改善の余地のあることは明らかであった.胎児期ではなく成人の腎臓であること,糸球体において毛細血管が発達していること,尿を腎臓から排出する出口となる尿管をもつこと,十分な大きさと数のネフロンをもつことなど,少なくともこれらすべての課題が達成されなければ腎臓オルガノイドを移植に利用することはむずかしい.とはいえ,移植のほかにも腎臓オルガノイドの利用価値はある.この研究においては,薬剤の腎臓に対する毒性の試験に利用できる可能性が示されたが,ほかにも,先天的な腎臓疾患をもつ患者の細胞から作製したiPS細胞を使ってその病態を腎臓オルガノイドにおいて再現できれば,疾患の発症機構の解明につなげることができる.あるいは,腎臓オルガノイドの内部の特定の細胞を単離すれば細胞療法に使用できるかもしれない.また,純粋にヒトの腎臓の発生の分子機構を解明するツールとしても利用できるだろう(図2).
略歴:2008年 東京大学大学院理学系研究科博士課程 修了,同年 研究員,2009年 オーストラリアQueensland大学 研究員を経て,2015年よりオーストラリアMurdoch Childrens Research Institute上級研究員.
研究テーマ:ヒトの多能性幹細胞を使った腎臓の分化誘導系の開発.
関心事:基礎研究の成果をいかに医療への応用へとつなげるか,を模索中.
© 2015 高里 実 Licensed under CC 表示 2.1 日本
(オーストラリアMurdoch Childrens Research Institute)
email:高里 実
DOI: 10.7875/first.author.2015.114
Kidney organoids from human iPS cells contain multiple lineages and model human nephrogenesis.
Minoru Takasato, Pei X. Er, Han S. Chiu, Barbara Maier, Gregory J. Baillie, Charles Ferguson, Robert G. Parton, Ernst J. Wolvetang, Matthias S. Roost, Susana M. Chuva de Sousa Lopes, Melissa H. Little
Nature, 526, 564-568 (2015)
この論文に出現する遺伝子・タンパク質のUniprot ID
要 約
ヒトの腎臓は最大で約200万個のネフロンから構成され,血液のろ過,電解質やpHの調節,体内の水分量のバランスを担う重要な器官である.腎臓の発生は2種類の前駆細胞である尿管芽と後腎間葉の相互作用により進行する.尿管芽はおもに集合管,後腎間葉はそれ以外の部分のネフロンへと分化するが,両者とも中間中胚葉に由来する細胞である.近年,種々の報告により,尿管芽はとくに前方中間中胚葉,後腎間葉は後方中間中胚葉に由来することが認識されつつある.筆者らは,この研究において,個体の発生における中間中胚葉の前後軸の形成の機序をモデルとして,尿管芽および後腎間葉をヒトのiPS細胞から任意の割合で分化させることに成功した.この手法を用いて作製された腎臓のオルガノイドはすべての構成要素を含むネフロンをもち,血管系や腎臓間質も同時に発生していた.次世代シークエンサーを用いた解析により,腎臓のオルガノイドとヒトの胎生期における各種の臓器とで転写産物のプロファイルを比較したところ,腎臓のオルガノイドは妊娠3カ月目の胎児の腎臓と近似していた.腎臓のオルガノイドの内部に発生した近位尿細管はエンドサイトーシスによるタンパク質の再吸収が可能で,尿細管としての機能をもっていた.さらに,腎臓のオルガノイドに腎臓に対する毒性をもつシスプラチンを処理したところ,近位尿細管に特異的な細胞死が確認された.この研究においてヒトのiPS細胞から作製された腎臓のオルガノイドは,腎臓のすべての組織をもちあわせていたうえ,in vitroにおいてヒトの腎臓の発生を模倣する系であり,将来的には,腎臓に対する毒性の試験,腎臓の病態モデルの確立,細胞療法などへの応用が期待される.
はじめに
腎臓は中胚葉系の器官であり,その由来は原始線条にさかのぼる.原始線条は脊椎動物の発生の初期,原腸陥入期にエピブラストの片側に出現する線状の構造体で,前部原始線状は内胚葉への分化能をもち,後部原始線状は沿軸中胚葉,中間中胚葉,側板中胚葉のいずれかの体幹中胚葉に分化する.腎臓のもとになる中間中胚葉はウォルフ管と腎間葉へと分化し,それぞれ,尿管芽と後腎間葉の2種類の前駆細胞へと分化するとされている.しかし近年,マウスの胚の詳細な解析により,ウォルフ管と腎間葉は中間中胚葉において前後に離れて発生することが認識されはじめた1,2).これによると,ウォルフ管は胚の前方の中間中胚葉から発生し,そののち後方へと伸長する.一方,腎間葉は後方中間中胚葉から発生し,前方から伸長してきたウォルフ管と隣接し尿管芽の侵入をうける.腎臓の発生はこの尿管芽と後腎間葉の接触により開始される.以前に筆者らは,尿管芽および後腎間葉をヒトのES細胞から同時に分化させる手法について報告したが3),本来は由来の異なる2種類の前駆細胞をなぜ同時に分化させることができるのかについて疑問が残っていた.その謎を解くには,体幹中胚葉においてどのように前後軸が形成されるのかについて理解する必要があった.
ニワトリの胚の観察によると,成長にともない胚が前後に伸長していく際には,胚の尾部(後方)に位置する原始線状から細胞がつぎつぎと分裂し,胚の体幹(前方)へと送り出される4).これは,さきに体幹へと送り出された細胞が体幹中胚葉の前方に位置し,のちに送り出された細胞は後方に位置することを意味する.では,移動を開始する時期により細胞の運命が左右されるのはどのような機序によるものであろうか.胚の前後軸の形成を支配するモルフォゲンとして,胚の前方において産生されるレチノイン酸,中間中胚葉への分化を誘導するFGF9,胚の尾部において発現するWNTが知られている.ここから筆者らは,原始線状から最初に前方へと移動した細胞は早期にレチノイン酸やFGF9に暴露されるがゆえに前方中間中胚葉へと分化する一方,遅れて移動した細胞はより長いあいだWNTシグナルに影響されるがゆえに後方中間中胚葉へと分化するという,中間中胚葉の前後軸の形成のモデルを仮定した5)(図1).そして,この仮説がヒトの多能性幹細胞から中胚葉への分化においても適用されるのかiPS細胞を用いて検証した.
1.前方中間中胚葉と後方中間中胚葉の選択的な誘導
筆者らは,さきの報告において,ヒトの多能性幹細胞をWNTシグナル刺激物質により数日間にわたり処理することで後部原始線条へと分化させ,そののち,FGF9の処理により中間中胚葉へと分化させた3).この手法は,胚における尾部の古典的WNTシグナルおよび体幹のFGF9シグナルを模倣した系である.そこで,この分化誘導系を使い,最初のWNTシグナル刺激物質による処理の期間を変化させる,つまり,細胞へFGF9の曝露が開始される時期を前後させることにより,前方中間中胚葉と後方中間中胚葉を選択的に分化させることができるかどうか検証した.実験では,ヒトのiPS細胞を4通りの処理期間にわたり培養したのち,FGF9の添加により中間中胚葉を分化させその違いを調べた.すると,短期間の処理からは前方中間中胚葉が分化し,逆に,長期間の処理からは後方中間中胚葉が分化した.これらの中間中胚葉を2次元培養しつづけると,前方中間中胚葉からは尿管芽細胞が発生し,後方中間中胚葉からは後腎間葉が発生した.一方,中期間の処理からは両方の中間中胚葉が同時に分化した.また,レチノイン酸が中間中胚葉の発生にあたえる影響について検証するため,FGF9の処理と同時にレチノイン酸あるいはレチノイン酸阻害剤を添加したところ,レチノイン酸は前方中間中胚葉の分化を促進した一方,レチノイン酸阻害剤はそれを阻害し,逆に,後方中間中胚葉の分化を促進した.以上より,原始線条細胞が体幹の方向へと移動する時間差が前方中間中胚葉および後方中間中胚葉の細胞運命を決定するというモデルは,ヒトのiPS細胞の分化誘導系にも適用されることが確認された.
2.腎臓のオルガノイドの作製
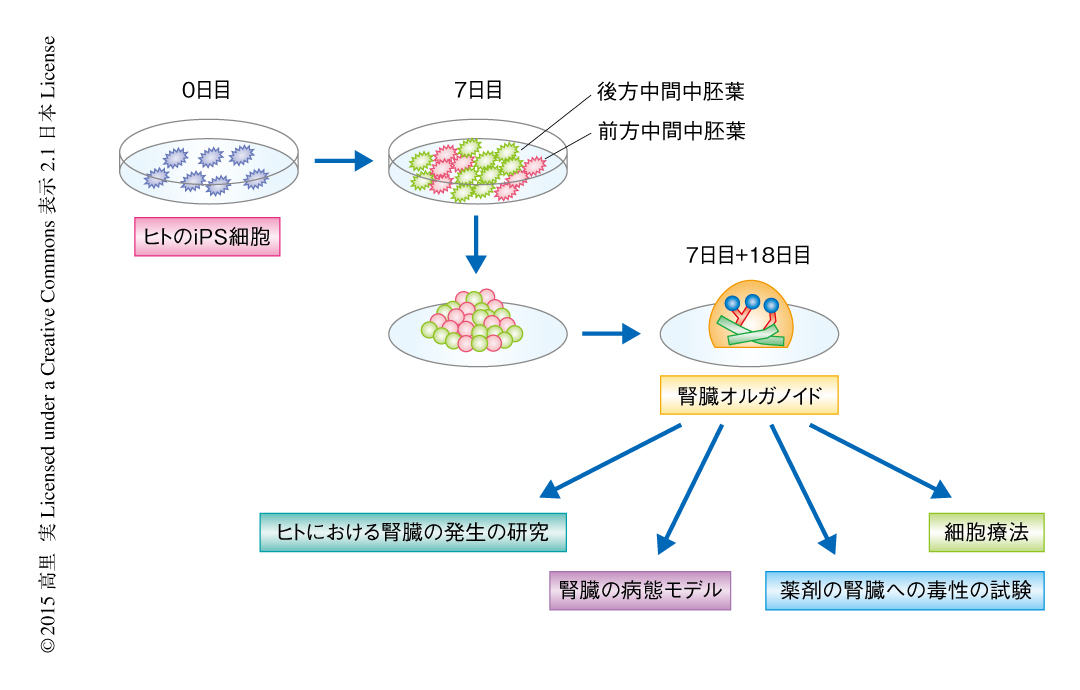
この結果をふまえ,尿管芽と後腎間葉とを同時に分化させることのできるWNTシグナル刺激物質による4日間の処理の系を用いて腎臓のオルガノイドの作製を試みた.分化の開始から7日後(3日間のFGF9の処理)に細胞を培養皿より分離し,遠心分離により試験管内において再集合体を形成させたのち,メンブレンフィルターのうえで最長で20日間にわたり3次元培養をした.再集合体は時間の経過とともに成長し,3日目には豆状の腎包の形成がみられ,11日目には複雑なネフロンを自発的に構築する直径3~5 mm程度のオルガノイドが形成された.オルガノイドの内部には糸球体,近位尿細管,遠位尿細管,集合管の4つの構成要素をもつネフロンが特徴的な方向性をもち発生していた(図2).実際の腎臓の内部では皮質に糸球体,髄質に集合管が配置されているが,腎臓のオルガノイドでも同様に,底面に枝分かれした集合管が形成され,それが上方の遠位尿細管および近位尿細管へと伸びていき,最上面において糸球体へと終着していた.マウスの後腎間葉細胞を高濃度の古典的WNTシグナルにより刺激するとin vitroにおいてもネフロンへと分化することが知られているが6),オルガノイドにおいても初期における高濃度のWNTシグナル刺激物質による短時間の刺激により最大数のネフロンが形成された.作製された腎臓オルガノイドにおける遺伝子発現プロファイルを調べるため,次世代シークエンサーを用いたRNA-seq法により時系列にトランスクリプトームを解析した.その結果,オルガノイドの形成の過程において,まず腎臓前駆細胞のマーカー遺伝子が失われ,つづいて糸球体や尿細管などネフロンの構成要素のマーカー遺伝子の発現が上昇していた.また,ヒトの胎児の各種の臓器から得られた21のトランスクリプトームのデータセットと比較したところ7),ヒトのiPS細胞から作製された腎臓オルガノイドは妊娠3カ月目の胎児の腎臓にもっとも近似していることがわかった.
3.腎臓オルガノイドの内部の組織
生体の腎臓においてはネフロンをとりかこむ腎臓間質には血管が発達している.体内の血液を濾過する役割をもつ腎臓にとり,これら血管の発生は非常に重要である.中間中胚葉は後腎間葉になるだけではなく,腎臓間質細胞や血管内皮細胞にも分化することが知られているため8),ヒトのiPS細胞から中間中胚葉を経由して分化した腎臓オルガノイドに血管系が存在していても不思議ではない.実際に,オルガノイドのネフロンのあいだには腎臓間質細胞が充満しており,そのなかで血管内皮細胞が血管網を形成していた.腎臓間質細胞は血管周皮細胞や糸球体のメザンギウム細胞に分化するが9),オルガノイドにおいても血管周皮細胞や糸球体のメザンギウム細胞が確認された.オルガノイドにみられたPDGFRA陽性のメザンギウム細胞はヒトの胎児期の腎臓においてごく初期の糸球体に存在するもので10),オルガノイドの糸球体が発生の初期の段階にあることが示唆された.透過型電子顕微鏡による観察により,それら初期の糸球体においては足細胞が足突起を糸球体の基底膜へと伸ばしているようすが確認されたが,糸球体の内部には血管系が発達していないためスリット膜は観察されなかった.ただし,一部の糸球体においては血管内皮細胞の侵入がみられ,今後,最適化された培養条件においては血管化された糸球体が形成される可能性が示唆された.また,透過型電子顕微鏡での観察によると,オルガノイドの近位尿細管および遠位尿細管はそれぞれに特徴的な管腔の構造,すなわち,近位尿細管の刷子縁および遠位尿細管の比較的平らな内皮と短い微絨毛をもっていた.これらの結果より,ヒトのiPS細胞から分化させた腎臓オルガノイドは,ネフロンのみならず間質や血管系といった腎臓の発生に必要な組織をすべて内包していることがわかった.
4.腎臓オルガノイドの機能性
ヒトのiPS細胞から作製された腎臓オルガノイドが将来的に腎臓に対する毒性の試験や腎臓の病態モデルに利用できるかどうかは,ネフロンの機能的な成熟度しだいである.これを調べるため,腎臓においてビタミン,ホルモン,アミノ酸の再吸収を担う近位尿細管に焦点をしぼり解析した.近位尿細管における再吸収はおもにCubilinおよびMegalinの2種類の膜タンパク質を介したエンドサイトーシスによる.その発現を調べたところ,オルガノイドの近位尿細管は管腔側の膜においてCubilinを発現していた.また,蛍光標識したデキストランをオルガノイドの培養液に24時間にわたり添加したところ,デキストランは近位尿細管に特異的に取り込まれ,近位尿細管はほかの細胞よりもより活発にエンドサイトーシスを行っていることがわかった.
近位尿細管はその表面に薬物を取り込むさまざまなトランスポーターを発現しているため,薬剤のもつ毒性におかされやすく,とくに,新薬の開発の段階において腎臓に対する毒性を試験できる系の開発は社会的な要請が大きい.抗がん剤であるシスプラチンは腎臓に対し毒性をもつ薬剤のひとつであり,人体に対する長期間あるいは高濃度の使用により副作用として近位尿細管にアポトーシスをひき起こす11).この毒性がオルガノイドの近位尿細管においても再現できるかどうか調べるため,さまざまな濃度のシスプラチンを培養液に添加し,24時間後にアポトーシスの進行の指標である切断型カスパーゼ3の免疫染色を行った.その結果,高濃度のシスプラチンはオルガノイドの内部のあらゆる細胞にアポトーシスをひき起こしたが,低濃度のシスプラチンは近位尿細管のとくに成熟した部分に有意にアポトーシスをひき起こすことがわかった.この結果から,腎臓オルガノイドの近位尿細管は機能的にある程度まで成熟しており,将来的には,腎臓に対する毒性の試験に利用できる可能性が示された.
おわりに
この研究においては,中間中胚葉の前後軸の形成の分子機構を解き明かすことにより,ヒトのiPS細胞から腎臓が本来もつ構造的な複雑性をもつオルガノイドの作製に成功した.オルガノイドはすべての構成要素からなるネフロン,および,血管系や腎臓間質などの周辺組織も内包し,その遺伝子発現プロファイルはヒトの胎生期の腎臓と類似していた.一方,その成熟度に関してはさらなる改善の余地のあることは明らかであった.胎児期ではなく成人の腎臓であること,糸球体において毛細血管が発達していること,尿を腎臓から排出する出口となる尿管をもつこと,十分な大きさと数のネフロンをもつことなど,少なくともこれらすべての課題が達成されなければ腎臓オルガノイドを移植に利用することはむずかしい.とはいえ,移植のほかにも腎臓オルガノイドの利用価値はある.この研究においては,薬剤の腎臓に対する毒性の試験に利用できる可能性が示されたが,ほかにも,先天的な腎臓疾患をもつ患者の細胞から作製したiPS細胞を使ってその病態を腎臓オルガノイドにおいて再現できれば,疾患の発症機構の解明につなげることができる.あるいは,腎臓オルガノイドの内部の特定の細胞を単離すれば細胞療法に使用できるかもしれない.また,純粋にヒトの腎臓の発生の分子機構を解明するツールとしても利用できるだろう(図2).
文 献
- Taguchi, A., Kaku, Y., Ohmori, T. et al.: Redefining the in vivo origin of metanephric nephron progenitors enables generation of complex kidney structures from pluripotent stem cells. Cell Stem Cell, 14, 53-67 (2014)[PubMed]
- Xu, J., Wong, E. Y. M., Cheng, C. et al.: Eya1 interacts with Six2 and Myc to regulate expansion of the nephron progenitor pool during nephrogenesis. Dev. Cell, 31, 434-447 (2014)[PubMed]
- Takasato, M., Er, P. X., Becroft, M. et al.: Directing human embryonic stem cell differentiation towards a renal lineage generates a self-organizing kidney. Nat. Cell Biol., 16, 118-126 (2014)[PubMed]
- Sweetman, D., Wagstaff, L., Cooper, O. et al.: The migration of paraxial and lateral plate mesoderm cells emerging from the late primitive streak is controlled by different Wnt signals. BMC Dev. Biol., 8, 63 (2008)[PubMed]
- Takasato, M. & Little, M. H.: The origin of the mammalian kidney: implications for recreating the kidney in vitro. Development, 142, 1937-1947 (2015)[PubMed]
- Park, J., Ma, W., O’Brien, L. L. et al.: Six2 and Wnt regulate self-renewal and commitment of nephron progenitors through shared gene regulatory networks. Dev. Cell, 23, 637-651 (2012)[PubMed]
- Roost, M. S., van Iperen, L., Ariyurek, Y. et al.: KeyGenes, a tool to probe tissue differentiation using a human fetal transcriptional atlas. Stem Cell Reports, 4, 1112-1124 (2015)[PubMed]
- Mugford, J. W., Sipila, P., McMahon, J. A. et al.: Osr1 expression demarcates a multi-potent population of intermediate mesoderm that undergoes progressive restriction to an Osr1-dependent nephron progenitor compartment within the mammalian kidney. Dev. Biol., 324, 88-98 (2008)[PubMed]
- Kobayashi, A., Mugford, J. W., Krautzberger, A. M. et al.: Identification of a multipotent self-renewing stromal progenitor population during mammalian kidney organogenesis . Stem Cell Reports, 3, 650-662 (2014)[PubMed]
- Floege, J., Hudkins, K. L., Seifert, R. et al.: Localization of PDGF α-receptor in the developing and mature human kidney. Kidney Int., 51, 1140-1150 (1997)[PubMed]
- Cummings, B. S. & Schnellmann, R. G.: Cisplatin-induced renal cell apoptosis: caspase 3-dependent and -independent pathways. J. Pharmacol. Exp. Ther., 302, 8-17 (2002)[PubMed]
著者プロフィール
略歴:2008年 東京大学大学院理学系研究科博士課程 修了,同年 研究員,2009年 オーストラリアQueensland大学 研究員を経て,2015年よりオーストラリアMurdoch Childrens Research Institute上級研究員.
研究テーマ:ヒトの多能性幹細胞を使った腎臓の分化誘導系の開発.
関心事:基礎研究の成果をいかに医療への応用へとつなげるか,を模索中.
© 2015 高里 実 Licensed under CC 表示 2.1 日本