新奇の環境における海馬の発火パターンの形成はシナプス可塑性により制御される
北西 卓磨
(ノルウェーNorwegian University of Science and Technology,Kavli Institute for Systems Neuroscience)
email:北西卓磨
DOI: 10.7875/first.author.2015.079
Novelty-induced phase-locked firing to slow gamma oscillations in the hippocampus: requirement of synaptic plasticity.
Takuma Kitanishi, Sakiko Ujita, Mehdi Fallahnezhad, Naomi Kitanishi, Yuji Ikegaya, Ayumu Tashiro
Neuron, 86, 1265-1276 (2015)
ニューロンの正確な発火のタイミングは脳における情報処理において重要である.ガンマ波という脳波に位相固定した精密な発火パターンは,ニューロンどうしの相互作用を促進し学習など高次の脳機能に寄与すると考えられている.しかし,ガンマ波への位相固定を制御する細胞機構については,これまで理解が進んでいなかった.筆者らは,この課題に取り組むため,ウイルスベクターによる局所における遺伝子の改変とマルチユニット記録法とを組み合わせた新たな手法を開発した.そして,海馬CA1野におけるGluR1に依存的なシナプス可塑性は,海馬CA3野から海馬CA1野へと伝達される“遅いガンマ波”への位相固定,および,場所細胞の活動のすばやい形成に必要な細胞機構であることを見い出した.さらに,こうした結果から,海馬CA1野におけるシナプス可塑性は,新奇の経験の際に海馬CA3野→海馬CA1野→嗅内皮質という投射経路にそった情報伝達を促進する細胞機構であることも示唆された.
ニューロンは短い電気的なパルスを発して情報を伝達する.この発火活動はミリ秒の時間精度で生じ,こうした正確な発火のタイミングは脳における適切な情報処理に欠かせない.発火のタイミングを精密に制御するしくみとして,位相固定という現象が知られている.これは,局所におけるフィールド電位である脳波の振動に対し特定の位相で発火するように,ニューロンの発火のタイミングが制御される現象である.海馬をふくめた脳の広い範囲においてガンマ波という脳波が観察される.ガンマ波の周期は10~30ミリ秒であるため,特定のガンマ波に位相固定したニューロンの集団の発火活動は同期性が高く,下流の領域を強力に興奮させる.そのため,ガンマ波への位相固定は領域のあいだの情報伝達を促進し,記憶や学習など高次機能において重要な役割をはたすと考えられている1).
ガンマ波への位相固定はどのような細胞機構により制御されているのだろうか? ニューロンへの興奮性と抑制性のシナプス入力のバランスがガンマ波への位相固定に寄与すると考えられてきたが2),その詳細な機構は不明であった.筆者らは,学習などにより生じるシナプス可塑性が3,4),シナプス入力のバランスを変調することにより位相固定を制御すると考えた.そこで,生きた動物において海馬におけるシナプス可塑性を抑制し,これらのニューロンにおける発火パターンを調べることによりこの仮説を検証した.
ところが,薬理学的な手法や遺伝子改変マウスの利用などシナプス可塑性を阻害する一般的な手法は,脳の広い範囲の神経活動に影響し動物の認知や行動にも変化をきたす5-7).こうした脳の全体への影響が生じると,記録された発火パターンの変化は,記録しているニューロンにおけるシナプス可塑性の阻害により直接に生じたのか全身性の変化により間接的に生じたのか,区別がむずかしくなってしまう.そこで,筆者らは,局所における遺伝子の改変とマルチユニット記録法とを組み合わせた新たな手法を考案した.具体的には,シナプス可塑性を阻害するウイルスベクターを海馬CA1野に局所的に注入し,自由に行動している動物からマルチユニット記録法を用いてこのウイルスベクターにより改変された領域の神経活動を一斉に計測した.この手法では,海馬CA1野の大部分や周辺の領域におけるシナプス可塑性は損なわれないので,正常な脳の機能のもとでシナプス可塑性と発火パターンとの因果性を追求することが可能になった.
シナプス可塑性を局所的に阻害するため,GluR1のC末端側の断片の遺伝子を発現するアデノ随伴ウイルスベクターを作製した.GluR1のC末端側の断片はGluR1サブユニットを含むAMPA受容体のシナプスへの輸送を阻害しシナプスの長期増強を抑制する8).このウイルスベクターをラットの海馬CA1野に注入することにより,局所的(背側CA1野の20%)かつ高効率(注入した部位の周辺の95%の錐体細胞)で,錐体細胞に選択的な遺伝子導入を実現した.ウイルスベクターを導入した部位の急性切片を作製してシナプス可塑性への効果を調べたところ,GluR1のC末端側の断片は長期増強を抑制することが確認された.
自由に行動する動物においてシナプス可塑性を阻害した海馬CA1野の神経活動を計測するためマルチユニット記録法を用いた.マルチユニット記録法とは,ねらった脳の部位から脳波と個々のニューロンの発火活動とをリアルタイムに計測できる多細胞同時記録法である.片側のCA1野にはGluR1のC末端側の断片の遺伝子を発現するウイルスベクターを,反対側のCA1野には対照としてGFPの遺伝子を発現するウイルスベクターを注入し,両側のCA1野から同時に神経活動を計測した.
海馬は空間の認識および記憶に重要な部位である.そこで,動物に慣れた環境あるいは新奇の環境を探索させ,その際の神経活動について解析することにした.探索行動の際に海馬において観察されるおもな脳波にはシータ波とガンマ波がある.海馬CA1野において観察されるガンマ波には海馬CA3野→海馬CA1野と伝達される“遅いガンマ波”と,内側嗅内皮質→海馬CA1野と伝達される“速いガンマ波”の2種類がある9).GluR1のC末端側の断片の局所的な発現はこれらすべての脳波の強度や波形には影響しなかった.したがって,この研究では,脳波は正常に保たれた状態でシナプス可塑性と発火活動との因果関係を調べることが可能になった.
ガンマ波に対する個々のニューロンの発火パターンについて調べた.対照のニューロンは,既存の報告と一致して,遅いガンマ波や速いガンマ波に位相固定した発火パターンを示した.ところが,GluR1のC末端側の断片を発現させることによりシナプス可塑性を阻害した海馬CA1野においては,速いガンマ波への位相固定は保たれたのに対し,遅いガンマ波への位相固定は失われた(図1a).
シナプス可塑性は学習の際に情報を獲得するための細胞機構だと考えられている.そこで,動物に新たな空間情報を学習させるために新奇の環境を体験させたときのガンマ波への位相固定について調べた.対照の海馬CA1野では,動物が新奇環境に入ると遅いガンマ波の強度が一過的に増し,このガンマ波への位相固定も増強した.一方,GluR1のC末端側の断片を発現させた海馬CA1野では,遅いガンマ波の強度は同様に増したものの,位相固定の増強は失われた.速いガンマ波については新奇の環境において強度も位相固定も変化せず,GluR1のC末端側の断片の発現もこれらに影響しなかった.こうした結果から,新奇の経験により遅いガンマ波への位相固定が一時的に増強され,この増強にはシナプス可塑性が必要であることが示された.
海馬には動物が環境のなかで特定の位置にいるときにのみ発火するニューロンがあり,これらは場所細胞とよばれている10)(北西卓磨・松尾直毅, 海馬体-嗅内皮質における空間認知システム. 領域融合レビュー, 4, e001, 2015 も参照されたい).動物が新奇の環境におかれると,新たな場所細胞の活動パターンがすばやく形成され長期間にわたり維持される.こうした発火パターンの形成と維持は空間情報の獲得と維持の過程を反映すると考えられている.そこで,シナプス可塑性の阻害により遅いガンマ波への位相固定が失われた状態は,場所細胞としての発火パターンにどう影響するか調べた.
動物を慣れ親しんだ環境においた場合には,GluR1のC末端側の断片を発現した領域においても,対照と同じ程度に精密な場所細胞の活動が観察された.このことから,すでに形成された場所細胞の活動の維持および発現にはシナプス可塑性は不要だと考えられた.動物を新奇の環境におくと,対照のニューロンにおいては精密な場所細胞の活動がすばやく形成されたのに対し,GluR1のC末端側の断片を発現させた領域のニューロンは,より広い領域で発火するという空間的な選択性の低い場所細胞の活動を示した(図1b).新奇の環境を複数回にわたり経験させると,GluR1のC末端側の断片を発現させた領域においてもしだいに精密な場所細胞の活動が形成された.
場所細胞の活動の形成の過程をよりくわしく調べるため,新奇の環境において最初の10分間の発火活動のデータを2分ごとに区切って解析した.対照のニューロンにおいては最初の10分間のあいだに環境のなかの特定の位置での発火率がしだいに上昇することにより空間選択的な発火パターンが形成されていた.一方,GluR1のC末端側の断片を発現させたニューロンにおいては,最初の2分間の発火率が対照のニューロンに比べ低く,遅れて発火率が上昇することがわかった.こうした結果から,シナプス可塑性は精密な場所細胞の活動をすばやく形成するために必要な細胞機構であることが示された.
遅いガンマ波への位相固定と場所細胞の活動の形成は,密接に関連した切り離せない現象なのだろうか,それとも,シナプス可塑性により制御されるものの,それ以外には関連のない独立な現象だろうか? このヒントを得るため,個々のニューロンの位相固定の強さと場所細胞の活動の精密さとの相関について調べた.すると,遅いガンマ波への位相固定が新奇の環境において強いニューロンほど,精密な場所細胞の活動を形成することがわかった.また,この相関はGluR1のC末端側の断片を発現させても保たれた.したがって,遅いガンマ波への位相固定と場所細胞の活動はなんらかの機構により密接に結びついた現象である可能性が考えられた.
この研究により,GluR1に依存的なシナプス可塑性が,遅いガンマ波への位相固定と場所細胞の活動という2種類の発火パターンの形成を制御する細胞機構であることが明らかにされた.また,遅いガンマ波は海馬CA3野→海馬CA1野,速いガンマ波は内側嗅内皮質→海馬CA1野と伝達されることを考慮すると,シナプス可塑性は海馬CA3野→海馬CA1野→嗅内皮質という投射経路にそった情報伝達を促進する役割をもつことも示唆された.この研究により,新奇の経験にともなう海馬回路の活動の一連の流れが明らかにされ,この回路の活動を制御する鍵がシナプス可塑性であることが示された.
ニューロンの発火パターンはシナプス入力とニューロンそれ自体の細胞機構により決まる.細胞機構を調べるには,シナプス入力は正常に保ちつつニューロンの性質を操作する必要がある.しかし,脳の広い範囲に影響する一般的な操作手法ではこれを実現することはむずかしい.この研究においては,局所における遺伝子改変とマルチユニット記録とを組み合わせることによりこの課題を解決した.この手法は,自由行動をしている動物の脳の活動をささえる細胞基盤を調べるための汎用的な手段になりうる.たとえば,RNAi法をもちいて任意の遺伝子をノックダウンし発火活動への影響を調べることもできる.こうしたアプローチをさらにおし進めることにより,分子レベルあるいは細胞レベルからのボトムアップな情報処理の理解に貢献したい.
略歴:2009年 東京大学大学院薬学系研究科 修了,同年 ノルウェーNorwegian University of Science and Technology博士研究員,2013年 京都大学生命科学系キャリアパス形成ユニット 研究員を経て,2014年より大阪大学大学院医学系研究科 研究員.
研究テーマ:海馬における情報処理の機構.
関心事:脳に流れる情報を手にとるようにみたい.
© 2015 北西 卓磨 Licensed under CC 表示 2.1 日本
(ノルウェーNorwegian University of Science and Technology,Kavli Institute for Systems Neuroscience)
email:北西卓磨
DOI: 10.7875/first.author.2015.079
Novelty-induced phase-locked firing to slow gamma oscillations in the hippocampus: requirement of synaptic plasticity.
Takuma Kitanishi, Sakiko Ujita, Mehdi Fallahnezhad, Naomi Kitanishi, Yuji Ikegaya, Ayumu Tashiro
Neuron, 86, 1265-1276 (2015)
要 約
ニューロンの正確な発火のタイミングは脳における情報処理において重要である.ガンマ波という脳波に位相固定した精密な発火パターンは,ニューロンどうしの相互作用を促進し学習など高次の脳機能に寄与すると考えられている.しかし,ガンマ波への位相固定を制御する細胞機構については,これまで理解が進んでいなかった.筆者らは,この課題に取り組むため,ウイルスベクターによる局所における遺伝子の改変とマルチユニット記録法とを組み合わせた新たな手法を開発した.そして,海馬CA1野におけるGluR1に依存的なシナプス可塑性は,海馬CA3野から海馬CA1野へと伝達される“遅いガンマ波”への位相固定,および,場所細胞の活動のすばやい形成に必要な細胞機構であることを見い出した.さらに,こうした結果から,海馬CA1野におけるシナプス可塑性は,新奇の経験の際に海馬CA3野→海馬CA1野→嗅内皮質という投射経路にそった情報伝達を促進する細胞機構であることも示唆された.
はじめに
ニューロンは短い電気的なパルスを発して情報を伝達する.この発火活動はミリ秒の時間精度で生じ,こうした正確な発火のタイミングは脳における適切な情報処理に欠かせない.発火のタイミングを精密に制御するしくみとして,位相固定という現象が知られている.これは,局所におけるフィールド電位である脳波の振動に対し特定の位相で発火するように,ニューロンの発火のタイミングが制御される現象である.海馬をふくめた脳の広い範囲においてガンマ波という脳波が観察される.ガンマ波の周期は10~30ミリ秒であるため,特定のガンマ波に位相固定したニューロンの集団の発火活動は同期性が高く,下流の領域を強力に興奮させる.そのため,ガンマ波への位相固定は領域のあいだの情報伝達を促進し,記憶や学習など高次機能において重要な役割をはたすと考えられている1).
ガンマ波への位相固定はどのような細胞機構により制御されているのだろうか? ニューロンへの興奮性と抑制性のシナプス入力のバランスがガンマ波への位相固定に寄与すると考えられてきたが2),その詳細な機構は不明であった.筆者らは,学習などにより生じるシナプス可塑性が3,4),シナプス入力のバランスを変調することにより位相固定を制御すると考えた.そこで,生きた動物において海馬におけるシナプス可塑性を抑制し,これらのニューロンにおける発火パターンを調べることによりこの仮説を検証した.
ところが,薬理学的な手法や遺伝子改変マウスの利用などシナプス可塑性を阻害する一般的な手法は,脳の広い範囲の神経活動に影響し動物の認知や行動にも変化をきたす5-7).こうした脳の全体への影響が生じると,記録された発火パターンの変化は,記録しているニューロンにおけるシナプス可塑性の阻害により直接に生じたのか全身性の変化により間接的に生じたのか,区別がむずかしくなってしまう.そこで,筆者らは,局所における遺伝子の改変とマルチユニット記録法とを組み合わせた新たな手法を考案した.具体的には,シナプス可塑性を阻害するウイルスベクターを海馬CA1野に局所的に注入し,自由に行動している動物からマルチユニット記録法を用いてこのウイルスベクターにより改変された領域の神経活動を一斉に計測した.この手法では,海馬CA1野の大部分や周辺の領域におけるシナプス可塑性は損なわれないので,正常な脳の機能のもとでシナプス可塑性と発火パターンとの因果性を追求することが可能になった.
1.ウイルスベクターを用いたシナプス可塑性の局所的な抑制
シナプス可塑性を局所的に阻害するため,GluR1のC末端側の断片の遺伝子を発現するアデノ随伴ウイルスベクターを作製した.GluR1のC末端側の断片はGluR1サブユニットを含むAMPA受容体のシナプスへの輸送を阻害しシナプスの長期増強を抑制する8).このウイルスベクターをラットの海馬CA1野に注入することにより,局所的(背側CA1野の20%)かつ高効率(注入した部位の周辺の95%の錐体細胞)で,錐体細胞に選択的な遺伝子導入を実現した.ウイルスベクターを導入した部位の急性切片を作製してシナプス可塑性への効果を調べたところ,GluR1のC末端側の断片は長期増強を抑制することが確認された.
2.シナプス可塑性を抑制した領域における神経活動の計測
自由に行動する動物においてシナプス可塑性を阻害した海馬CA1野の神経活動を計測するためマルチユニット記録法を用いた.マルチユニット記録法とは,ねらった脳の部位から脳波と個々のニューロンの発火活動とをリアルタイムに計測できる多細胞同時記録法である.片側のCA1野にはGluR1のC末端側の断片の遺伝子を発現するウイルスベクターを,反対側のCA1野には対照としてGFPの遺伝子を発現するウイルスベクターを注入し,両側のCA1野から同時に神経活動を計測した.
海馬は空間の認識および記憶に重要な部位である.そこで,動物に慣れた環境あるいは新奇の環境を探索させ,その際の神経活動について解析することにした.探索行動の際に海馬において観察されるおもな脳波にはシータ波とガンマ波がある.海馬CA1野において観察されるガンマ波には海馬CA3野→海馬CA1野と伝達される“遅いガンマ波”と,内側嗅内皮質→海馬CA1野と伝達される“速いガンマ波”の2種類がある9).GluR1のC末端側の断片の局所的な発現はこれらすべての脳波の強度や波形には影響しなかった.したがって,この研究では,脳波は正常に保たれた状態でシナプス可塑性と発火活動との因果関係を調べることが可能になった.
3.シナプス可塑性は遅いガンマ波への位相固定を増強する
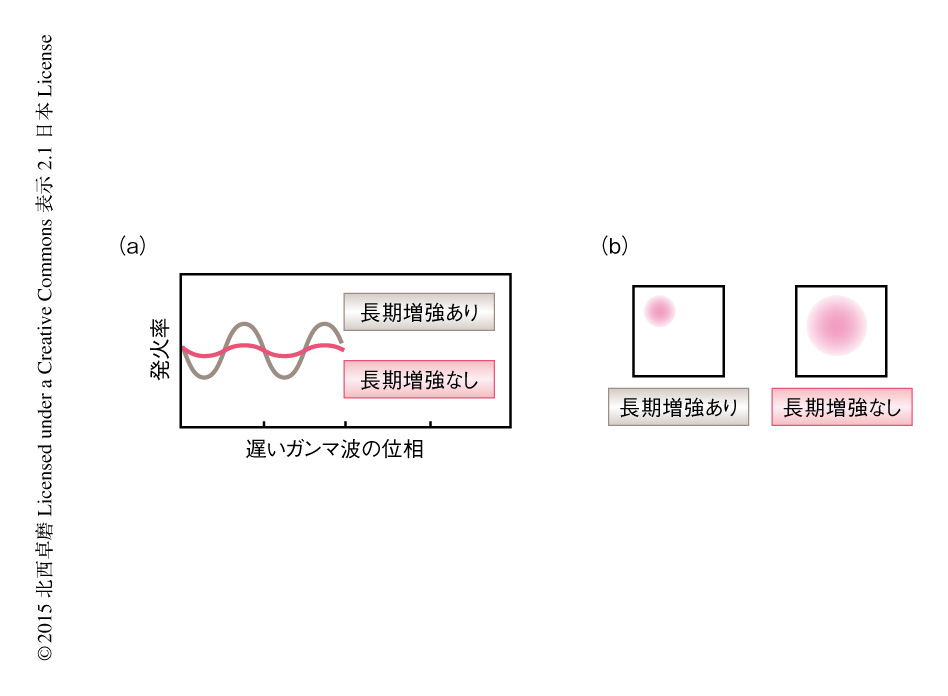
ガンマ波に対する個々のニューロンの発火パターンについて調べた.対照のニューロンは,既存の報告と一致して,遅いガンマ波や速いガンマ波に位相固定した発火パターンを示した.ところが,GluR1のC末端側の断片を発現させることによりシナプス可塑性を阻害した海馬CA1野においては,速いガンマ波への位相固定は保たれたのに対し,遅いガンマ波への位相固定は失われた(図1a).
シナプス可塑性は学習の際に情報を獲得するための細胞機構だと考えられている.そこで,動物に新たな空間情報を学習させるために新奇の環境を体験させたときのガンマ波への位相固定について調べた.対照の海馬CA1野では,動物が新奇環境に入ると遅いガンマ波の強度が一過的に増し,このガンマ波への位相固定も増強した.一方,GluR1のC末端側の断片を発現させた海馬CA1野では,遅いガンマ波の強度は同様に増したものの,位相固定の増強は失われた.速いガンマ波については新奇の環境において強度も位相固定も変化せず,GluR1のC末端側の断片の発現もこれらに影響しなかった.こうした結果から,新奇の経験により遅いガンマ波への位相固定が一時的に増強され,この増強にはシナプス可塑性が必要であることが示された.
4.シナプス可塑性は場所細胞のすばやい形成に寄与する
海馬には動物が環境のなかで特定の位置にいるときにのみ発火するニューロンがあり,これらは場所細胞とよばれている10)(北西卓磨・松尾直毅, 海馬体-嗅内皮質における空間認知システム. 領域融合レビュー, 4, e001, 2015 も参照されたい).動物が新奇の環境におかれると,新たな場所細胞の活動パターンがすばやく形成され長期間にわたり維持される.こうした発火パターンの形成と維持は空間情報の獲得と維持の過程を反映すると考えられている.そこで,シナプス可塑性の阻害により遅いガンマ波への位相固定が失われた状態は,場所細胞としての発火パターンにどう影響するか調べた.
動物を慣れ親しんだ環境においた場合には,GluR1のC末端側の断片を発現した領域においても,対照と同じ程度に精密な場所細胞の活動が観察された.このことから,すでに形成された場所細胞の活動の維持および発現にはシナプス可塑性は不要だと考えられた.動物を新奇の環境におくと,対照のニューロンにおいては精密な場所細胞の活動がすばやく形成されたのに対し,GluR1のC末端側の断片を発現させた領域のニューロンは,より広い領域で発火するという空間的な選択性の低い場所細胞の活動を示した(図1b).新奇の環境を複数回にわたり経験させると,GluR1のC末端側の断片を発現させた領域においてもしだいに精密な場所細胞の活動が形成された.
場所細胞の活動の形成の過程をよりくわしく調べるため,新奇の環境において最初の10分間の発火活動のデータを2分ごとに区切って解析した.対照のニューロンにおいては最初の10分間のあいだに環境のなかの特定の位置での発火率がしだいに上昇することにより空間選択的な発火パターンが形成されていた.一方,GluR1のC末端側の断片を発現させたニューロンにおいては,最初の2分間の発火率が対照のニューロンに比べ低く,遅れて発火率が上昇することがわかった.こうした結果から,シナプス可塑性は精密な場所細胞の活動をすばやく形成するために必要な細胞機構であることが示された.
5.遅いガンマ波への位相固定の強いニューロンほど精密な場所細胞の活動を形成する
遅いガンマ波への位相固定と場所細胞の活動の形成は,密接に関連した切り離せない現象なのだろうか,それとも,シナプス可塑性により制御されるものの,それ以外には関連のない独立な現象だろうか? このヒントを得るため,個々のニューロンの位相固定の強さと場所細胞の活動の精密さとの相関について調べた.すると,遅いガンマ波への位相固定が新奇の環境において強いニューロンほど,精密な場所細胞の活動を形成することがわかった.また,この相関はGluR1のC末端側の断片を発現させても保たれた.したがって,遅いガンマ波への位相固定と場所細胞の活動はなんらかの機構により密接に結びついた現象である可能性が考えられた.
おわりに
この研究により,GluR1に依存的なシナプス可塑性が,遅いガンマ波への位相固定と場所細胞の活動という2種類の発火パターンの形成を制御する細胞機構であることが明らかにされた.また,遅いガンマ波は海馬CA3野→海馬CA1野,速いガンマ波は内側嗅内皮質→海馬CA1野と伝達されることを考慮すると,シナプス可塑性は海馬CA3野→海馬CA1野→嗅内皮質という投射経路にそった情報伝達を促進する役割をもつことも示唆された.この研究により,新奇の経験にともなう海馬回路の活動の一連の流れが明らかにされ,この回路の活動を制御する鍵がシナプス可塑性であることが示された.
ニューロンの発火パターンはシナプス入力とニューロンそれ自体の細胞機構により決まる.細胞機構を調べるには,シナプス入力は正常に保ちつつニューロンの性質を操作する必要がある.しかし,脳の広い範囲に影響する一般的な操作手法ではこれを実現することはむずかしい.この研究においては,局所における遺伝子改変とマルチユニット記録とを組み合わせることによりこの課題を解決した.この手法は,自由行動をしている動物の脳の活動をささえる細胞基盤を調べるための汎用的な手段になりうる.たとえば,RNAi法をもちいて任意の遺伝子をノックダウンし発火活動への影響を調べることもできる.こうしたアプローチをさらにおし進めることにより,分子レベルあるいは細胞レベルからのボトムアップな情報処理の理解に貢献したい.
文 献
- Fell, J. & Axmacher, N.: The role of phase synchronization in memory processes. Nat. Rev. Neurosci., 12, 105-118 (2011)[PubMed]
- Buzsaki, G. & Wang, X. J.: Mechanisms of gamma oscillations. Annu. Rev. Neurosci., 35, 203-225 (2012)[PubMed]
- Whitlock, J. R., Heynen, A. J., Shuler, M. G. et al.: Learning induces long-term potentiation in the hippocampus. Science, 313, 1093-1097 (2006)[PubMed]
- Kitanishi, T., Ikegaya, Y., Matsuki, N. et al.: Experience-dependent, rapid structural changes in hippocampal pyramidal cell spines. Cereb. Cortex, 19, 2572-2578 (2009)[PubMed]
- Morris, R. G., Anderson, E., Lynch, G. S. et al.: Selective impairment of learning and blockade of long-term potentiation by an N-methyl-D-aspartate receptor antagonist, AP5. Nature, 319, 774-776 (1986)[PubMed]
- Tsien, J. Z., Huerta, P. T. & Tonegawa, S.: The essential role of hippocampal CA1 NMDA receptor-dependent synaptic plasticity in spatial memory. Cell, 87, 1327-1338 (1996)[PubMed]
- Resnik, E., McFarland, J. M., Sprengel, R. et al.: The effects of GluA1 deletion on the hippocampal population code for position. J. Neurosci., 32, 8952-8968 (2012)[PubMed]
- Shi, S., Hayashi, Y., Esteban, J. A. et al.: Subunit-specific rules governing AMPA receptor trafficking to synapses in hippocampal pyramidal neurons. Cell, 105, 331-343 (2001)[PubMed]
- Colgin, L. L., Denninger, T., Fyhn, M. et al.: Frequency of gamma oscillations routes flow of information in the hippocampus. Nature, 462, 353-357 (2009)[PubMed]
- O'Keefe, J. & Dostrovsky, J.: The hippocampus as a spatial map. Preliminary evidence from unit activity in the freely-moving rat. Brain Res., 34, 171-175 (1971)[PubMed]
著者プロフィール
略歴:2009年 東京大学大学院薬学系研究科 修了,同年 ノルウェーNorwegian University of Science and Technology博士研究員,2013年 京都大学生命科学系キャリアパス形成ユニット 研究員を経て,2014年より大阪大学大学院医学系研究科 研究員.
研究テーマ:海馬における情報処理の機構.
関心事:脳に流れる情報を手にとるようにみたい.
© 2015 北西 卓磨 Licensed under CC 表示 2.1 日本